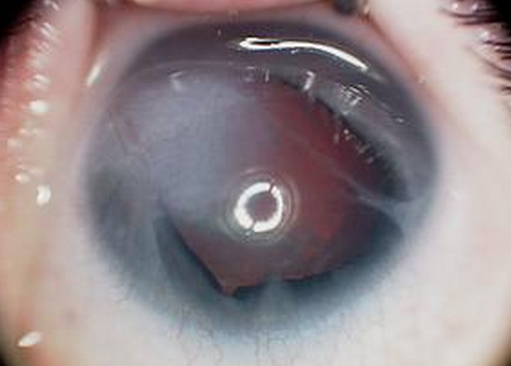
1897年Von Hippel報導1例伴有雙眼角膜中央混濁並與虹膜粘連的牛眼病例。1906年Peter描述了現今稱為Peter異常(Peter anomaly)的一些病例。在1個多世紀以來,對於本病究竟是一種單純的疾病,還是有同一表現的多種疾病構成始終存在爭論。
基本介紹
- 中文名:Peter異常
- 病因:子宮內感染角膜內潰瘍
- 發病機制:角膜後彈力層異常
- 實質:病菌
流行病學,病因,發病機制,臨床表現,併發症,診斷,檢查,治療,預防:,
流行病學
大多數患者有家族遺傳史常染色體隱性遺傳或不規則顯性遺傳,也有散發病例報導。尚缺乏有關發病率等方面的資料。
病因
Peter異常的病因尚不完全了解,但從組織病理學和電鏡發現不同的改變,認為不是單一原因。起初認為是由於子宮內感染(Von Hipple角膜內潰瘍),這種學說認為通過羊水或胎盤獲得子宮內角膜炎,導致角膜穿孔,使虹膜-晶狀體隔前移,造成角膜後缺損,角膜白斑及角膜晶狀體及虹膜角膜粘連。這些改變亦可由深層角膜膿腫引起,膿液向前房內引流無角膜穿孔國外報告在21名患者中有5位母親有先天性角膜中央厚的混濁及中央部前粘連在懷孕的最初3個月有過病毒性特別是風疹感染。還報導一例Peter異常的單眼患者存在先天性巨細胞病毒感染,對側眼為正常眼。用電子顯微鏡檢查了一批Peter異常患者的標本顯示角膜後基質的細胞為慢性炎性細胞,用光鏡檢查被破壞的基質可見不正常的成纖維細胞及組織細胞在伴有晶狀體異常的患者,可能是由於晶狀體泡與表層外胚層分化不完全所致。
發病機制
對Peter異常的發病機制仍有爭論。Tripethi認為中央部角膜的缺陷是由於在胚胎10~14mm時,視杯邊緣第一和第二間葉細胞(mesenchymal cell)停止向內生長;角膜後彈力層異常和內皮細胞的喪失,是由於原發性間葉細胞的缺陷這一缺陷可能進一步受到晶狀體泡分離延遲或分離不全的影響;晶狀體混濁和角膜晶狀體條索的形成,則可能與外胚葉的缺陷有關。總之Peter異常的不同表現是與形成角膜內皮角膜基質和虹膜基質的3期間葉組織不同程度的發育缺陷有關。它可以同時伴有或不伴有晶狀體泡的異常。
Kupfer則用神經嵴細胞遷徙過程中的某種障礙或終末誘導的某種缺陷來解釋包括Peter異常在內的前眼部中胚葉發育不全和繼發性青光眼的各種變化角膜基質的遷徙或終末誘導失常,可導致一系列的角膜混濁及發育異常。內皮細胞的缺陷可以引起後彈力層的缺損以及角膜正常含水量的失調,這種異常的內皮細胞可能格外有“黏”性,從而導致角膜虹膜粘連。虹膜基質的部分或全部消失可對其下的虹膜色素上皮和無色素上皮產生繼發影響,造成一系列的瞳孔異常和色素上皮的缺損如果虹膜基質的缺陷發展到一定程度,足以影響到鄰近組織如晶狀體及其懸韌帶時,即可產生晶狀體異位和前極性白內障小梁內皮的遷徙或終末誘導過程中的障礙,可使正常房水外流阻力發生變異而導致眼壓升高這種眼壓升高不一定和虹膜條索黏在角膜及小樑上的數量成比例。Kupfer等報告一名2歲兒童伴有青光眼,其小梁切除標本的超微結構顯示小梁網有典型的老化改變。另有一些學者認為房水排出阻礙可能由於虹膜角膜角微細的改變所致。另有人發現Peter異常的組織病理學改變及視網膜色素上皮層及脈絡膜後部的完全缺損發現了完全的周邊虹膜前粘連伴有虹膜基質的萎縮,且未見到小梁網和Schlemm管結構。其他一些病例伴有虹膜角膜角的神經嵴細胞的分化不全,呈更典型的Axenfeld異常及Rieger綜合徵。
臨床表現
Peter異常的表現是角膜中央部有先天性白斑,並有相應部位的後基質層及後彈力層缺損。在角膜混濁的部位有自中央到周邊的虹膜粘連8%的患者為雙眼患病。角膜水腫可有可無,白斑厚而大者無法看到前房。由於角膜水腫,早期角膜呈毛玻璃樣外觀並有點狀上皮著色。如角膜水腫加重說明病變進行,且青光眼加重了這種狀況但如眼壓正常則水腫會逐漸消失留下邊界較清楚的角膜瘢痕,並有正常光澤的上皮。雖然角膜緣的硬化常見但周邊角膜常為透明,且受累的角膜很少有血管形成。
虹膜與角膜粘連常位於顳側虹膜睫狀區相應部位有角膜白斑,但其他方位的角膜比較透明。粘連可為局部,也可擴展到360°虹膜睫狀區。
Peter異常者還常伴有全身異常,如有短身材,智力遲滯,唇頜齶裂畸形及耳異常。還有報導有腦癱、小紅痣、無牙、少牙、並指(趾)、屈曲指、短頭畸形、半側面部發育不良、Wilsm瘤、顱面成骨不全,腦積水、無腦、肺發育不全、Dandy-Walker綜合徵、心臟及泌尿生殖系統異常Lowe綜合徵等。
有人將Peter異常分3型:①不伴有角膜晶狀體粘連或白內障;②伴有角膜晶狀體粘連或白內障;③伴有Rieger綜合徵。
併發症
有些患眼可有中央部的角膜晶狀體粘連,伴有淺前房,而有一些為前極性白內障。50%~70%的患眼發生青光眼。此外,Peter異常還可有很多不常見的眼部異常,包括小角膜、小眼球、扁平角膜、角膜硬化虹膜缺損、瞳孔異位、無虹膜、前葡萄腫、小晶狀體、先天性無晶狀體等。
診斷
根據病變累及角膜中央部分、虹膜及晶狀體等上述特徵性的臨床表現不難做出診斷。如有眼壓升高即可診斷合併繼發性青光眼。眼壓的測量最好用Tono-pen眼壓計測定,減少或不受角膜白斑的影響。
鑑別診斷 對新生兒及嬰兒,主要是鑑別中央角膜白斑與其他造成角膜混濁的原因。這些其他的原因是指先天性青光眼、黏多糖症產傷、先天遺傳性角膜營養不良和角膜混濁。產傷所致的角膜混濁,後彈力層的撕裂呈垂直性波紋狀;Peter異常與先天性青光眼不同處還在於角膜直徑無擴大,角膜混濁與透明區有明顯的分界線。當眼壓下降后角膜混濁處不會變透明,並有淺前房;黏多糖症嬰兒角膜混濁為瀰漫性,有小的點狀基質層混濁,在後部混濁比前部更緻密,上皮與內皮均未涉及;先天性遺傳性角膜內皮細胞營養不良不伴有青光眼,角膜混濁均勻前房形成良好,且無明顯虹膜異常;角膜潰瘍穿孔者,虹膜嵌於角膜瘢痕中,而Peter異常的虹膜附於混濁的角膜後面附近,如角膜混濁進展前房狀況更看不清楚,正確診斷就很困難。
檢查
嬰兒發育性角膜疾病的處理比較困難。應儘可能早做全麻下的全面檢查。如可能,拍攝或畫下角膜與視神經形態。測定角膜橫徑、縱徑及混濁大小,並測定視盤C/D縱徑及橫徑值。因患者角膜前部異常,測眼壓時可用眼壓筆或氣動眼壓計還應查A超、B超、ERG及角膜內皮細胞等。
治療
最初用藥物治療青光眼包括局部滴用β腎上腺素能阻斷藥,亦可用擬腎上腺素藥及膽鹼能類藥物。在角膜移植術前如眼壓不能用藥物控制,應採用手術治療。但由於房水排出受阻的原因不詳,Schlemm管可能不存在,對有先天異常的房角可以選用小梁切開術,小梁切除術加抗纖維化藥物可能是最佳選擇。
雙眼角膜混濁很重的患者,在發生嚴重的形覺剝奪性弱視前,早期做穿透性角膜移植術是獲得有用視力的惟一希望。
雙眼晶狀體混濁嚴重的白內障在生後3個月內手術。
雖然顯微手術已有很大進展,但對於角膜移植術的預後仍應謹慎考慮有人回顧了穿透性角膜移植的病例,術後植片成功只達到20%病例,且常有嚴重的合併症。兒童因先天性角膜混濁術後獲得的視力常令人失望因大部分兒童在手術前已有嚴重的弱視。單眼患者雖角膜移植手術成功,戴用角膜接觸鏡但對防止弱視效果不滿意。有些學者反對早期手術因為有些患者角膜有可能恢復透明,如果角膜混濁很局限,周邊角膜透明長期擴瞳或作光學性虹膜切除術可以改進視力,避免角膜移植術所致的危險性。
預防:
預後:預後多不理想。
預防:儘早處理,防止弱視。