鹽酸表柔比星注射液,適應症為用於治療白血病、惡性淋巴瘤、多發性骨髓瘤、乳腺癌、肺癌、軟組織肉瘤、胃癌、結腸直腸癌、、卵巢癌等。
基本介紹
- 藥品名稱:鹽酸表柔比星注射液
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:細胞毒性藥物
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,
成份
本品活性成份化學名稱為:(8S,10S)-10-[(3’-氨基-2’,3’,6’-三脫氧-α-L-阿拉伯吡喃糖基)氧代]-6,8,11-三羥基-8-(羥乙醯基)-1-甲氧基-7,8,9,10-四氫並四苯-5,12-二酮鹽酸鹽
其結構式:
其結構式:
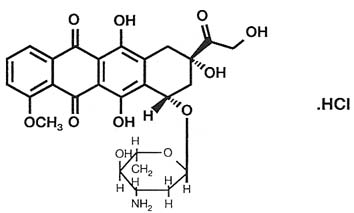
分子式:C27H29NO11·HCl
分子量: 580.0
輔料:氯化鈉,稀鹽酸,注射用水。
性狀
本品為紅色澄明溶液。
適應症
用於治療白血病、惡性淋巴瘤、多發性骨髓瘤、乳腺癌、肺癌、軟組織肉瘤、胃癌、結腸直腸癌、、卵巢癌等。
規格
(1)5ml:10mg;(2)25ml:50mg;(3)50ml:100mg;(4)100ml:200mg。
用法用量
本品應採用緩慢靜脈或動脈內注射,也可加100-250ml氯化鈉注射液點滴。在進行肝動脈插管介入治療時,可用碘化油混和以期増強療效。
常規劑量:表柔比星單獨用藥時成人劑量為60-90mg/m2體表面積,靜脈注射,3-5分鐘內注入體內。根據病人血象可間隔21天重複使用。
高劑量:若單獨使用表柔比星治療肺癌時,應按下述方案給藥:
*未經治療的小細胞肺癌:每天按體表面積120mg/m2,每三周一次。
*未經治療的非小細胞肺癌(鱗狀上皮細胞肺癌、大細胞肺癌或肺腺癌):每天按體表面積135mg/m2,每三周一次;或45mg/m2,每三周的第一、二、三天各一次。
聯合化療時,可參閱阿黴素的聯合化療方案,以相應的較高劑量表柔比星替代阿黴素即可。據國外文獻報導,以CEF-120[環磷醯胺(C):75mg/m2,PO, D1,14;鹽酸表柔比星注射液(E):60mg/m2,IV,D1,8;5-氟脲嘧啶(F):500mg/m2,EV,D1,8]和FEC-100方案組[5-氟脲嘧啶(F):500mg/m2,IV,D1;鹽酸表柔比星注射液(E):100mg/m2,IV,D1;環磷醯胺(C):500mg/m2,IV,D1 較為常用,其中CEF-120方案組尚需額外給予甲氧苄啶-磺胺甲噁唑或氟喹諾酮類抑菌劑治療,並根據血液毒性對劑量進行調整。
本品體外溶血性實驗結果表明本品具有溶血特性,給藥時注意緩慢給藥或緩慢點滴並嚴密監測血象。
特殊人群給藥
肝功能不全者:肝臟為表柔比星的主要代謝途徑,肝功能不全可降低本品的清除率,引起藥物總毒性的增加。故應降低給藥劑量,中度肝功能受損患者(膽紅素1.4~3mg/100ml或BPS滯留量9~15%),藥量應減少50%;重度肝功能受損患者(膽紅素>3mg/100ml或BPS滯留量>15%),藥量應減少75%。
腎功能不全的患者:本品僅有少量經由腎臟排出,故輕、中度腎功能受損患者無需減少劑量,但嚴重腎衰患者(血清肌酐>5mg/ml)應減少給藥劑量。
骨髓功能不全的患者:對因以往化療、放療、老年或骨髓浸潤而造成骨髓造血功能不良的病人,可用小劑量(即常規劑量的60-75mg/m2體表面積,高劑量的105-120mg/m2體表面積)治療。每個療程的總量分2-3次使用。
使用注意
保護措施:接觸本品時,應釆取以下措施:
1.給藥人員應當接受過相關的配液及注射技術培訓。
2.孕婦不應從事接觸本品的工作。
3.給藥人員應穿戴防護衣服、手套,並在接觸本品後予以拋棄。
4.注射時應在指定區域(最好在通風處),並鋪上保護性的廢棄吸水性塑膠紙。
5.所有配液及注射時用過的器具、手套等均應放入高危廢棄袋中高溫焚燒。
一旦發生藥物外溢或泄漏,應給予低濃度的次氯酸鈉(0.1%氯),最好是用肥皂水、水依次沖洗。一旦皮膚或眼睛意外接觸本品,套用大量的清水、肥皂水或碳酸鈉溶液沖洗,眼結膜套用鹽水沖洗。並注意不要傷及皮膚,傷及皮膚時應尋求醫療監護。脫下手套後應立即洗手。
常規劑量:表柔比星單獨用藥時成人劑量為60-90mg/m2體表面積,靜脈注射,3-5分鐘內注入體內。根據病人血象可間隔21天重複使用。
高劑量:若單獨使用表柔比星治療肺癌時,應按下述方案給藥:
*未經治療的小細胞肺癌:每天按體表面積120mg/m2,每三周一次。
*未經治療的非小細胞肺癌(鱗狀上皮細胞肺癌、大細胞肺癌或肺腺癌):每天按體表面積135mg/m2,每三周一次;或45mg/m2,每三周的第一、二、三天各一次。
聯合化療時,可參閱阿黴素的聯合化療方案,以相應的較高劑量表柔比星替代阿黴素即可。據國外文獻報導,以CEF-120[環磷醯胺(C):75mg/m2,PO, D1,14;鹽酸表柔比星注射液(E):60mg/m2,IV,D1,8;5-氟脲嘧啶(F):500mg/m2,EV,D1,8]和FEC-100方案組[5-氟脲嘧啶(F):500mg/m2,IV,D1;鹽酸表柔比星注射液(E):100mg/m2,IV,D1;環磷醯胺(C):500mg/m2,IV,D1 較為常用,其中CEF-120方案組尚需額外給予甲氧苄啶-磺胺甲噁唑或氟喹諾酮類抑菌劑治療,並根據血液毒性對劑量進行調整。
本品體外溶血性實驗結果表明本品具有溶血特性,給藥時注意緩慢給藥或緩慢點滴並嚴密監測血象。
特殊人群給藥
肝功能不全者:肝臟為表柔比星的主要代謝途徑,肝功能不全可降低本品的清除率,引起藥物總毒性的增加。故應降低給藥劑量,中度肝功能受損患者(膽紅素1.4~3mg/100ml或BPS滯留量9~15%),藥量應減少50%;重度肝功能受損患者(膽紅素>3mg/100ml或BPS滯留量>15%),藥量應減少75%。
腎功能不全的患者:本品僅有少量經由腎臟排出,故輕、中度腎功能受損患者無需減少劑量,但嚴重腎衰患者(血清肌酐>5mg/ml)應減少給藥劑量。
骨髓功能不全的患者:對因以往化療、放療、老年或骨髓浸潤而造成骨髓造血功能不良的病人,可用小劑量(即常規劑量的60-75mg/m2體表面積,高劑量的105-120mg/m2體表面積)治療。每個療程的總量分2-3次使用。
使用注意
保護措施:接觸本品時,應釆取以下措施:
1.給藥人員應當接受過相關的配液及注射技術培訓。
2.孕婦不應從事接觸本品的工作。
3.給藥人員應穿戴防護衣服、手套,並在接觸本品後予以拋棄。
4.注射時應在指定區域(最好在通風處),並鋪上保護性的廢棄吸水性塑膠紙。
5.所有配液及注射時用過的器具、手套等均應放入高危廢棄袋中高溫焚燒。
一旦發生藥物外溢或泄漏,應給予低濃度的次氯酸鈉(0.1%氯),最好是用肥皂水、水依次沖洗。一旦皮膚或眼睛意外接觸本品,套用大量的清水、肥皂水或碳酸鈉溶液沖洗,眼結膜套用鹽水沖洗。並注意不要傷及皮膚,傷及皮膚時應尋求醫療監護。脫下手套後應立即洗手。
不良反應
除骨髓抑制和心臟毒性(注意事項項下已描述)以外,其它不良反應如下:
血液和淋巴系統障礙:
大量的未接受過治療的各種實體瘤患者使用大劑量的表柔比星是安全的,發生不良反應情況與常規劑量沒有差異,多數患者發生的可逆性重度中性粒細胞減少症除外(中性粒細胞<500/mm3持續<7天)。大劑量用藥時發生的重度感染併發症,僅少數患者需要入院治療和支持性治療。
很常見>10%
骨髓抑制、粒細胞減少、白細胞減少、血小板減少,中性粒細胞減少。
常見>1%
貧血、出血,
少見:
有報導說同時接受表柔比星和DNA毒性抗癌藥物治療的患者可出現繼發性急性骨髓白血病,這種病例可以有一個短的潛伏期(1-3年),可以經過或不經過前白血病病變期。
免疫系統障礙
少見:
後遺症包括骨髓抑制、發熱、感染、肺炎、膿毒症、敗血症休克、出血,可能發生組織缺氧甚至導致死亡。偶見發熱、膿毒症、感染性高熱、寒戰和尋麻疹的報導;可能發生過敏反應。
迷路神經障礙:
很常見>10%
噁心
心臟異常
常見>1%
心臟毒性
胃腸功能失調:
很常見>10%
開始用藥後5-10天可能出現黏膜炎,常伴有疼痛糜爛部位口炎,主要沿舌邊緣和舌下黏膜生長。
常見>1%
噁心,嘔吐和腹瀉
皮膚異常:
很常見>10%
60-90%用藥患者出現脫髮,該症通常可逆;男性患者伴有鬍鬚生長減少。
不常見>0.1%
皮膚對光過敏
皮膚色素沉著
尋麻疹不常見
膀胱內給藥時,由於藥物吸收減少,系統副作用少見;更常見為化學性膀胱炎,出血性膀胱炎時有發生。
血液和淋巴系統障礙:
大量的未接受過治療的各種實體瘤患者使用大劑量的表柔比星是安全的,發生不良反應情況與常規劑量沒有差異,多數患者發生的可逆性重度中性粒細胞減少症除外(中性粒細胞<500/mm3持續<7天)。大劑量用藥時發生的重度感染併發症,僅少數患者需要入院治療和支持性治療。
很常見>10%
骨髓抑制、粒細胞減少、白細胞減少、血小板減少,中性粒細胞減少。
常見>1%
貧血、出血,
少見:
有報導說同時接受表柔比星和DNA毒性抗癌藥物治療的患者可出現繼發性急性骨髓白血病,這種病例可以有一個短的潛伏期(1-3年),可以經過或不經過前白血病病變期。
免疫系統障礙
少見:
後遺症包括骨髓抑制、發熱、感染、肺炎、膿毒症、敗血症休克、出血,可能發生組織缺氧甚至導致死亡。偶見發熱、膿毒症、感染性高熱、寒戰和尋麻疹的報導;可能發生過敏反應。
迷路神經障礙:
很常見>10%
噁心
心臟異常
常見>1%
心臟毒性
胃腸功能失調:
很常見>10%
開始用藥後5-10天可能出現黏膜炎,常伴有疼痛糜爛部位口炎,主要沿舌邊緣和舌下黏膜生長。
常見>1%
噁心,嘔吐和腹瀉
皮膚異常:
很常見>10%
60-90%用藥患者出現脫髮,該症通常可逆;男性患者伴有鬍鬚生長減少。
不常見>0.1%
皮膚對光過敏
皮膚色素沉著
尋麻疹不常見
膀胱內給藥時,由於藥物吸收減少,系統副作用少見;更常見為化學性膀胱炎,出血性膀胱炎時有發生。
禁忌
-對表柔比星活性成分過敏
-先前使用其它抗腫瘤藥治療或放療出現了嚴重的骨髓抑制
-患者接受過蒽環藥物如多柔比星、柔紅黴素治療,總量已經達到最大安全劑量
-重度黏膜炎,目前或先前具有心功能不全病史(心臟缺損IV級)
-先前使用其它抗腫瘤藥治療或放療出現了嚴重的骨髓抑制
-患者接受過蒽環藥物如多柔比星、柔紅黴素治療,總量已經達到最大安全劑量
-重度黏膜炎,目前或先前具有心功能不全病史(心臟缺損IV級)
注意事項
患者的治療必須在有抗菌劑和細胞毒性劑治療經驗的醫生指導下進行。由於可能發生骨髓抑制併發症,表柔比星大劑量治療時應在有相應監測設備的醫院進行。避免同時進行放射治療。
在治療前,必須測定各項實驗室參數和心功能。
表柔比星的每個治療周期,必須頻繁嚴密地為患者進行監測。治療前以及在治療的間歇期間,對白細胞、紅細胞、血小板和中性粒細胞進行嚴密監測。在標準劑量和大劑量治療過程中,淋巴細胞減少和中性粒細胞減少通常是一過性的,細胞計數在治療開始後第10-14天降到最低,第21天時,常能恢復:上述情況在大劑量方案時更嚴重。即使是大劑量治療的患者,也極少發展為血小板減少症(<100,000血小板/mm3)
治療前以及如果可能在治療期間,檢測肝功能(AST,ALT,鹼性磷酸酯酶,膽紅素)累計劑量應該不超過900-1000mg/m2。
超過上述劑量不可逆的充血性心衰風險大大增加。低於該劑量範圍,這種心臟毒性的客觀可能性極少發生。然而,在治療期間應該嚴密進行心功能的監測減少發生類似其它蒽環類藥物誘導的心衰風險。
心衰甚至可能出現在中止治療後幾周,而且對症藥物治療沒有效果。曾接受縱隔心包區協同治療,或先期治療,放療的患者,心臟毒性的潛在風險可能會增加。
在建立表柔比星最大累積劑量時,任何聯合使用的潛在心臟毒性藥物也應該考慮在內。
治療周期前後建議進行心電圖(ECG)檢查。心電圖的改變,如T波的變平或反常,S-T段降低,或心律失常的發作,上述症狀通常是暫時和可逆的,一般不需要終止治療。
蒽環藥物誘導的心肌病通常同時伴有以下表現:QRS波群區域持續低電壓,收縮間隔時間(PEP/LVET)高於正常值,射血分數降低。對接受依路畢治療的患者進行心臟監測非常重要,評價心功能的適用方法包括使用非-侵入技術如心電圖,超聲心動描記術,以及必要時用放射性核素血管造影術測定射血分數。
與其它細胞毒性劑一樣,表柔比星可以誘發高尿酸血,從而迅速溶解腫瘤細胞。因此應該密切觀察血尿酸水平這樣可以從藥學上控制高尿酸血現象。
本品治療1-2天后,尿液可能變成紅色。
在治療前,必須測定各項實驗室參數和心功能。
表柔比星的每個治療周期,必須頻繁嚴密地為患者進行監測。治療前以及在治療的間歇期間,對白細胞、紅細胞、血小板和中性粒細胞進行嚴密監測。在標準劑量和大劑量治療過程中,淋巴細胞減少和中性粒細胞減少通常是一過性的,細胞計數在治療開始後第10-14天降到最低,第21天時,常能恢復:上述情況在大劑量方案時更嚴重。即使是大劑量治療的患者,也極少發展為血小板減少症(<100,000血小板/mm3)
治療前以及如果可能在治療期間,檢測肝功能(AST,ALT,鹼性磷酸酯酶,膽紅素)累計劑量應該不超過900-1000mg/m2。
超過上述劑量不可逆的充血性心衰風險大大增加。低於該劑量範圍,這種心臟毒性的客觀可能性極少發生。然而,在治療期間應該嚴密進行心功能的監測減少發生類似其它蒽環類藥物誘導的心衰風險。
心衰甚至可能出現在中止治療後幾周,而且對症藥物治療沒有效果。曾接受縱隔心包區協同治療,或先期治療,放療的患者,心臟毒性的潛在風險可能會增加。
在建立表柔比星最大累積劑量時,任何聯合使用的潛在心臟毒性藥物也應該考慮在內。
治療周期前後建議進行心電圖(ECG)檢查。心電圖的改變,如T波的變平或反常,S-T段降低,或心律失常的發作,上述症狀通常是暫時和可逆的,一般不需要終止治療。
蒽環藥物誘導的心肌病通常同時伴有以下表現:QRS波群區域持續低電壓,收縮間隔時間(PEP/LVET)高於正常值,射血分數降低。對接受依路畢治療的患者進行心臟監測非常重要,評價心功能的適用方法包括使用非-侵入技術如心電圖,超聲心動描記術,以及必要時用放射性核素血管造影術測定射血分數。
與其它細胞毒性劑一樣,表柔比星可以誘發高尿酸血,從而迅速溶解腫瘤細胞。因此應該密切觀察血尿酸水平這樣可以從藥學上控制高尿酸血現象。
本品治療1-2天后,尿液可能變成紅色。
孕婦及哺乳期婦女用藥
沒有確切的資料證實表柔比星是否引起人生育率下降或致畸作用。但是一些試驗提示表柔比星可能損害胎兒。動物試驗顯示,與多數其它抗癌藥一樣,表柔比星也可能具有致畸作用和致癌作用。妊娠及哺乳期間禁用表柔比星。使用順鉑期間和至少6個月內,育齡婦女應該避孕防止懷孕和/或生育。
兒童用藥
兒童用藥尚不明確。
老年用藥
老年用藥尚不明確。
藥物相互作用
表柔比星不應與其它藥物混合。但是可以與其它抗癌藥聯合使用。
西米替丁能增加表柔比星活性代謝產物的形成,通過藥代動力學相互作用,也能增加表柔比星以原形的排泄。
表柔比星不能使用alcaline輸注溶液(如碳酸氫溶液)稀釋。
西米替丁能增加表柔比星活性代謝產物的形成,通過藥代動力學相互作用,也能增加表柔比星以原形的排泄。
表柔比星不能使用alcaline輸注溶液(如碳酸氫溶液)稀釋。
藥物過量
單次大劑量給藥能在24小時內誘發急性心衰,並且在10到14天內發生嚴重骨髓抑制。有必要進行對症處理如輸血及將患者轉移到無菌病房。曾觀察到超量使用蒽環類藥物後近6個月時發生遲發性心衰。患者應該嚴密觀察,一旦心衰徵兆增強,按照常規方法處置。
藥理毒理
體外研究表明,對一些動物和人類的腫瘤細胞系來說,表柔比星少有與多柔比星等效的細胞毒性。包括從乳腺、肝、肺、胃、結腸直腸、鱗狀細胞、子宮頸、膀胱、卵巢癌、成神經細胞瘤和白血病提取的腫瘤細胞。
表柔比星抗腫瘤機制尚不完全清楚;然而蒽環類抗生素通過插入DNA鹼基對之間,與DNA形成複合體,從而抑制DNA的複製和轉錄。這種作用可以干擾,至少部分干擾拓樸異構酶Ⅱ和DNA形成的複合物以及蒽環類抗生素的螺旋酶活性。半醌自由基的減少可以引起對DNA、細胞膜脂質和線粒體的損傷。
毒理:動物試驗顯示,表柔比星可能損傷胎兒並具有致畸作用和致癌作用。
表柔比星抗腫瘤機制尚不完全清楚;然而蒽環類抗生素通過插入DNA鹼基對之間,與DNA形成複合體,從而抑制DNA的複製和轉錄。這種作用可以干擾,至少部分干擾拓樸異構酶Ⅱ和DNA形成的複合物以及蒽環類抗生素的螺旋酶活性。半醌自由基的減少可以引起對DNA、細胞膜脂質和線粒體的損傷。
毒理:動物試驗顯示,表柔比星可能損傷胎兒並具有致畸作用和致癌作用。
藥代動力學
快速靜脈內給藥後,血漿中的表柔比星分成三個階段清除:t 1/2 α(初始分布半衰期):
1.8-4.8min,t 1/2 β(中期半衰期):0.5-2.6h,t 1/2 γ(終末清楚衰期):15-45h。
表柔比星分布容積很大(13-52 L/kg),但是與報導的多柔比星相似。調整血漿濃度與時間曲線下面積,表柔比星單劑靜脈給藥劑量比多柔比星高30-70%。靜脈給藥後,表柔比星迅速代謝為2葡萄糖醛酸甙(glucuronides),以及表柔比星的4個糖苷配基。表柔比星通過肝膽系統初始清除,大約11-15%的表柔比星以原形及其代謝產物從尿中清除。中重度肝功能不全的患者用藥後表柔比星的清除下降,血藥漿度升高。
1.8-4.8min,t 1/2 β(中期半衰期):0.5-2.6h,t 1/2 γ(終末清楚衰期):15-45h。
表柔比星分布容積很大(13-52 L/kg),但是與報導的多柔比星相似。調整血漿濃度與時間曲線下面積,表柔比星單劑靜脈給藥劑量比多柔比星高30-70%。靜脈給藥後,表柔比星迅速代謝為2葡萄糖醛酸甙(glucuronides),以及表柔比星的4個糖苷配基。表柔比星通過肝膽系統初始清除,大約11-15%的表柔比星以原形及其代謝產物從尿中清除。中重度肝功能不全的患者用藥後表柔比星的清除下降,血藥漿度升高。
貯藏
避光,冰櫃溫度(2-8℃)下貯存。至於外包裝盒內。
包裝
10ml/5ml/瓶,1瓶/盒,玻璃小瓶
50ml/25ml/瓶,1瓶/盒,玻璃小瓶
100ml/50ml/瓶,1瓶/盒,玻璃小瓶
200ml/100ml/瓶,1瓶/盒,玻璃小瓶
50ml/25ml/瓶,1瓶/盒,玻璃小瓶
100ml/50ml/瓶,1瓶/盒,玻璃小瓶
200ml/100ml/瓶,1瓶/盒,玻璃小瓶
有效期
24個月
執行標準
進口藥品註冊標準JX20060150
