簡介,結構,膠質細胞間的交流,ATP是信使分子,細胞命運,神經元之外部分,
簡介
越來越多的證據表明,被忽略了近半個世紀的膠質細胞,在思維和學習過程中扮演著幾乎和神經元一樣重要的角色。
《走進愛因斯坦先生》一書中,講述了病理學家Thomas Harvey的真實故事,他曾在1955年對愛因斯坦進行過遺體解剖。在完成工作後,Harvey似乎很不敬地將愛因斯坦的大腦帶回了家中,在接下來的40年中,愛因斯坦的大腦就被保存在一個塑膠容器中。Harvey不時地將這些腦片像施捨一樣分給世界各地的科學家和偽科學家,供他們從這些組織中找到愛因斯坦的遺傳線索。但是當Harvey 80歲時,他把剩餘的大腦裝進了箱子,為了把它還給愛因斯坦的孫女,他開始了穿越整個國家的公路旅行。
Marian C.Diamond是位於伯克利市加利福尼亞大學的一位受人尊重的科學家,她曾研究過Harvey給她的腦片。在神經元(神經細胞)數量和大小上,她沒有發現任何異常。但在負責高級認知功能的聯絡皮層中,她發現了異常豐富的非神經元細胞,也就是已知的膠質細胞,該腦區的膠質細胞分布要遠遠多於整個大腦分布的平均數量。
這是偶然的怪現象嗎?也許不是。越來越多的證據表明膠質細胞所發揮的功能要遠遠大於歷史曾給予它的定義。幾十年來,生理學家把焦點集中在了神經元上,認為它是腦內主要的信息傳遞者。儘管膠質細胞的數量超過神經元的9倍,但人們認為它僅發揮一種保護功能:從血管中攜帶營養物質供給神經元,維持腦內離子濃度的正常平衡狀態,防止逃逸免疫系統檢測的病原體的攻擊。在膠質細胞的支撐作用下,神經元可以自由地通過稱為突觸的精細接觸部位傳遞信息,建立連線網路,並在此基礎上形成了我們的思維、記憶以及興奮時的跳躍動作。
如果關於膠質細胞的新認識成立的話,那么長久以來被人們認可的腦功能模式將發生巨大的變化。在過去的幾年中,高敏感的成像技術已經證實,從胚胎髮育階段直到老年,神經元和膠質細胞參與了一種雙向對話。膠質細胞影響突觸的形成,幫助篩選哪些神經聯繫隨時間而增強或減弱;這些變化對於學習和長期記憶的儲存是很關鍵的。更新的研究表明,膠質細胞之間也可以一種獨立的,並且和神經元網路相平行的網路結構進行信息傳遞,影響腦功能。神經科學家很謹慎,他們不急於賦予膠質細胞新的重要性,但他們興奮地看到了腦功能研究的前景。人類大腦的大半部分還是未被開發的處女地,關於腦功能的研究將會包含大量的信息寶藏。
結構
以往神經科學家沒有檢測到膠質細胞間的信號聯繫,一方面可能是技術原因,更主要的還是注意力沒有放在關鍵問題上。他們錯誤地認為,膠質細胞間的相互交流,也需採用與神經元同樣的電學模式,即產生動作電位,最終使神經細胞釋放神經遞質,從而激活與之形成突觸聯繫的其他神經元。因為膠質細胞缺乏傳播自身動作電位所需的膜結構,科學家通過檢測裝置雖然發現膠質細胞突起上有許多能產生電信號的電壓依賴性離子通道,但他們猜測這些通道僅僅能間接地改變周圍神經細胞的興奮性。現在利用先進的成像技術,揭示了以往無法證實的現象,即膠質細胞是依賴化學信號而不是電信號來傳遞信息。
關於神經膠質細胞如何感知周圍神經細胞的活動,直到1990年代中期才取得一些有價值的進展。神經科學家發現,在膠質細胞膜上有各種各樣的受體,能夠對一系列的化學物質起反應,其中也包括神經遞質。這一發現顯示膠質細胞間可能是利用化學信號進行交流,而神經元並不能識別這些化學信號。而且,膠質細胞可能對神經元釋放的神經遞質有直接的應答。
為了證實這些假說,科學家首先必須證實,神經膠質細胞確實能感知神經元之間的交流,並且,它們能基於其所“聽”到的一切做出相應的反應。更早期的工作提示我們,膠質細胞的鈣內流是它們被激活的標誌。基於這種理論,研究者設計了鈣內流的實驗分析方法,通過這種技術可以發現諸如施萬細胞(包裹著外周神經肌肉接頭處的突觸)是否對神經肌肉接頭處釋放的神經遞質敏感,以及神經膠質細胞是否僅僅通過清除突觸處釋放的神經遞質來感知神經元的活性。實際上,更多具有普遍功能的施萬細胞包裹著外周神經軸突的全長,而並非僅限於突觸部分。而少突膠質細胞則包裹著中樞神經系統(腦和脊髓)的軸突。我們想了解當神經衝動沿著軸突傳導時,是否神經環路上任一位置的動作電位都能被膠質細胞所感知,如果真是這樣,它們之間的信息交流究竟是怎樣完成的?更重要的是,動作電位又是如何來影響膠質細胞的?
為了找到答案,在裝有電極的特製培養皿中,我們培育了一些小鼠的脊髓背根神經節(DRG)感覺神經元細胞,通過這些電極我們能夠引發軸突上的動作電位。在一些培養皿中加入了施萬細胞,而其餘的則加入了少突膠質細胞。
我們需要分別檢測軸突和膠質細胞的活性,以明確後者是否能感知軸突傳導的信息。在此我們通過鈣成像技術可視地記錄細胞的活動。當神經元被激活時,神經元上的電壓敏感性離子通道開放,從而使鈣離子內流,我們就能看到綠色的螢光如火焰般從神經元內部迅速點燃整個細胞。當鈣離子濃度升高時,螢光就會變得更強。光電倍增管能檢測光的強度,而且發光細胞的影像可經數位化處理,實時地顯示在監測器上,就如同我們平時在天氣預報中所看到的暴風雨的雷達影像圖一樣。如果膠質細胞能在一定程度上通過攝取周圍環境中的鈣離子來感知神經元的活動,那么它們也將會被“點燃”,只是要稍遲一些而已。
當我和美國衛生研究院(NIH)的同事、生物學家Stevens在黑暗的房子裡盯著電腦顯示器時,我已經知道,在數月的準備之後,我們的假說將在瞬間被證實。當我們打開刺激裝置,DRG神經元立即有了反應,隨著鈣離子如潮水般湧入細胞,螢幕上表示鈣離子濃度的偽彩階逐漸由藍變綠,然後是紅色,最後變成了白色。起初,施萬細胞和少突膠質細胞並沒有改變,但在大約15秒之後,膠質細胞就如同聖誕節的彩燈一樣突然被點燃了。膠質細胞通過某種方式提高了胞漿內的鈣濃度,以此來感知軸突的衝動並做出反應。
膠質細胞間的交流
我們已經確切地證明了膠質細胞是通過攝取鈣離子來感知軸突的電活動。在神經元中,鈣離子激活能產生合成神經遞質的酶。我們可以假設,膠質細胞中的鈣內流也可能激活了能引起某種反應的酶。但是引起的究竟是何種反應?更基本的問題是,鈣內流究竟是怎樣引發的呢?
我們可以回顧一下腦內其他膠質細胞如星形膠質細胞的功能。膠質細胞的功能之一是將營養物質從毛細血管運送到神經細胞內。另一個功能是維持神經元周圍引發神經衝動所必需的陽離子環境,而這種功能就是通過部分地移去神經元興奮時釋放的神經遞質和離子來實現的。1990年,美國耶魯大學的Smith(目前在史丹福大學)領導的一個小組,用鈣離子成像技術顯示,當給培養的細胞加入一種神經遞質谷氨酸時,星形膠質細胞的反應就像這些神經遞質是被一個神經元釋放的一樣,它們之間通過相互信息交流模擬神經元放電。
一些神經科學家一直懷疑,這些由鈣離子或其他相關信息分子介導的細胞間交流是否僅僅通過相鄰星形膠質細胞上的離子通道來實現。1996年, Kater及其同事解答了這個疑問,通過使用一個鋒利的微電極,他們在培養的單層星形膠質細胞中,劃出一條直線,形成一條無細胞的區域,就像用公路把著火的森林分隔開一樣。但當他們在一邊刺激鈣流的波動時,鈣波可以毫無障礙地跨過分隔區擴散到對側的星形膠質細胞。星形膠質細胞只能通過細胞外介質而不是物理接觸來傳遞信號。
在接下來的幾年間,許多實驗室在此方面開展了廣泛的研究,得出了相似的結論。給星形膠質細胞施加神經遞質或套用電極刺激突觸部位神經遞質的釋放都可以誘導出星形膠質細胞的鈣應答。同時,生理學家和生物化學家發現,膠質細胞擁有許多作為神經元間突觸傳遞信號的神經遞質的受體,以及可以使神經元放電產生動作電位的離子通道。
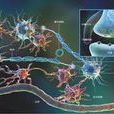
膠質細胞和神經元在大腦和脊髓里共同工作,一個神經元通過長長的軸突運送到突觸前膜,並通過突觸間隙,傳遞到另一個神經元的樹突上,星形膠質細胞可以為神經元運送營養物質,包裹突觸並調節其功能。少突膠質細胞則合成使軸突絕緣的髓鞘。當一個神經元的電信號(動作電位)到達軸突末梢(觸發),促使突觸末梢的囊泡向突觸前膜靠攏並釋放神經遞質(信號分子),這些遞質在突觸間隙中擴散並與樹突上的受體結合——相似的原理同樣適用於外周神經,但在外周神經中是由施萬細胞包裹髓鞘。
ATP是信使分子
這些結果和其他的結果引起了人們的困惑。膠質細胞間的信息傳遞和神經元間的信息傳遞一樣,都是由鈣內流控制的。但是,電衝動引起了神經元的鈣變化,而在膠質細胞上是不可以產生電衝動的,或者說電衝動不能到達膠質細胞。那么,膠質細胞的鈣內流是由另外一種電現象或其他機制啟動的嗎?
在關於膠質細胞的實驗中,研究者注意到一個熟悉的分子總是突然出現——ATP(三磷酸腺苷),每個生物學學生都知道它是細胞活動的能量來源。它可以作為一個巨大的能源儲備,同時也具有許多特點,可以使它成為很好的細胞間信使分子。它們在細胞內高度富集,而在細胞外幾乎不存在。ATP屬於小分子,因此可以快速彌散,迅速降解。所有這些特點都保證ATP分子傳遞的信息對已經存在的信息不至於造成混亂。而且,ATP幾乎全部聚集在軸突末端的內側,也是神經遞質分子儲存的地方;它和神經遞質可以在突觸部位一起釋放出來,也可以彌散到突觸以外的地方。
1999年,美國猶他大學的Peter B.Guthrie及其同事結論性地指出,當膠質細胞興奮時,它可以釋放ATP到周圍環境中。ATP與鄰近膠質細胞的受體結合,引起離子通道的開放和鈣離子的內流。鈣離子水平的升高又促使這些細胞釋放ATP,從而啟動了星形膠質細胞群體ATP介導的鈣應答的鏈式反應。
同時,他們還提出了關於圍繞軸突的膠質細胞是如何感知神經元活動,以及它如何和位於軸突突觸部位的其他膠質細胞進行信息傳遞的模型。神經元的放電可以某種未知的方式誘導軸突周圍的膠質細胞釋放ATP,從而引起鄰近的膠質細胞鈣內流,促使更多的ATP釋放,因此激發了一串膠質細胞的信息傳遞,可以達到與原始興奮神經元相距甚遠的地方。但是,軸突和膠質細胞之間沒有突觸聯繫,而且圍繞軸突的膠質細胞也不存在於突觸周圍,那么在我們的實驗中,膠質細胞是如何感知神經元放電的?首先不是神經遞質,因為它們不能彌散到軸突以外的部分(如果可以彌散的話,神經遞質就可以在腦內不適宜的部位發揮功能,造成功能紊亂)。可能是ATP,神經元放電時,它可以和神經遞質一起被釋放出來,以某種方式沿著軸突逃逸到突觸以外的部位。
為了驗證這種想法,我們對純的DRG軸突培養物給予電刺激,分析培養基發生的變化。在培養基中加入可以產生螢光的酶(該酶促反應需要ATP的參與),當軸突放電時,我們通過觀察培養基中的螢光就可以檢測到軸突ATP的釋放。然後,我們在培養基中加入施萬細胞,檢測鈣的反應性。它們在軸突放電產生動作電位後也被活化。然而,當我們加入三磷酸腺苷雙磷酸酶時,它可以迅速降解ATP----因此可以阻斷ATP,阻止它到達任何施萬細胞----當軸突放電時,膠質細胞中沒有螢光產生。由於細胞接收不到ATP信使分子的信號,施萬細胞的鈣應答被阻斷。
軸突釋放的ATP確實可以引發施萬細胞的鈣內流。同時套用生物化學分析方法和數字顯微鏡,我們觀察到鈣內流使信號從胞膜向胞核傳遞。由於胞核是基因存儲的部位,從而引起各種基因的表達。令人驚奇的是,軸突通過放電同其他神經元進行信息傳遞,同時可以指導膠質細胞的基因表達,藉此影響它的行為。
細胞命運
在這點上,我們以及其他人的工作都得出結論,膠質細胞通過感知軸突放電釋放的ATP或者是從突觸部位漏出的ATP而感知神經元的動作電位。膠質細胞通過自身的鈣離子進行信息的中繼傳遞。鈣離子激活ATP釋放酶,釋放ATP到其他膠質細胞,也可以激活控制基因表達的酶類。
觀察到這種現象就使我們想進一步知道,這些基因控制著細胞的哪些功能?它們是要告訴膠質細胞以某種方式影響周圍的神經元活動嗎?為回答這個問題,Stevens集中在研究軸突周圍髓鞘絕緣層的產生過程,這個過程顯然可以影響神經元的功能。這種絕緣性對於長距離、高速度的神經衝動傳導是很關鍵的。它的生成可以使嬰兒逐漸抬頭,而它的破壞如多發性硬化等疾病可以造成嚴重損害。
我們轉向研究髓鞘是因為我們想知道,胎兒或嬰兒周圍神經系統軸突上的未成熟施萬細胞是如何分辨哪些軸突是需要髓鞘的,何時開始形成髓鞘,或者說,它是怎樣知道是否應該轉化成不形成髓鞘的細胞?通常,只有大直徑軸突需要髓鞘。軸突的神經衝動或者ATP釋放影響了這些過程的選擇?我們發現,培養的施萬細胞,在放電的軸突周圍較靜止的軸突周圍,其增殖速度更加緩慢。而且,施萬細胞的發育和髓鞘形成過程都被阻斷。加入ATP產生了同樣的效應。
可是,我們和Vittorio Gallo及其在NIH兄弟實驗室的同事,在參與腦內髓鞘形成的少突膠質細胞上,發現了一種相反的現象。ATP不會抑制它們的增殖,而ATP去除磷酸分子後的腺苷,可以刺激細胞的成熟,形成髓鞘。這兩種現象表明,神經元通過膠質細胞上的不同受體來分別給予中樞和周圍神經系統膠質細胞不同的信號,而不必產生單獨的信號分子或指定信號分子的靶點。
深入認識成鞘過程是很重要的。每年,成千上萬的人因為脫髓鞘疾病而死亡,更有數不清的人因該病而癱瘓或者失明。比如,每700個人中就有一個發生多發性硬化。沒有人確切地知道成鞘過程是如何啟始的,而腺苷是第一個已知的來自於軸突的可以刺激髓鞘形成的物質。軸突放電可以引起腺苷釋放的事實,意味著腦內的活動的確影響了成鞘過程。這些發現可以為疾病的治療開闢出新的道路。腺苷的類似物可能發揮作用。在幹細胞中加入腺苷可能使它們轉化為成髓鞘的膠質細胞,進而被移植到受損神經部位。
神經元之外部分
我們實驗室的實驗以及其他人的實驗都強烈支持ATP和腺苷介導了施萬和少突膠質細胞網路的信息傳遞,而ATP單獨就可以在星形膠質細胞誘發出鈣信號。但是,除了成鞘功能外,膠質細胞還有調節神經元功能的其他途徑嗎?
答案看來是肯定的。加拿大蒙特婁大學的Richard Robitaille在蛙的肌肉上觀察到突觸部位的電壓隨注入突觸部位施萬細胞的化學物質不同而增強或減弱。美國明尼蘇達大學的Eric A.Newman在大鼠視網膜上的研究發現,膠質細胞鈣離子流的波動隨視神經元放電的改變而變化。美國紐約醫學院的Maiken Nedergaard對海馬(參與記憶過程)腦切片的研究中觀察到,當附近的星形膠質細胞刺激鈣流的波動時,突觸部位的電活動也增加。突觸強度的變化被認為是神經系統通過經驗(概念上稱為可塑性)改變其反應性的基本方式,表明膠質細胞在學習的細胞機制上發揮重要作用。
這些觀察也發現了一個問題。就像歌迷歡呼聲可以橫掃整個體育館一樣,鈣波也在整個星形膠質細胞群中播散。對整體而言,大範圍的應答是有效的,但它不能傳遞複雜的信息。快速反應(Go team)活動的一致性對睡眠-覺醒周期或癲癇發作期間,協調大腦的整體活動可能是有用的,但如果膠質細胞參與在信息加工的複雜過程中,保持局部的穩態又是很必要的。
Smith及其同事在他們於1990年發表的文章的腳註中指出,他們相信神經元和膠質細胞具有更加分散的穩態功能。然而,研究人員缺乏更加精確的實驗方法給予一種神經遞質,使其接近實際情況下突觸部位星形膠質細胞發生的變化。2003年,美國賓州大學的Philip G. Haydon實現了這個目標。他套用改良的雷射技術在海馬腦片上釋放極小量的谷氨酸,僅可以被一個星形膠質細胞感知。在這種條件下,Haydon發現一個星形膠質細胞僅對其周圍少量的星形膠質細胞傳送特定的鈣信號。就像Haydon指出的,除了鈣信號影響星形膠質細胞的整體活動以外,“星形膠質細胞間有著短程連線”。
換言之,腦內分散的星形膠質細胞迴路和神經元迴路產生協調的活動。(目前,對定義這些不同的星形膠質細胞迴路的生理或生物化學因子還不清楚)。其他人的研究也表明,星形膠質細胞可以分泌與軸突釋放的神經遞質相同的物質,加強突觸部位的信號傳遞----有效地對信號進行放大。
Haydon和我以及我的同事從這些發現中得出的工作假設是,星形膠質細胞間的信息交流有助於激活軸突終止部位相對較遠的神經元,進一步有助於遠端突觸神經遞質的釋放。這種作用可以調節遠端的突觸在強度上發生何種變化,這將是學習和記憶的分子機制。
2003年11月在神經科學協會年會上報導的結果支持上述論點,很可能把膠質細胞的功能擴大到參與新突觸的形成中[參見下頁圖文]。一些研究發現是建立在兩年前史丹福大學的Ben A.Barres和Frank W. Pfreger及其同事的研究結果上,他們報導,培養的大鼠神經元在星形膠質細胞存在的情況下可以形成更多的突觸。
隨後,在Berres的實驗室工作的博士後Karen S. Christopherson和Eric M. Ullian發現了一種可能來自於星形膠質細胞的蛋白質thrombospondin,它可能是是促使突觸形成的化學信號分子。Thrombospondin具有多種生物功能,但人們認為它不是神經系統中的一個關鍵分子。在星形膠質細胞培養基中加入越多的thrombospondin,就有越多的突觸形成。在新生的神經網路形成過程中,Thrombospondin可能是負責把一些形成突觸需要的蛋白質和其他化合物聚集在一起,因此thrombospondin也可能參與成年期突觸的重塑過程。
進一步的實驗將會加深我們對膠質細胞是如何影響腦功能這一新觀念的認識。其中一個問題是證明記憶----或者記憶在細胞上的類似現象,如長時程增強----可以被與突觸功能相關的星形膠質細胞影響。另一個問題是明確星形膠質細胞環路發出的信號可以影響到多遠的突觸結構和功能。
星形膠質細胞可以遠距離作用的方式影響突觸形成,這也許不應令人驚奇。由不同神經元迴路處理的不同的刺激信號,比如對特定的氣味的嗅覺體驗、講話,以及接收刺激的人形成的情感體驗,它們之間要形成聯繫,大腦就必須在這些沒有直接聯繫的神經元迴路之間建立快速的信息傳遞方式。如果神經元就像電話通過電信號傳遞信息一樣,它們通過突觸之間的物理連線進行信息傳遞,那么星形膠質細胞就像細胞電話機,向四處發放化學信號傳遞信息,但是僅有那些具備適當受體的星形膠質細胞可以感知到傳遞的信息。如果信號可以通過星形膠質細胞迴路廣泛傳播,那么一個部位的膠質細胞就可以激活遠處的膠質細胞,對整個腦區神經元迴路的放電進行調製。
大腦的比較學研究揭示,隨著動物進化程度的升高,膠質細胞對神經元的比例大大升高。Haydon對星形膠質細胞之間存在的廣泛聯繫是否有助於更好的學習的課題很感興趣。他和同行們正在用新的實驗驗證這個假說。或許,提高膠質細胞在腦內的濃度,或出現一種更大潛能的膠質細胞就可以使一些人成為天才。愛因斯坦告訴了我們敢於打破常規思考的價值。那些不只看到神經元,更看到膠質細胞是如何參與信息加工的神經科學家正在走著與愛因斯坦同樣的路。