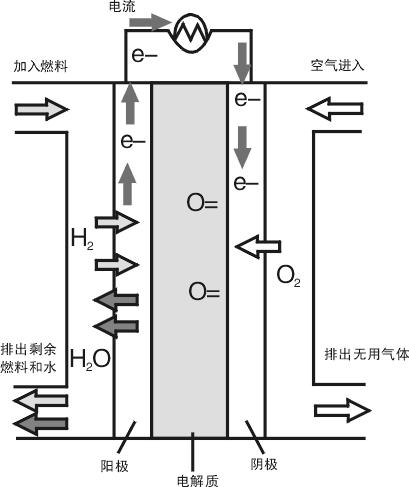
雙極鹼性燃料電池是以鹼性溶液為電解質,將存在於燃料與氧化劑中的化學能直接轉化為電能的發電裝置。是最早獲得套用的燃料電池,由於其電解質必須是鹼性溶液,因此而得名鹼性燃料電池。在1973年成功地套用於阿波羅登月飛船的主電源,使人們看到了燃料電池的誘人前景。
基本介紹
- 中文名:雙極鹼性燃料電池
- 外文名:Bipolar alkaline fuel cell
- 屬性:能源裝置
- 領域:化學能源利用
概述,原理,催化劑的性能衰減機制,
概述
電動車輛和規模化儲能等新能源產業的發展,以及高性能攜帶型電子設備的進步,迫切需要高效、清潔的電化學儲能系統。目前廣泛使用的鋰離子電池的能量密度已接近理論極限,無法滿足對儲能系統的迫切要求。因此,全世界都在積極探索下一代的電化學儲能系統。
燃料電池(fuel cells,FC)是一種可以將儲存在燃料和氧氣中的化學能直接轉化為電能的電化學儲能裝置。普通的內燃機由於需要經歷熱機過程,受卡諾循環的限制,其能量轉化率大多低於 15%,燃料電池不受此限制,因而具有很高的能量轉化率,一般為 40%~60%,如果將餘熱充分利用,甚至可以高達 90%。此外,燃料電池在工作時,其反應產物一般只有 H2O 和CO2,很少會排放出 NOx和 SOx,
因而不會污染環境,是新一代的綠色能源。燃料電池在工作時排出的二氧化碳量,也低於傳統火力發電廠的 60%。可見,燃料電池對解決目前全世界所面臨的能源安全(Energy Security)和環境保護(Environment Protection)兩大難題都具有極其重要的意義。同時,燃料電池由於具有高效、綠色、安全等優點,被認為是 21 世紀的新能源之星。
原理
使用的電解質為水溶液或穩定的氫氧化鉀基質,且電化學反應也與羥基(-OH)從陰極移動到陽極與氫反應生成水和電子略有不同。這些電子是用來為外部電路提供能量,然後才回到陰極與氧和水反應生成更多的羥基離子。
負極反應:2H2+ 4OH-→ 4 H2O + 4e-
正極反應:O2+ 2H2O + 4 e-→ 4OH-
鹼性燃料電池的工作溫度大約80℃。因此,它們的啟動也很快,但其電力密度卻比質子交換膜燃料電池的密度低十來倍,在汽車中使用顯得相當笨拙。不過,它們是燃料電池中生產成本最低的一種電池,因此可用於小型的固定發電裝置。
催化劑的性能衰減機制
關於鹼性體系中催化劑的性能衰減機制尚無相關研究,但是在PEMFC中關於Pt催化劑性能衰減機制方面,國內外學者已經進行了大量研究工作,目前研究人員普遍認為,在PEMFC的工作環境下,Pt催化劑性能衰減的主要原因有:碳載體被腐蝕,導致Pt從載體上脫落;Pt顆粒的溶解-再沉積;Pt顆粒在碳載體表面的團聚。