來源,物化性質,化學性質,α-BGT蛋白質結構,β-BGT蛋白質結構,κ-BGT蛋白質結構,γ-BGT蛋白質結構,分離純化,毒素作用機理,β-BGT毒理,磷脂酶活性,β-BGT受體,對大鼠腦突觸體作用,PLA2活性,毒素與基因工程,基因組,克隆和表達,免疫學特性,套用,
來源 銀環蛇 (Krait,Bunga rus Spp.)屬動物界,脊索動物門,爬蟲綱,有鱗目,
眼鏡蛇 科,環蛇屬。全身背面是黑白相間的環紋,具30~50個白色或乳黃色窄橫紋,是世界十大
毒蛇 之一。主要分布在
泰國 、
緬甸 、印度、中國的南部和中國台灣等地,有12種亞種。其中分布在中國南部和中國台灣省的Bungarus multicinctus,Blyth的毒液成分研究報導較多,台灣產銀環蛇蛇源已枯竭,而銀環蛇在中國有兩個亞種-指名亞種(即中國銀環蛇,Bungarus multicinctusBlyth Chinese Krait)和雲南亞種(B.muticinctus Pope)。
銀環蛇屬前溝牙類毒蛇,被銀環蛇咬傷的主要症狀為傷口疼痛、局部腫脹、嗜睡、運動神經失調、眼瞼下垂、瞳孔散大、局部無力、顎咽麻痹、口吃、垂涎、噁心、嘔吐、昏迷、呼吸困難、呼吸衰竭,8~72 h內死亡。其一次排毒4.6mg,1mg乾毒就能致人於死地。
物化性質 化學性質 根據神經毒素的作用靶點不同,把銀環蛇神經毒素分為兩類:一類為突觸後
神經毒素 或α-神經毒素,這類毒素競爭性的與神經肌肉接頭處的乙醯膽鹼受體結合,阻斷神經遞質的傳導;另一類為突觸前神經毒素或β-神經毒素,其直接作用於運動神經突觸前膜,阻斷乙醯膽鹼的釋放,使骨骼肌失去收縮功能而麻痹。根據相對的分子質量大小和二硫鍵的數目把突觸後神經毒素又分為短鏈神經毒素(60~62個胺基酸殘基,4對二硫鍵)和長鏈神經毒素(70~74個胺基酸殘基,5對
二硫鍵 )。其中短鏈神經毒素的阻斷作用具有一定的可逆性。
α銀環蛇毒素紫外光譜 銀環蛇毒素新鮮毒液呈灰白色,粘稠具有特殊的腥味,毒性較強,是一種鹼性多肽,是典型的長鏈突觸後神經毒素,由74個胺基酸殘基組成,含有較多的鹼性胺基酸殘基和10個半胱氨酸殘基,所有的半胱氨酸殘基都參與二硫鍵的形成,含有5對二硫鍵,具有蛋白質的通性,加熱和受紫外線照射會產生絮狀沉澱,導致毒性部分或全部喪失,強酸、強鹼、氧化劑、還原劑、消化酶、重金屬鹽、酒精、
酚 類均能破壞其毒性;經甲醛和
戊二醛 處理其毒性喪失,但抗原性仍能保留。通常採取甲醯基化的方法脫毒後免疫動物,製備抗血清。
銀環蛇毒素的主要成分為蛋白質和多肽,其中毒性成分主要是多種毒性多肽中的神經毒素(Tu A T,1996)。李鎮源等曾先後報導了從台灣銀環蛇中分離鑑定出α-銀環蛇毒素(α-BGT)、β-銀環蛇毒素(β-BGT)、κ-銀環蛇毒素(κ-BGT)和一些酶類如磷脂酶A、凝血酶因子等。錢友存等通過RT-PCR方法從銀環蛇中克隆到神經毒素,心臟毒素(cardiotoxin)和一些心臟毒素樣鹼性蛋白(CLBPs)以及4個神經毒素類似物(neuro-toxin-likeproteins)(BMNTL 1-4)和1個三環結構蛋白(BML-CL)。Aird S D等從銀環蛇毒腺細胞中分離出一種新的神經毒素γ-銀環蛇毒素(γ-BGT),並利用質譜分析法和Edman降解法測定了γ-BGT的一級結構。
銀環蛇毒素粗毒電泳圖 β-銀環蛇毒素(Beta-bungarotoxin,β-Butx)來源於銀環蛇(Bungarus multicinctus)蛇毒中,是一種突觸前多肽神經毒,表現出Ca2+依賴性磷脂酶A2(Phospholipase A2,PLA2)活性。首先由Chang於1963年在台灣銀環蛇(Bungarus multicinctus)中發現,是第一個具有藥理特徵的突觸前蛇神經毒素。分子量(Mr)為20500,由兩個亞基通過二硫鍵共價連線成二聚體,分子量較大的A亞單位(Mr=13500)上存在PLA2活性中心,分子量較小的B亞單位(Mr=7000)與蛋白激酶抑制物有一些序列同源性。當亞基間二硫鍵斷裂時,或PLA2活性中心被共價修飾時,都可導致β-BuTx的神經毒性和PLA2活性喪失。
純化後的蛇毒蛋白電泳圖 β-BGT是一種高
鹼性 多肽,其分子量為20-22KD,等電點為8.8-9.7。由A、B兩條鏈構成,二者通過一個鏈間二硫鍵共價連線。A鏈含有120個胺基酸殘基,分子量為13500D,具有磷脂酶A2的活性,在結構上與哺乳動物胰腺分泌的磷脂酶A2及其它蛇毒液中的磷脂酶A2有同源性。B鏈含有60個胺基酸,分子量為7000D,與哺乳動物胰腺、蛇毒及蝸牛毒中的kunitz型蛋白酶抑制劑、毒素Ⅰ及樹眼蛇毒素具有序列同源性。但是β-BGT對胰島素、胰凝乳蛋白酶、枯草桿菌蛋白酶、彈性蛋白酶無任何抑制活性,說明B鏈並不是作為蛋白酶抑制劑起而作用的。β-BGT中的鹼性胺基酸含量較高,半胱氨酸含量也較多,但尚未發現β-BGT中有自由的巰基。不同的學者分離到的β-BGT性質有差異,有的學者認為是分離時的交叉污染造成的。
通過胺基酸序列分析及DNA序列分析表明,存在5個以上的A鏈變異體,4個以上的B鏈變異體,組成7個以上的β亞型毒素。其中A1、A2及A3與B1及B2組成β1-β5,β6也已獲得分離純化。它們之間存在非常高的序列同源性,具有高度的保守區,包括了活性位點。其中各鏈之間胺基酸差異數目分別為A1和A2:5個,A和A3:9個,A2和A3:12個,B1和B2:22個。
α-BGT蛋白質結構 α-BGT是1963年發現的。是一種鹼性多肽,含較多的鹼性胺基酸和10個半胱氨酸殘基,半胱氨酸殘基都參與5對二硫鍵的形成。屬於長鏈突觸後神經毒素,由74個胺基酸組成,相對分子質量為8000 D,空間結構複雜,幾乎每一個胺基酸都對空間結構的形成發揮著重要作用。雖然分子量並不大,但α-BGT具有相當豐富的空間結構,該分子中幾乎每一個胺基酸殘基對其空間結構的形成都發揮著重要的作用,因此是探討蛋白質一級結構與高級結構以及結構與功能很好的材料。α-BGT結構如三指形,4個二硫鍵聚集在一起形成一個緻密的核心,由此核心伸展出3個肽鏈環仿佛3個手指,長的C末端尾巴從緻密的二硫鍵核心伸出。4對二硫鍵與結構穩定性有關,大部分集中在中間大環上且分布於環的一側,形成一個活性表面。α-BGT不存在α螺旋,主要由β-摺疊和β-轉角組成。長鏈和短鏈的蛇毒突觸後神經毒素主要區別在於尾巴表面存有不同的識別位點,在一級結構上的差別是長鏈蛇神經毒素比短鏈的蛇神經毒素多10~15個胺基酸和一對二硫鍵,空間結構上的差別在於長鏈神經毒素的第5對二硫鍵存在於中央大環loopII的頂部,產生一個循環螺旋樣的動態的構象,使得長鏈神經毒素適應不同受體亞型。具有三指形結構的蛇神經毒素一般由60~80個胺基酸殘基組成一條多肽鏈,胺基酸殘基的組成及相對位置具有很大的同源性。長鏈和短鏈的蛇毒突觸後神經毒素都屬於這類結構,三指型毒素摺疊的可塑性已經歷了最佳的進化,可利用功能基團的不同組合特異性識別nAChR亞型間的細微差別。
Ohta M等(1987)的研究結果顯示了在N-末端的9-11,67-68和71-72位置分別存在Ser-ProIle,Pro-His和Gln-Arg,而非先前報導的Ile-Pro-Ser,His-Pro和Arg-Gln胺基酸排列順序。Love RA等(1986)利用X射線晶體衍射法進行α-BGT蛋白質結構的研究表明,α-BGT蛋白質晶體結構的解析度為2.5A。其晶體結構是與眼鏡蛇神經毒素和埃布拉神經毒素相比較而言的,它的溶液結構由質子-NMR分光鏡方法推導而來,主要的不同是α-BGT的β-sheet飄帶比其它神經毒素少,而且在不變的
色氨酸 結晶中有不同尋常的定位。Tali Scherf等利用二維質子-
核磁共振 光譜學方法解決了α-BGT和第13個胺基酸殘基肽庫(MRYYESSLKSYPD)的複合物溶液結構,其肽譜是採用1個由Tyr-11肽組成的疏水核心環繞三圈而成的球狀骨架結構和飄帶結構。Moise L等報導了一個新的更高清晰度的α-BGT核磁共振結構,它定義了決定二硫化物的核心和β-sheet圖的區域範圍。
乙醯膽鹼受體種類很多,α-BGT是與N-型的乙醯膽鹼受體結合,其結合是專一性的,飽和的和不可逆性的,具很高的親和力。乙醯膽鹼受體α2βγδ的α-亞基是結合乙醯膽鹼和毒素的亞基,關鍵胺基酸位於125~147殘基之間。
β-BGT蛋白質結構 β-銀環蛇毒素最初是從台灣銀環蛇(Bungarus multicinctus)中分離鑑定出的為突觸前鹼性多肽神經毒素,由A鏈和B鏈兩條鏈構成,其分子量為20~22kD,等電點為8.8~9.7。A鏈通過Cys15和B鏈的Cys55相連,把2條鏈連線起來。A鏈含120個胺基酸,有13個半胱氨酸,分子量為13500D,一級結構類似於蛇毒和哺乳動物胰腺中的磷脂酶A2(PLA2),但活性比較弱。His48,Asp99和Tyr52的側鏈互相影響形成一個氫鍵中心,組成活性中心區域,處於活性中心的胺基酸是相當保守的。B鏈由60個胺基酸組成,分子量為7000 D,與胰蛋白酶抑制劑、毒素I及樹眼鏡蛇毒素具有序列同源性,並且有阻斷鉀離子通道的功能。其中樹眼鏡蛇毒素分離自非洲的曼巴蛇,選擇性地阻斷神經元的電壓門控鉀通道。
從台灣銀環蛇(Bungarus multicinctus)中已分離出7種β-銀環蛇毒素異構體。除了A2鏈外,A1和A3鏈的cDNA還未克隆到。然而,另外三個A鏈異構體(A4~A6)的cDNA已被克隆。化學修飾研究結果表明,A鏈是具有較弱磷脂酶A2活力的亞基,並且具有神經毒性效應。眼鏡蛇蛇毒中並沒有發現突觸前神經毒素即β-神經毒素。眼鏡蛇中克隆到的磷脂酶A2含119個胺基酸和7對二硫鍵,為酸性蛋白質,具有較強的PLA2活性。
Yang等研究β1-BGT的免疫化學性質時,通過定量沉澱反應和研究Fab片段組成的可溶性複合物的分子量分析發現β1-BGT A鏈,B鏈的抗原決定簇的數目分別為5和2。其製備了23個單克隆抗體,其中7個能抑制PLA270%的活性,中和毒素的毒性。免疫印跡顯示,6個單克隆抗體識別連續的表位。A鏈的序列31-37,46-51,91-98,100-106是可以被中和的表位。
通過比較分析眼鏡蛇和海蛇科PLA2的cDNA序列,發現5′-,3′-非編碼區和信號肽編碼區十分保守。1.5 g/L瓊脂糖泳分析表明,在500 bp左右有特異的PCR產物條帶,和預期的cDNA大小基本一致。經低熔點瓊脂糖回收PCR產物,連線於pGEMT載體,轉化DH5α,進行藍白斑篩選。對陽性克隆進行PCR和ApaI/PstI雙酶切鑑定。抽質粒進行雙鏈DNA測序。cDNA序列分析表明,一種新的A鏈被克隆到,其全長486bp,編碼27個胺基酸的信號肽和120個胺基酸的成熟蛋白,命名為A7鏈。該信號肽和A4的信號肽有較高的同源性,僅有3個胺基酸的不同,即26位的Tyr→Asn,3位的His→Glu和2位的Pro→His。但A7的信號肽和A2的信號肽差異較大,其差異主要在N-端的10個胺基酸。A7的信號肽和A4的信號肽在數量上一樣,為27個胺基酸,而A2的信號肽為25個胺基酸。A5和A6的信號肽不完整,而A1及A3的cDNA尚未被克隆到。新的A鏈即A7鏈,和其他A鏈一樣,含13個半胱氨酸。胺基酸序列同源性比較表明,A7鏈和其他A鏈(A1~A6)具有很高的同源性,分別為89.2%,86.7%,94.2%,92.5%,88.3%和89.2%。cDNA序列同源性分析結果表明,A7鏈的cDNA和A2,A4~A6cDNA的同源性分別是92.2% ,94.7%,93.7%,92.9%。儘管從台灣銀環蛇中鑑定出6種A鏈異構體(A1~A6),但從大陸銀環蛇中只克隆到一種A鏈(A7)。是否大陸銀環蛇也存在A鏈多態性還有待進一步闡明。從中國大陸眼鏡蛇(Naja naja atra)中RT-PCR擴增PLA2cDNA,克隆並測定了全序列。序列分析表明,該cDNA和從台灣產眼鏡蛇(Naja naja atra)中克隆到的cDNA僅差一個鹼基,且為沉默突變。該cDNA編碼一個27個胺基酸的信號肽和一個119個胺基酸的成熟蛋白,即眼鏡蛇PLA2。
銀環蛇毒素DNA排列圖冊參考資料。
κ-BGT蛋白質結構 κ-BGT是1983年從台灣產銀環蛇毒素中首次分離、分子量6500,等電點為9.1的一種神經毒素,由於k-BGT能選擇性地阻斷α3β2亞型,被認為是少數能作為神經元菸鹼乙醯膽鹼受體(nAChRs)分型的特異性工具之一。κ-BGT的蛋白質一級結構由A、B兩條鏈構成,每條鏈由66個胺基酸殘基組成,含有五對二硫鍵,其分子量均為7258。
GrantG A等報導了作為神經元菸鹼型受體探針的κ-BGT的完整胺基酸序列,以後陸續有人從銀環蛇毒素中分離純化到六種新的κ-神經毒素(κ1-κ6),並分別報導分析了其前體細胞和完整胺基酸排列順序。根據其基因編碼的序列可以看出,κ1-κ6存在著高度的同源性。κ-神經毒素和與其在結構上相關的α-神經毒素有決定性的區別。例如,κ4-BGT缺乏Try-殘基,而Try-殘基在α-BGT的功能位點上是無變化的且相當重要的。κ-BGT在決定性序列位點上有一個無變化的Pro-殘基也不同於α-神經毒素。從κ2-BGT和κ3-BGT中還檢測到了包含一個亞單位的異二聚體。
γ-BGT蛋白質結構 γ-BGT是從銀環蛇毒腺中分離出的一種新的突觸後神經毒素。Aird SD等(1999)利用質譜測量法和Edman降解法測定了其一級結構。γ-BGT的一級結構由68個胺基酸殘基構成,分子量為7524.7。其胺基酸序列為:MQCKTCSFYT CPNSETCPDGKNICVKR-SWT AVRGDGPKRE IRRECAATCP PSKL-GLTVFC CTTDNCNH。在結構上γ-BGT類似於κ-BGT和眼鏡蛇長鏈突觸後神經毒素,C-末端九個胺基酸殘基與κ-BGT完全相同。然而,靜脈注射小鼠LD50為0.15μg/g,其毒性是其它毒素的30-150倍,可與α-nAchR拮抗物的毒性相比較。
分離純化 從粗毒液中分離純化毒素一般採取
離子交換 層析柱及
高效液相 層析法。將粗毒素溶於0.05mol/L pH值5.8醋酸銨中,加於CM-Sephadex C-25柱中,採用兩相線性梯度醋酸銨洗液洗脫:Ⅰ為從50mmol/L(pH值5.8)到500mmol/L(pH值7.0),Ⅱ為從500mmol/L到1.0mmol/L(pH值7.0),可得到12種蛋白組份。其中Ⅹ、Ⅺ、Ⅻ-1、Ⅻ-2和Ⅸ分別為β1至β5,每一種組份可用Sephadex G-75或高效液相層析進一步純化。
銀環蛇毒素層析分離圖譜 對於毒素中A鏈與B鏈的分開一般採用Chang(1993)的方法,即用二硫
蘇糖醇 還原鏈間二硫鍵,蛋白與二硫蘇糖醇的分子比率為1∶4,然後在Syn Chropak RP-P柱(4.6mm×250mm,用0.1%TFA平衡,25%-30%的乙腈線性梯度液洗脫)上進行高效液相層析分離純化。A、B鏈的分離也可以選用2-巰基乙醇還原,然後用
碘乙酸 烷化。
毒素作用機理 β-BGT毒理 β-BuTx主要作用於神經系統,在外周神經系統中它能不可逆地阻斷神經肌肉的興奮傳遞;在中樞神經系統中它能特異地抑制某些神經元突觸前膜遞質的釋放。為了進一步研究β-BuTx對中樞神經系統的作用機理,大多數實驗研究都是在分離出的突觸體上進行的。β-BGT主要作用於神經系統,在外周神經系統中不可逆地阻斷神經肌肉的興奮傳遞,在中樞神經系統中特異地抑制某些神經元突觸前膜遞質的釋放。其毒性作用依賴於PLA2活性,A鏈的Lys64與PLA2活性和β-BGT其他毒性有關。當亞基間二硫鍵斷裂,或PLA2活性中心被共價修飾時,都可導致β-BGT的神經毒性喪失。PLA2活性具有間接溶血作用,在Ca2 +存在下能水解卵磷脂(專一水解C-2酯鍵),生成能溶解紅細胞的溶血卵磷脂及脂肪酸,兩者促進突觸囊泡和突觸前膜的融合,在膜表面暴露出突觸囊泡蛋白的內部表位,誘導突觸囊泡分泌到胞外,伴隨著細胞外的大量鈣離子流向神經末梢。這兩者還使神經末梢的突出囊泡儲存庫消失。用谷胱甘肽還原鏈間二硫鍵可提高β-BGT的膜破壞活性。B鏈識別特定靶細胞膜,阻斷電壓門控鉀通道,但也需要A鏈的相互作用及鈣離子的參與。但Cheng等發現B鏈引起人類神經節SK-N-SH細胞凋亡,這種細胞毒性與A鏈的PLA2活性沒有多大關係。Pei-Fung Wu等發現當β-BGT的濃度為357 nM時,內化為NB41A3細胞時並不引起胞質的鈣離子濃度變化,其中,鈣離子的增加與PLA2有關。所以當EGTA(鈣離子螯合劑)存在時,也不會影響細胞的突起生長。這說明,β-BGT的內化與A鏈的PLA2的活性是獨立的。是否只與B鏈有關,還需要進一步的實驗來確定。利用瓜蟾的神經肌肉組織研究β-BGT A鏈和B鏈的作用,發現β-BGT能增強自發突觸電流(SSC)的發生頻率,用5’-磷酸-吡哆醛修飾β-BGT或用Ba2+代替緩衝液中的Ca2+則能消除β-BGT的磷酸酶A2活性,減少SSC的發生頻率。針對A鏈或B鏈的特異性抗體均能有效地抑制磷酸酶A2活性,但對SSC的發生頻率沒有太大影響。說明A鏈和B鏈對增強瓜蟾的神經肌肉SSC的發生頻率都是必不可少的。
β-BuTx對神經系統作用的研究最早是從外周神經、肌肉組織起始的,1963年Chang等首先從銀環蛇蛇毒中分離出這種突觸前神經毒,發現它可阻斷由刺激引起的運動神經末梢ACh的釋放。隨後對β-BuTx進行了毒理學、電生理學、藥理學、形態學等研究,獲得大量實驗證據,對其機理研究取得了一些進展。電生理學和組織學研究表明:在神經肌接頭處,β-BuTx廣泛作用於突觸前膜,導致神經遞質釋放的阻斷,最終引起運動神經末梢的破壞。當β-BuTx孵育從大鼠中分離出的神經肌肉標本時,大約1.5~3小時後,β-BuTx引起完全的神經肌肉阻斷。如果標本孵育期間反覆刺激神經,則阻斷髮生的更快。將β-BuTx用bromophenacyl bromide進行化學修飾後,可使β-BuTx的PLA2活性失活。用無PLA2活性的β-BuTx對神經肌肉標本進行孵育,結果使β-BuTx同族毒素對同一神經肌肉的阻斷作用所需時間增加,因此說明:同族毒素可能結合於神經末梢的特殊位點,這個位點能被修飾後的β-BuTx競爭性占據。Howard認為,β-BuTx引起神經肌肉阻斷在電生理方面表現為三個階段。第一階段:神經肌肉標本經過5~10分鐘的β-BuTx孵育後,終板電位(End Plate Potential,EPP)幅度先出現一個輕微的下降;第二階段:以後30~60分鐘期間EPP幅度出現增高現象;第三階段:然後EPP幅度出現進行性下降直至EPP觀察不到。第三個階段小終板電位(Miniature End PlatePotential,MEPP)的頻率也逐漸降低,直到神經肌肉完全阻斷時,MEPP也幾乎觀察不到。但β-BuTx不影響MEPP的振幅。
關於β-BuTx作用於神經肌肉標本初期可使EPP振幅輕微下降的機理仍不清楚,但是其隨後引起EPP振幅增高的機理多數學者認為:它是由於神經末梢內游離Ca2+增高所致,而神經末梢內游離Ca2+增高可能是β-BuTx阻斷K+通道,使神經末梢膜去極化時程延長,電壓依賴性Ca2+通道開放時間比正常時延長,則進入神經末梢內的Ca2+增加,使遞質釋放增加,Mallart在20世紀80年代用大量實驗證實這個觀點。Petersen等在豬背根神經節電壓鉗的實驗中進一步發現:β-BuTx可以選擇性地阻斷K+電導成份。除以上β-BuTx通過阻斷K+能道引起EPP振幅增加之外,還有其他一些關於此現象的解釋:β-BuTx可通過某種方式使突觸前遞質囊泡與膜融合的可能性增高;β-BuTx通過某種機制使Ca2+釋放的結構敏感性增加;β-BuTx直接使神經末梢動作電位時Ca2+進入神經末梢內的量增加。Chen和Lee認為:電子顯微鏡下發現遞質囊泡被排空,遞質耗竭,最終使神經-肌肉興奮傳遞阻斷;而Kelly和Brow在神經末端觀察到Coated囊泡累積。Bowerd認為是神經末梢ATP的耗竭。Intira等認為是β-BuTx抑制膽鹼轉運系統造成ACh囊泡含量減少,最終導致ACh耗竭。
肉毒毒素(Botulin,BoTx)可拮抗β-BuTx,當神經肌肉標本用這兩種毒素同時處理時,神經肌肉阻斷所需的時間比用其中任一種毒素阻斷所需時間要長,因此實驗中可知β-BuTx是通過增加細胞內游離Ca2+濃度來拮抗BoTx的,但這兩種毒素相互拮抗的本質還不清楚。Othman用鼠腦突觸體研究β-BuTx作用機理時發現,β-BuTx在腦突觸體上結合位點可被dendrotoxin占據,但dendrotoxin卻沒有引起突觸體膜的去極化。
在一定條件下,通過電子顯微鏡觀察,β-BuTx能引起蟾蜍神經末梢質膜的大範圍損傷,但是,研究證實如此損傷並不是產生神經毒性作用,即引起神經肌肉阻斷所必需的。β-BuTx阻斷的大鼠外周神經末梢在遞質囊泡數目方面表現出輕微降低及質膜內折數目增加。Chen等認為這種形態學的變化是由於蛇毒導致遞質囊泡在出胞作用釋放出遞質後囊泡膜再循環受到抑制而引起的。早期研究報導稱β-BuTx引起的神經末梢阻斷標本中ACh數量正常,而Gunderson等研究稱:經β-BuTx孵育的膈神經-膈肌標本ACh水平增加了2~3倍。
β-BGT具有β類神經毒素的共同特點,在作用於神經末梢之前有一個5-20min的延遲期,為結合突觸細胞膜所必需,能夠阻礙可興奮膜上的K+的轉運;選擇性抑制神經末梢釋放乙醯膽鹼。它作用於運動神經末梢產生一種三相變化,首先是傳出遞質數量的迅速降低,即短暫抑制,繼而是釋放易化,隨後是進一步抑制,導致不可逆的傳導阻滯。該毒素誘導的系列變化可以通過測量單極運動終板記錄的動作電位或在低Ca2+濃度介質中測量孵育的離體小鼠膈肌神經-橫膈膜製備物的收縮力觀察到。β-BGT中毒後的運動神經末梢在軸膜上出現Ω型被膜竇數量的特徵性增加,而這時突觸前泡的數量及形狀變化不大。
β-BuTx阻斷膽鹼轉運到Torpedo電器官的神經末梢內,這與β-BuTx對鼠腦突觸體作用類似,但有些學者認為β-BuTx抑制膽鹼轉運過程不能解釋β-BuTx導致的神經肌肉阻斷作用。另外,β-BuTx也作用於非膽鹼結構,如GABA能神經元突觸體,這一現象同樣使β-BuTx在神經末梢的特殊作用位點是膽鹼轉運系統的提法不成立。Emmanuilo Delot在Torpedo突觸體上對多種突觸前PLA2神經毒的比較研究發現:Crotoxin和β-BuTx對突觸體的ACh釋放和膜去極化程度不同,認為這兩種毒素是從不同作用位點或不同機理來影響神經遞質釋放過程的。Howard認為:從β-BuTx對鼠腦突觸體和對Torpodeo突觸體的影響可得出,β-BuTx是通過改變離子通道或/和離子泵而發揮作用的。Ng和Howard提出:由於質膜上磷酸甘油酸分解可抑制膜蛋白的活性,β-BuTx可能通過水解某些特殊磷酸甘油酸,調節離子通道或/和離子泵的活化狀態。
磷脂酶活性 β-BGT的藥理學作用較為複雜,它的突觸前毒性作用依賴於內源性磷脂酶A2的效應,因此β-BGT具有神經毒素和磷脂酶A2的雙重作用,除了可抑制運動神經末梢釋放乙醯膽鹼和攝取膽鹼以及阻斷運動神經肌肉接頭部位的衝動傳遞外,還具有間接溶血作用。這是因為PLA2在Ca2+存在下能水解卵磷脂(專一水解C-2酯鍵)生成能溶解紅細胞的溶血卵磷脂。另外β-BGT還能減少膜結合的乙醯膽鹼數,抑制膜結合酶的活性等。
實驗證明β-BGT的A鏈具有PLA2酶活性而B鏈沒有。PLA2可催化3-sn -磷酸甘油酯2-乙脂鍵的水解。用p-BromophenocylBromide烷化活性位點的組氨酸殘基,不可逆地抑制了酶活性,同時也破壞了毒性。這說明在β-BGT中PLA2起到了不可缺少的作用。也有人對此提出了異議。但不管怎樣,既然存在不具有毒性的PLA2,就說明β-BGT毒性不能單獨歸於PLA2的活性。PLA2的活性與分析的條件有關。PLA2酶活性是否是β-BGT毒性的必要因素,Rosenberg列舉了正反兩方面的證據。關於PLA2對β-BGT所引起的運動神經末梢三相變化的影響研究表明初期的釋放抑制及其後的釋放易化都與PLA2無關,Strong(1976)首次報導了PLA2的催化活性在由β-BGT所引起的自發神經遞質釋放降低方面起著重要的作用。雖然A鏈具有PLA2活性,在毒素中具有重要作用,但是考慮到毒素與雞肌肉的結合能夠被樹眼蛇毒素、毒素I及曼巴蛇毒素k所抑制,所以B鏈在毒素中的結構和作用也就不能被忽視。B鏈作為識別亞單位可特異識別靶細胞膜阻斷電壓門控鉀通道。
β-BGT受體 β-BGT的受體(β-BGTR)主要位於胞突結合處的質膜上,在神經組織以外的地方不存在。這種受體可能是一種K+通道。常利用放射性標記來鑑定β-BGTR。研究檢測到了一些非組織特異性的低親和力的結合位點,一些作為潛在受體的高親和力的結合位點,這些受體呈低密度分布(150fmol/mg蛋白)於小鼠和雞腦的突觸質膜上,而其他組織沒有。β-BGT的與受體的結合可通過用蛋白水解酶預處理而消除,說明是一種蛋白,分子量為430000D,與β-BGT有很高的親和力(Kd=1nM),可用Tritonx-100從雞細胞膜上溶解下來。在雞腦SPM上還有一個95000D的多肽,也能夠標記,這種結合可以被樹眼蛇毒素非競爭性抑制,但不被其他β-神經毒素抑制。由β-BGT所引起的神經傳遞阻斷可由於預先用樹眼蛇毒素處理而減弱,考慮到β-BGT的B鏈與樹眼蛇毒素的同源性,說明這兩種毒素可能作用於突觸前細胞膜的同一受體上,但卻通過兩種不同的機制起作用,這種受體是一種鉀通道。
對大鼠腦突觸體作用 用β-BuTx對大鼠製備的腦突觸體進行短時間孵育後,Howard歸納出以下突觸體的改變:①接納和保留幾種遞質和非遞質複合物的能力降低,包括γ-氨基丁酸、去甲腎上腺素、5-羥色胺、膽鹼等;②ATP減少;③用螢光碳花青苷染色測得質膜電位降低。β-BuTx產生以上變化並沒有溶解突觸體,而且Howard認為β-BuTx最初的效果是突觸體質膜電位的降低,隨這發生突觸體ATP量減少,故ATP量減少的部分原因是由於它被Na+/K+-ATP酶所利用試圖去重新建立原有的膜電位。且他推測β-BuTx引起多種突觸體遞質釋放過程抑制是繼發效果,可能由於膜去極化和ATP庫的耗竭,但還沒有證據證實β-BuTx導致突觸體膜去極化中所涉及的離子流。Ng和Howard早期研究認為:β-BuTx對突觸體上述作用的強弱不依賴於細胞外的Na+濃度,故認為β-BuTx不是通過開放質膜上的Na+通道或抑制Na+/K+-ATPase活性而使突觸體去極化的。但Yates SL在實驗中發現β-BuTx在低濃度時(0.05~5nmol/L)不影響Na+/K+ATPase活性,當β-BuTx濃度較高時(50nmol/L)使Na+/K+-ATPase活性增加;通過與無神經毒性PLA2的比較研究發現,β-BuTx對突觸體膜去極化影響是通過β-BuTx上的PLA2作用使自由脂肪酸產量改變而介導的。
β-BuTx在大鼠腦室內注射時可引起大鼠死亡,死亡率高於用β-BuTx處理外周神經系統引起的大鼠死亡。腦內注射β-BuTx引起的死亡率次於腦室內注射引起的死亡率,腦內注射β-BuTx引起廣泛的神經元損傷,沒有明顯的膽鹼能結構的選擇性,如將β-BuTx注射到大鼠齒狀回,谷氨酸脫羧酶(ghitamatedecarboxylase,一種GABA能神經元的標記物)的活性下降時間過程與同一腦區的膽鹼乙醯基轉移酶(Cholineacetytransferas,一種膽鹼能神經元的標記物)活性下降的時間過程相平行。但仍不明白:非膽鹼能結構的損傷是β-BuTx對它的單獨直接作用,還是β-BuTx特異地作用於膽鹼能神經元末梢引起的繼發效應。
PLA2活性 無神經毒性的PLA2酶活性是β-BuTx的PLA2活性的20倍,但無神經毒性的PLA2在改變突觸體膜電位和膜轉運過程方面遠比β-BuTx低得多。關於這一點的進一步證據來源於對β-BuTx的化學修飾實驗,用ethoxyformicanhydride(EOFA)處理後的β-BuTx,其PAL2活性和神經毒性都喪失;如果EOFA處理時加入dihexnoyllecithin(DiC6),則β-BuTx的PLA2活性保留;但是,EOFA仍降低了β-BuTx的致死率和它引起神經肌肉標本阻斷的能力,故用EOFA和DiC6處理的最終結果是將β-BuTx從一種具有神經毒性的PLA2轉變到無神經毒性的PLA2。Howard和Troug提出:EOFA至少對β-BuTx進行了兩點改變:PLA2活性部位和神經毒性所需要的另一部位。酶分析實驗發現經EOFA和DiC6處理後無神經毒性的β-BuTx具有表面上正常的PLA2活性,但其已失去了改變突觸體膜電位和ATP貯存及膜轉運能力,故可得出結論β-BuTx的PLA2活性部位與其神經毒性部位是分離開的,但β-BuTx的神經毒性的發揮是這兩個部位的共同作用結果,甚至神經毒性部位比PLA2活性部位更重要。在有關β-BuTx與無神經毒性的PLA2的特異底物的比較研究方面,研究未發現二者在突觸體膜磷酯醯膽鹼、磷酯醯絲氨酸和磷酯醯乙醇胺的水解比例和釋放出突觸體脂肪酸類型方面有顯著性差異。而Ghassemi等在鼠腦突觸體質膜得出與以上相矛盾的結果,發現β-BuTx可引起質膜上磷酯醯乙醇胺和磷酯絲氨酸內外二層分布的改變,認為此改變可能與β-BuTx引起ACh釋放增加有關。
在有關β-BuTx與無神經毒性的PLA2對蛋白激酶作用的比較研究方面,Eiko Veno和PhilipRosenbergp發現:β-BuTx可抑制腦突觸體內大量蛋白(如突觸蛋白Ⅰ)的磷酸化作用,且作用比無神經毒性的PAL2強。即使在磷酸酯酶存在的情況下,β-BuTx抑制磷酸化作用也未見降低,說明β-BuTx對磷酸化作用的抑制可能與ACh釋放受抑制有關。Eiko進一步研究還發現無神經毒性的PLA2可抑制依賴cAMP的蛋白激酶、蛋白激酶C(PKC)的活性,而β-BuTx則無此效應,且無神經毒性的PLA2對蛋白激酶活性的抑制是通過產生自由脂肪酸來介導的,Eilo推測β-BuTx與無神經毒性的PLA2對磷酸化作用的抑制途徑是不同的。β-BuTx對中樞神經系統ACh釋放也有特異性。Chakpell在大鼠腦突觸體上發現低濃度β-BuTx對完整突觸體ACh釋放既有促進作用又有抑制作用。Chapell[39]認為β-BuTx對突觸體ACh釋放的抑制作用可能不發生在突觸體內囊泡與突觸質膜的相互作用水平上,而是發生在神經遞質釋放過程的早期。
毒素與基因工程 基因組 α-BGT的cD-NA序列包括信號肽序列,編碼成熟蛋白的序列和5,,3,-UTR序列。不同來源的α-BGT的cDNA有很高的同源性,其中信號肽序列和5,,3,-UTR序列保守並與眼鏡蛇科和海蛇科的序列完全一樣,由此可以推斷它們由同一個祖先進化而來的。α-BGT的cDNA全長約500 bp,其中5,-端約30bp,3,-端約200 bp為非蛋白編碼區域。編碼區編碼一個由21個胺基酸殘基組成的信號肽和一個74個胺基酸殘基組成的成熟蛋白質。Liu等從銀環蛇毒腺中提取α-BGT的總mRNA,擴增了α-BGT cDNA片段,其全長為530 bp,5,-UTR 33 bp,信號肽63 bp,編碼區222 bp,3,-UTR 195 bp,有一個終止密碼子TGA和AATAA信號polyA序列。α-BGTmRNA在同一個體中也存在多樣性,是由轉錄後編輯形成,還是由於實驗中反轉錄過程的錯誤、基因克隆中的偏差以及測序過程的誤差造成,或兩者都有,一直存有爭論。
α-BGT的基因組DNA有3個外顯子,被2個內含子分隔開。外顯子、內含子連線遵循GT/AG法則,啟動子序列和3,-UTR是高度保守的,TATA盒位於轉錄起始位點上游25~33 bp。Chang等從銀環蛇毒中提取了2個約2700bp的基因組DNA,即α-Bgt(A31)和α-Bgt(V31),它們表現出完全一樣的基因結構,含有3個外顯子基因,在同樣的位置插入2個內含子,且它們的核苷酸序列具有98%的同源性。內含子1的長度約為1800 bp,內含子2的長度約為540bp。跟短鏈神經毒素相比,發現內含子2的長度變化比較小,比內含子1保守,短鏈神經毒素和長鏈神經毒素的外顯子區域比內含子區域更具多樣化。林魯萍用引物擴增得到2655 bp的α-BGT基因。α-BGT編碼區共有288 bp,第1個外顯子包括58 bp的編碼區部分,編碼信號肽部分N端的20個胺基酸;外顯子2全長105 bp,編碼信號肽剩餘的4個胺基酸和成熟肽N端的33個胺基酸;外顯子3全長128 bp,包括編碼剩餘41個胺基酸部分和1個終止密碼子,翻譯出來的蛋白序列符合V31變體。得到序列的2個內含子分別為1790 bp和538 bp。
從銀環蛇毒中已分離出7種β-銀環蛇毒素異構體,除了A2鏈外,A1和A3鏈的cDNA還未克隆到。另外4個A鏈異構體(A4-A7)的cDNA已被克隆,3個B鏈cDNA已被克隆。現代色譜技術及胺基酸分析揭示至少有16種β-BGT亞型。A鏈與B鏈的分開可用二硫蘇糖醇還原鏈間二硫鍵,也可用2-巰基乙醇還原,然後用碘乙酸烷化。Long-Sen Chang等通過PCR擴增β-BGT的A鏈和B鏈基因,分析A鏈和B鏈基因的編碼區,發現有3個外顯子被2個內含子分隔開,外顯子和內含子連線遵循GT/AG法則。分析啟動子序列,得出結論:A鏈和B鏈由不同的基因編碼。這個結論支持完整的β-BGT來自轉錄後的A鏈和B鏈配對這個觀點。克隆到的A鏈樣基因全長3022 bp,外顯子1編碼5,-UTR,25個胺基酸殘基組成的信號肽和胺基酸殘基1-43,外顯子2編碼胺基酸殘基43-81,外顯子3編碼胺基酸殘基81-120和3,-UTR。克隆到的B1鏈基因長5062bp,外顯子1編碼5,-UTR,24個胺基酸殘基組成的信號肽,胺基酸殘基1-5,外顯子2編碼胺基酸殘基5-59,外顯子3編碼胺基酸殘基59-61和3,-UTR。
Cheng等根據β-BGT的B1鏈啟動子區域,非編碼區,B1鏈cDNA分別設計引物,擴增從銀環蛇提取的β-BGT的基因組,克隆到B1、B2、B4、B5、B6鏈的基因組,B2、B4鏈的長度分別為4699 bp、3243 bp。B5、B6鏈約為2000 bp,但不包括啟動子序列。同源比較6條B1鏈的胺基酸序列,顯示信號肽有24個胺基酸組成,2個內含子在相同的位置分隔編碼區域,B2和B4鏈第61位上的胺基酸不同,B5、B6在C末端和N末端缺少2個胺基酸,但是所有的B鏈都有7個半胱氨酸,位於7個不同的保守位點。比較6條鏈的基因組,發現內含子1長度幾乎一樣,內含子2長度變化很大,B4、B5、B6鏈缺少內含子2的2個區域,但是6條鏈在剪接位點附近的內含子2的序列是高度保守的。和眼鏡蛇的胰凝乳蛋白酶抑制劑基因作比較,發現有共同的基因組結構,而且核苷酸序列高度相似。
在研究銀環蛇毒蛋白酶抑制劑類蛋白質(PILP)時,Chang等克隆並表達了PILP-1,PILP-2,PILP-3。蛋白酶活性試驗表明,重組PILP-1能抑制胰蛋白酶的活性。比較PILP和B鏈的基因序列,發現有相同的基因結構,除了編碼信號肽的外顯子外,編碼蛋白質的外顯子比內含子更具多樣性。這表明,PILP基因和B鏈基因起源於公共的祖先,進化的加速可能使PILP基因和B鏈基因具多樣化。Wen-MinChou等發現PILP-3還是基質金屬蛋白酶-2的抑制劑,能抑制神經母細胞瘤的侵襲和遷移。
克隆和表達 蛇毒神經毒素主要來源於捕蛇或養蛇提取蛇毒後進行純化的方法進行。銀環蛇由於人工養殖成本高、周期長、越冬存活率極低,因此通過人工養殖獲得大量銀環蛇毒有較大困難,而野生銀環蛇也由於過度捕獵使銀環蛇種群數量逐年下降,加上銀環蛇列入國家一級保護野生動物,從野生來源獲得銀環蛇毒也有很大問題。因此從天然蛇毒中分離純化得到足夠數量的α-BGT、β-BGT以供科學研究和臨床治療比較困難,而通過基因工程得到足夠的α-BGT、β-BGT成為一條很好的途徑。
錢友存等從銀環蛇毒腺中抽提總RNA,RT-PCR擴增編碼β-銀環蛇毒素A鏈的cDNA,克隆並測定了一個新的β-BGT-cDNA全序列,命名為A7鏈,編碼含有27個胺基酸的信號肽和120個胺基酸的成熟蛋白,該成熟蛋白和其他β-銀環蛇毒素A鏈一樣,具有13個位置固定的半胱氨酸,而且和這些A鏈具有很高的同源性。將β-銀環蛇毒素A鏈cD-NA亞克隆到表達載體pMAL-p2上,轉化大腸桿菌BL21菌株,得到高效的可溶性融合蛋白,表達產物經Xα因子酶切後顯示較弱的磷脂酶A2活性。為闡明磷脂酶A2的作用機制和生物活性的研究提供了材料。
Wu等構建了β-銀環蛇毒素B鏈(B1和B2)的cD-NA。B鏈cDNA編碼24個胺基酸組成的信號肽和精氨酸為起始的由61個胺基酸組成的成熟蛋白。B1鏈cDNA全長425 bp,B2鏈cDNA全長328 bp。將B鏈亞克隆到表達載體PET-32α(+),轉化大腸桿菌BL21(DE3)。用His-Bind樹脂柱純化表達的硫氧還蛋白融合蛋白。B鏈用Ser代替Cys-55,親和純化的融合蛋白量至少增加100倍。如果用腸激酶切掉融合的硫氧還蛋白,則分離的B鏈不溶於水。林魯萍等用已經構建的pGEX-BgTX(P22-A31)質粒在大腸桿菌BL21(DE3)中表達,並用谷胱甘肽SepharoseFF純化GST-α-銀環蛇毒素融合蛋白,再用凝血酶切掉融合標籤谷胱苷肽轉移酶(Glutathione S-transferase,GST),得到了較純的重組α-銀環蛇毒素同工毒素,得率約為1.225 mg/L。用重組α-銀環蛇毒素製備多克隆抗體,經ELISA和Wastern雜交鑑定後確定重組α-銀環蛇毒素與天然α-銀環蛇毒素的抗原性一致。
胡延春等將擴增獲得的α-BGT基因連線至pUCm-T載體構建克隆質粒pUCm-α-BGT,克隆質粒雙酶切後連線至融合蛋白表達載體pGEX-4T-1中,轉化大腸桿菌BL21(DE3)進行IPTG誘導表達,表達產物經15% SDS-PAGE分析,得到約34 kD的重組α-BGT,其表達量約占細菌總蛋白的32.16%。Wastern blotting和間接ELISA檢測結果表明,α-BGT的融合表達蛋白也與天然的α-BGT標準品具有相似的抗原性。在大腸桿菌BL21(DE3)中的非融合型表達α-BGT占細菌總蛋白的11.98%,主要以包涵體形式存在,也與天然α-BGT標準品具有相似的抗原性。α-BGT基因失望克隆、表達和活性研究,為改造α-BGT基因,降低其毒性和用表達的重組α-BGT研究乙醯膽鹼受體提供了有效的途徑。
通過以上研究證明,用基因工程的方法獲得蛇神經毒素是可行的,且融合表達效率高,具有較好的可溶性。得到的重組毒素蛋白具有一定的生物活性,並與天然的蛋白有相似的免疫原性。但表達的重組α-BGT、β-BGT與天然的蛋白相比生物活性有所降低,這可能是因為α-BGT、β-BGT都具有多對二硫鍵,從而造成無論真核還是原核表達都不能完全正確摺疊恢復成天然構象,也可能是在表達純化的過程中一些試劑的影響,使部分蛋白構象改變而導致生物活性降低。
免疫學特性 α-BGT與乙醯膽鹼受體結合的親和力高,因此是研究乙醯膽鹼受體結構的理想探針,可用於顯示完整細胞膜表面乙醯膽鹼受體的分布和密度,觀察各種藥物、毒物和其他致病因子對乙醯膽鹼受體動力學變化的影響,也是從組織中分離和純化乙醯膽鹼受體的重要工具。20世紀70年代末,套用I125標記的α-BGT作配體來探測nAchR的數量對闡明重症肌無力(myastherniagravis,MG)的發病機制起了極大的作用。MG是nAchR自身免疫性疾病,利用α-BGT純化的nAchR作為抗原,免疫接種於動物,可製成自身免疫性重症肌無力的模型,為免疫調節診療的研究提供了必不可少的工具。莫雪安等利用α-BGT能特異性地不可逆地與突觸後膜乙醯膽鹼受體結合,β-BGT能特異性地不可逆地與突觸前膜的相應蛋白質結合的特性,將α-BGT和β-BGT混合一起包被酶標板,結合隨後加的肌肉提取液中相應蛋白質為抗原,以ABC-ELISA法檢測重症肌無力病人血清中混合的抗乙醯膽鹼受體抗體(AchRab)和抗突觸前膜受體抗體(PsmRab),稱為抗突觸受體抗體。結果:75名正常人均陰性。80例臨床對照組中,除2例運動神經元疾病和1例多發性肌炎陽性外,其餘均陰性。122例重症肌無力病人中98例陽性(80.3%,其中全身型陽性87.5%),陽性率明顯高於單獨檢測AchRab(P<0.001)。創建了重症肌無力診斷的一個陽性率較高的實驗室指標。
Yang和Chang在1998年利用雜交瘤技術製備了23種抗β-BGT單克隆抗體,其中7株可抑制β-BGT70%的PLA2的活性並中和毒素,在這7株中和單抗中有6株可識別A鏈上連續抗原表位,1株識別毒素的共同表位。利用合成肽段及蛋白酶分析確定了A鏈上6種單抗識別的胺基酸位點,其中單抗17識別位點31-37,單抗2和8識別46-51,單抗21和22識別91-98,單抗6識別100-106。水化位點分析顯示單抗17、21和22識別的抗原表位在親水區,單抗2和8的識別表位在中性區。一方面,抗原的外形結構信息預示單抗21和22的識別表位具有高免疫原性,單抗2和8的識別表位具有中等免疫原性,而單抗6和7的識別表位具有低免疫原性。鏈的彈性分析表明單抗2、8、17、21和22的識別表位在中等彈性區域,而單抗6的識別表位則位於低的彈性區域。從這些可以看出單抗6識別的抗原表位位於一個親水、鋼性和不易接近的位置,表明這個區域抗原性不高。在單抗2和8的結合位點46-51上存在PLA2酶活性所必需的His-48和Asp-49兩個位點,所以封閉這兩個位點能夠抑制β-BGT的酶活性和神經毒性,由於單抗8的親和活性大於單抗2,所以單抗8抑制β-BGT的酶活性和神經毒性的能力更大一些。同樣Asp-92也是PLA2酶活性所必需的位點,因此單抗21和22也能抑制β-BGT的生物活性。參考牛胰PLA2的晶體結構,Tyr-28、Gly-30D羧基,Gly-32,和氧籠一起捕獲Ca2+。從以上觀察可知單抗17能夠結合Gly-32,從而抑制β-BGT的PLA2活性。
競爭性抗體結合抑制實驗表明這些中和抗體與抗原的親和性與合成的短肽兼容。利用合成的短肽A(31-37)、A(46-51)、A(91-98)和A(100-106)含有β-BGT的中和抗原表位,將這些短肽與BSA偶聯,注射小鼠,4周后小鼠體內抗體達到最高水平,可起到很好的免疫保護作用,為研究毒素疫苗做了準備。1999年Yang和Chang利用木瓜蛋白酶水解純化的單抗製備並研究了Fab片段的活性。通過研究Fab片段組成的可溶性複合物的分子量表明β-BGT、A鏈及B鏈的抗原決定簇數目分別為7、5和2。另外23種β-BGT單抗還用來確定β-BGT與β-BGT家族其他成員及其他毒素的交叉反應。
套用 蛇毒神經毒素能抑制中樞神經系統,尤其是延髓呼吸中樞,對周圍神經系統的作用主要是阻斷神經-肌肉接頭處衝動的傳導,導致骨骼肌尤其是呼吸肌癱瘓。林魯萍等採用小鼠化學法鎮痛試驗表明,重組α-銀環蛇毒素有一定的鎮痛藥效,在外周鎮痛作用中呈一定的量效關係。於是人們根據蛇毒α-神經毒素這一性質開發出了不成癮的新型鎮痛藥,用於鎮痛、麻醉和戒毒。神經毒素的鎮痛作用與阿片類鎮痛藥物相比起效較慢,一般肌肉注射或腹腔注射的起效時間在1h以上,3-5h達高峰。β-銀環蛇毒素主要用於醫學藥理學和分子免疫學,製備單克隆抗體,在蛇毒的檢測、蛇咬傷中毒的預防和救治等方面具有重要意義。通過研究PLA2酶活性可以幫助了解磷脂在生理生化過程中的作用。利用β-BGT還可以研究突觸前神經遞質傳遞的機制。
銀環蛇毒素可作為抗癌藥物使用,抑癌的主要成分是精氨酸酯酶類,能破壞癌細胞的物質是磷酯酶A2,此類物質可與敏感的細胞膜磷脂成分結合,破壞細胞膜結構而使細胞溶解其膜活性多肽,對細胞膜有特殊作用,能增加細胞膜的通透性,有利於抗癌藥物進入癌細胞而增強抑癌效果。
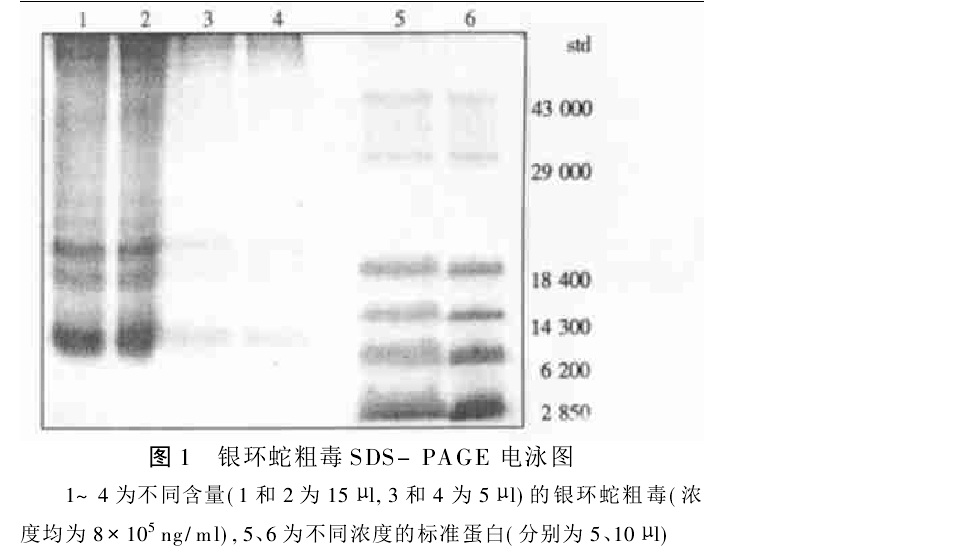 銀環蛇毒素粗毒電泳圖
銀環蛇毒素粗毒電泳圖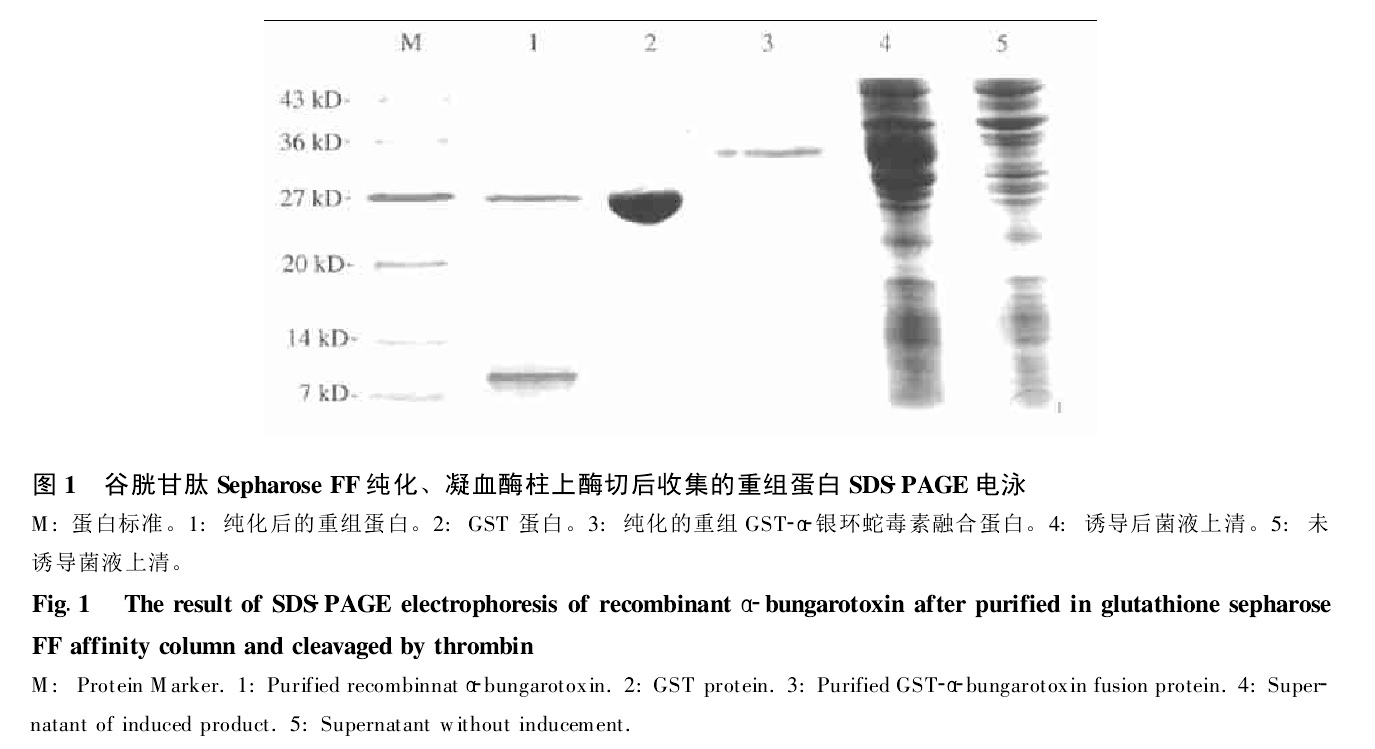 純化後的蛇毒蛋白電泳圖
純化後的蛇毒蛋白電泳圖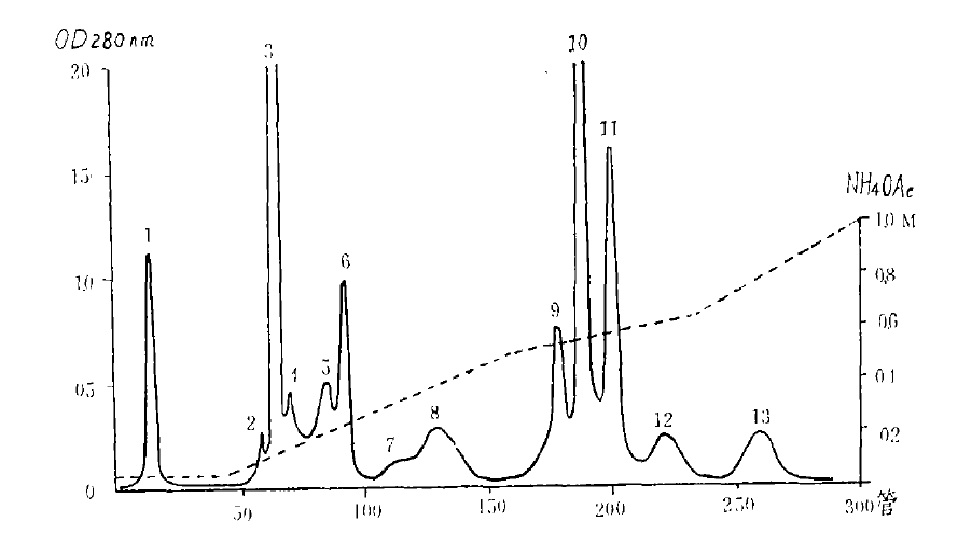 銀環蛇毒素層析分離圖譜
銀環蛇毒素層析分離圖譜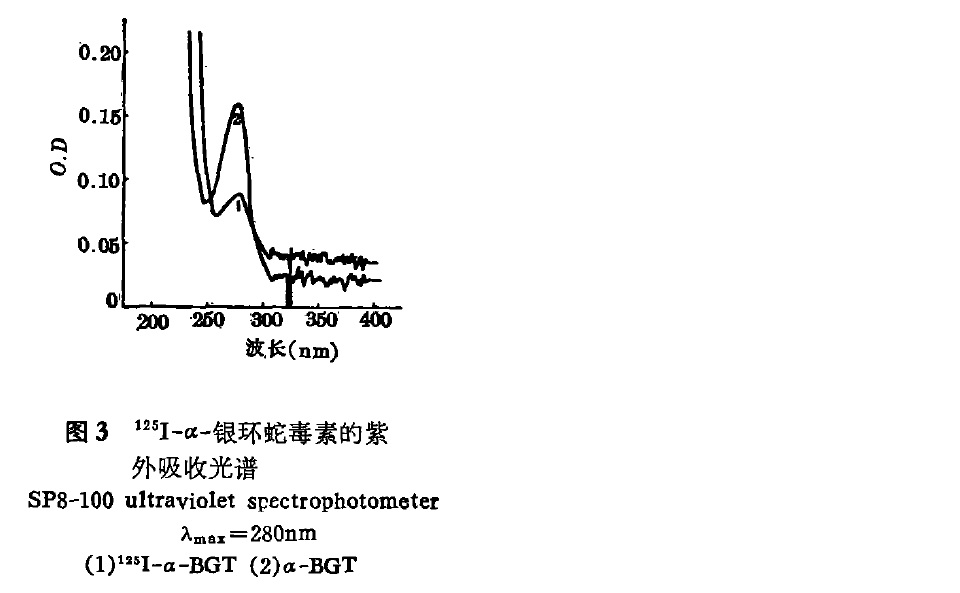 α銀環蛇毒素紫外光譜
α銀環蛇毒素紫外光譜