鉛扣是指一氧化鉛還原為金屬鉛並和貴金屬一起沉入容器底部,冷卻後變成一個含有貴金屬、大量金屬鉛和其它金屬雜質的金屬小球。
基本介紹
- 中文名:鉛扣
- 外文名:Lead buckle
- 用於:金的純度測定中
- 形狀:金屬小球
- 材質:一氧化鉛
- 學科:冶金工程
簡介,矽酸度對鉛扣大小的影響,覆蓋劑對鉛扣大小的影響,總結,
簡介
在對金的純度測定中,熔樣時將粉碎好的試樣與適當配方的熔劑如碳酸鈉、硼砂、玻璃粉、一氧化鉛、食鹽、麵粉等混勻,加熱熔融。一氧化鉛還原為金屬鉛並和貴金屬一起沉入容器底部,冷卻後變成一個含有貴金屬、大量金屬鉛和其它金屬雜質的金屬小球俗稱鉛扣。
矽酸度對鉛扣大小的影響
在增鍋試金法的熔煉過程中,配料不當會發生硫化反應。當毓作為捕集劑時,有意識地加入硫化劑和金屬氧化物,促使硫化反應順利進行,生成的毓可捕集樣品中的貴金屬元素;含C u, N i, F e的硫化礦物的試樣,在鉛試金分析過程中,如配料不當,試樣中的S和Cu, N i Fe形成毓(即冰銅FeS -Cu2混合物),這是不希望的硫化反應。因為融體中生成了一層毓,介於扣與渣之間,能捕集貴金屬,導致貴金屬的損失。硫化銅礦在鉛試金熔煉時,為了避免毓生成,在配料時加入大量的PbO,NaCO3,其作用有三:一是排除試樣中雜質Cu、Ni、Sn、Zn、Mn、Al等的干擾;二是脫硫,防止冰銅的生成;三是調節渣的熔點,防止“粒狀鉛”,的生成。
因此,經過造渣等反應後的熔渣呈鹼性,矽酸度在1.0以下,表3所列的是國內某銅精礦不同矽酸度對鉛扣重量、Au,Ag分析結果的影響。
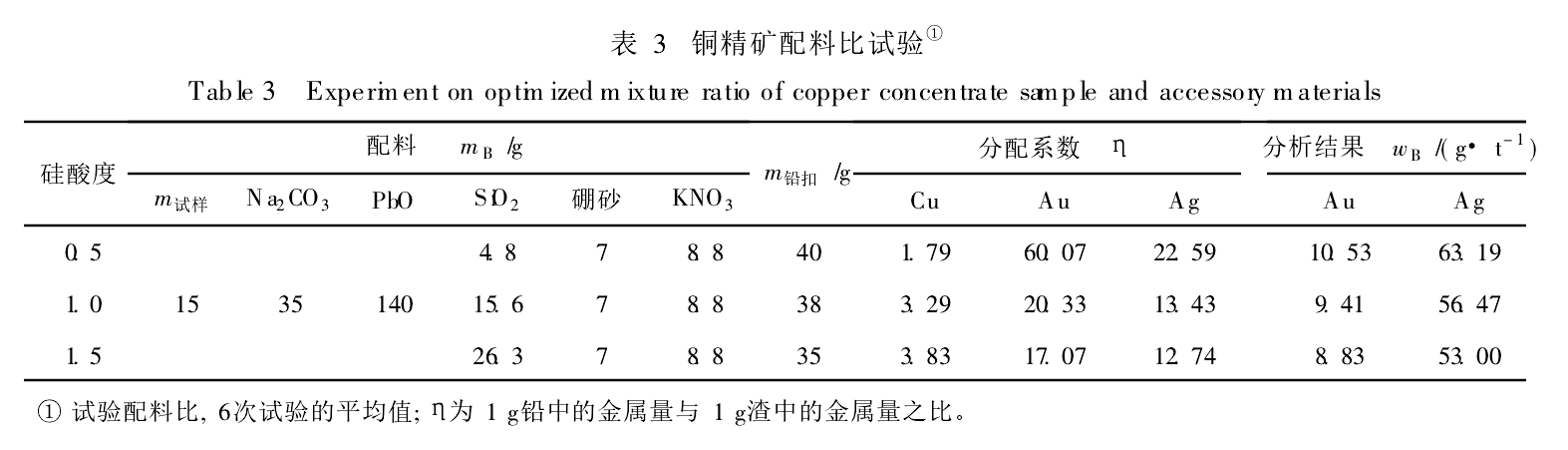
由表3可知,隨著矽酸度的增加,鉛扣的重量下降,分析結果降低。其原因之一是硫化物發生了如下反應:
2kNO3+FeS2+SiO2
K2O·FeO·SiO2+2SO2↑+N2↑
反應結果使得硫的還原能力下降,這是由於隨著矽酸度增大,渣的流動性差,硫沒有徹底脫淨所致。這樣,渣中所含的金屬硫化物顆粒增多,產生微觀的“冰銅效應”,吸附少量的Au, Ag導致Au,Ag的分析結果偏低。因此,對於銅精礦樣品分析矽酸度應控制在0.5左右,根據樣品組成計算配料時需要加入的PbO, SiO2及硼砂的量。
覆蓋劑對鉛扣大小的影響
在試金分析中,一般加覆蓋劑食鹽,而國際標準不加食鹽。加入食鹽的優點是在800℃熔融,熔化後形成很稀的流體,它浮在熔融體表面自成一相,因而能隔絕空氣並能防止熔融體沸騰時的濺失。覆蓋劑的影響列於表4。
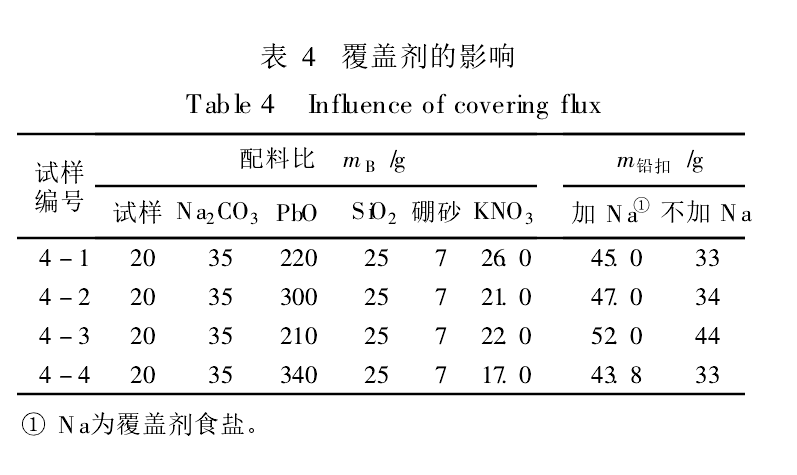
由表4可知,在氧化劑數量相同的條件下,覆蓋劑食鹽的加入使得硫的有效還原能力提高,鉛扣的重量增加。因此在加覆蓋劑的情況下適當加入氧化劑,能使鉛扣的重量符合要求。
總結
採用控制鉛扣的平衡方程式的情況看:採用控制鉛扣公式後,因鉛扣不合格而造成返工的現象明顯下降。隨著試金分析試樣的增多,採用該公式,具有節省分析時間、節約原材料,僅此一項每年節約分析成本近萬元,而且分析結果報出及時率明顯提高,因此,具有推廣套用價值。

