赤型異構體為描述一些開鏈含2個手性中心化合物的構型,由赤蘚糖(erythrose)派生出來的術語。
基本介紹
- 中文名:赤型異構體
- 外文名:erythrose
- 構型:手性中心化合物
- 來源:赤蘚糖
- 別稱:赤式異構體
- 學科:化學
定義,舉例,相關概念,對映異構體,非對映異構體,幾何異構,旋光異構,構象異構,表示法,親核取代反應,立體化學,
定義
赤蘚糖是含有2個不同手性碳原子的四碳醛糖,它有一對對映體,即D-和L-赤蘚糖,其費歇爾投影式的2個-OH位於碳鏈同側。其他含有2個手性碳原子的化合物,若分別連有2個相同的基團、第三個基團不同時,其費歇爾投影式的2個相同的基團位於碳鏈同側的;即稱該分子為赤式異構體,而此種構型稱赤式構型(erythro configuration),以區別它的非對映異構體蘇式構型。
舉例
與蘇阿糖構型相似者為蘇式構型;與赤蘚糖構型相似者為赤式構型。例:

相關概念
對映異構體
簡單的說也就是兩個異構體之間的關係就如同一個物體的立體結構在照鏡子,這個立體結構和它在鏡子中的像互為對映異構體。
1、兩個互為鏡像而不能重合的立體異構體,稱為對映異構體,簡稱對映體。
對映體對偏振光的作用不同,它們的比旋光度數值相同,但方向相反。對映體的生物活性不相同,化學反應中表現出等速率。等量的左旋體與右旋體的混合物構成外消旋體。從對映體中分離出單純一個光學異構體的方法稱拆解。最普通的拆解方法是將消旋體與光學活性相反的離子(稱拆解劑)作用生成非對映體。
非對映異構體
兩個結構相同的分子,由於具有構型不同的不對稱原子,彼此不呈實物與鏡像的關係。
非對映異構體是由已含有一個手性中心的分子產生第二個手性中心時的必然產物。與對映體的生成不同,由於第一個手性中心的影響,所得到的兩個非對映異構體的數量並不相同。這就是不對稱合成的基礎。
幾何異構
旋光異構
構象異構
能發生立體異構現象的化合物稱作立體異構體,包括幾何異構體、旋光異構體和構象異構體。幾何異構體和旋光異構體能分離開來,構象異構體可以通過單鍵旋轉而互變,通常無法分離,但當圍繞單鍵旋轉障礙很大時,這類異構體也是可以分離的。
表示法
在有機化學教學中,為了更好地表示反應過程中的立體化學,化學家想了許多辦法儘量在紙面上反映出分子的立體形象,用以準確地闡明反應過程中手性碳原子的構型問題。
特別是在研究反應歷程時,對於僅涉及到兩個手性碳反應物分子,其分子構型人們常借用赤式和蘇式的飛楔式表示法。這種表示法在紙面上能局部地反映出分子的立體形象,且書寫方便,節省篇幅。但正如前面所述,仍存在著一定的局限性。尤其對初學有機化學的人要理解這種表示法的含義仍然是較為困難的。如採用赤式和蘇式的Newman 投影表示法,則能獲得較為滿意的效果。
親核取代反應
飽和碳原子上的親核取代是一類極為重要的有機合成反應,其歷程研究得較為深入和廣泛。SN1,SN2已是公認的。(部分反應歷程為SNi )。研究親核取代反應的立體化學,對於認識反應歷程更具有重要意義。
SN2反應常伴隨構型轉化,它的立體化學特徵尚好描述,已研究得較為清楚,也好講授。但SN1反應的立體化學卻是較為複雜的。實驗結果指出,在SN1 反應中立體化學常表現以下幾種情況:
1、外消旋化;
2、部分或100 % 構型保持;
3、部分或~100% 構型轉化。
以下就SN1反應中構型保持問題加以討論。
一般而論,在SN1取代反應中,構型能否保持大致可取決於兩種情況, 一是碳架不能翻轉,像某些脂環族化合物,橋頭碳發生的取代反應,由於碳架的固定,反應後的構型也必須保持原來的樣子,第二種情況是被取代的原子如在鄰位上有鹵素,羧基負離子或苯基時, 取代反應也常得構型保持或部分構型保持產物。即所謂的鄰基參與效應,以下舉苯基的鄰基參入說明之。
研究(+) 一蘇式—3—苯基丁醇一2 的對甲苯磺酸酯在醋酸中的溶劑分解反應形成( ±) 一蘇式產物,如利用C 14 標記原料中的一個甲基,可證明產物 (±)一赤式一3 一苯基丁醇一2 的對甲苯磺酸酯起溶劑分解反應得到產物構型保持不變。像這樣一個由於苯基參與而形成的苯基正離子的溶劑解反應的立體化學轉化如用Newman 投影式表示,讀者會感到這一反應的更為清晰的立體形象。

立體化學
1、E2消去反應
形成烯烴的消去反應同樣是一類在理論和實際上都很重要的反應,其歷程也包括單分子消去( E1) 和雙分子消去( E2),但消去反應中,涉及較多的是雙分子消去中立體化學問題。一般而論, E 2的消去多按反式方式進行,即所謂反式消去優勢。如1 , 2 一二溴一
1 , 2 一二苯乙烷在鹼的作用下,消去一分子HBr,生成1一溴一1 , 2 一二苯乙烯。
如果反應均按正常的反式消去進行,則赤式和蘇式所得到的烯烴的構型是不同的,前者得順式產物,後者得反式產物。用一般的飛楔式表示這一消去反應的立體化學過程不如用Newman投影式描述得清楚。
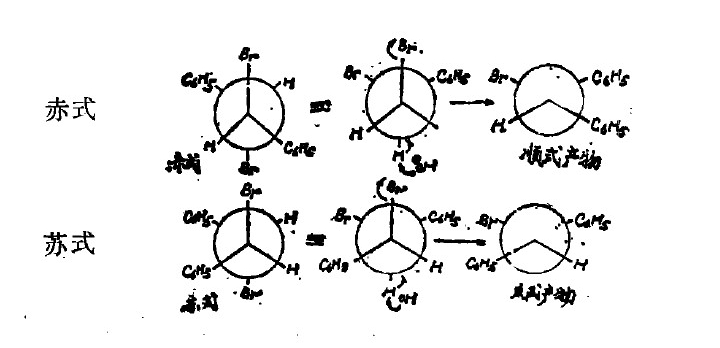 反式消去產物占優勢
反式消去產物占優勢2、熱消去反應
羧酸酯在加熱情況下( 400一600C) 的消去反應一般是通過六環狀過渡態發生的順式消去。例如加熱化合物赤式及蘇式2 一氘一1 , 2 一二苯乙醇的乙酸醋,赤式得到含D 的( E )一1 , 2 一二苯基乙烯,蘇式消去得不到含D 的烯烴,確證消去反應是按順式方式進行的。不過這一順式消去反應如用Newman 投影式表示則學生們能看得更為清楚,如下圖所示
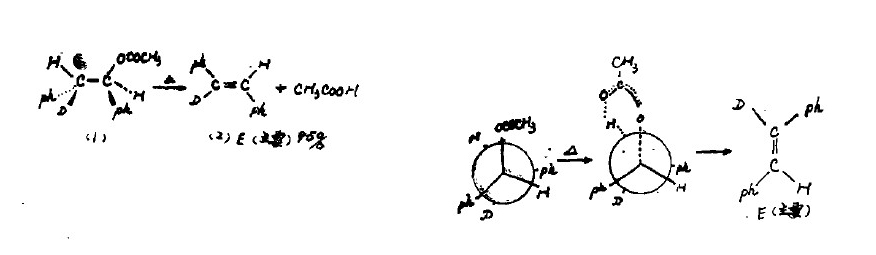
叔胺氧化物能在比較緩和條件下( 100一150C ) 熱介經五元環過渡態發生順式消去形成烯烴,主要生成Hofman烯烴。在Sayteff烯烴中反式比例大於順式。這一反應如改用
Newman 投影式表示比用一般教科書中所採用的飛楔式表示好。Newman式表示:


