變質反應(metamorphic reaction)是變質作用過程中形成新礦物的化學反應。變質反應的主要特點是,有關反應是在岩石基本上保持固態條件下進行的,而且新礦物的形成和原有礦物的分解同時發生。
基本介紹
- 中文名:變質反應
- 外文名:metamorphic reaction
- 性質:變質過程形成新礦物的化學反應
- 特點:新礦物和原有礦物同時發生
形成因素,反應類型,脫水,脫碳酸,
形成因素
溫度、負荷壓力和流體壓力是控制變質反應的主要因素。根據反應物和生成物的性質可將變質反應分為如下類型:①固體反應,包括同質多象轉變、固溶體出溶、固相之間反應等;②脫揮發分反應,包括脫水反應和脫碳酸反應;③氧化還原反應,生成其他物質,包括水,氧化物等。 變質反應
變質反應
 變質反應
變質反應反應類型
脫揮發分反應,按揮發分,又分為下列2類:
脫水
在變質作用中,由於溫度的升高,原岩中某些礦物所含的水在礦物晶體格架中變為不穩定而釋出,使礦物變為含水少的或不含水的礦物。如原岩中的高嶺石和石英,在溫度升高到300℃時,發生化學反應,形成葉蠟石和自由水分子。其反應式為 變質反應1
變質反應1
 變質反應1
變質反應1反應受溫度和流體壓力(p1)的控制,當p1=pS(岩壓)時,反應隨溫度的增高向右進行,使高嶺石失水,形成含水少的葉蠟石。若流體壓力增高,則不利於葉蠟石的形成。溫度達到400℃時,發生下列反應:
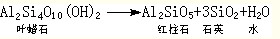 變質反應2
變質反應2形成不含水的紅柱石和石英。反應的脫水程度主要受溫度的控制,因此它可以作為劃分變質程度的標誌(見圖)。圖中兩條脫水反應曲線的斜率很陡,幾乎平行壓力軸,因此礦物相的轉變主要取決於溫度的變化。
在變質反應中,還區分出不連續反應和連續反應。前者指在變質反應中,形成新相(礦物)的反應,這時溫度和壓力是唯一的一對強度因素,形成一條單變反應曲線,在單變反應曲線的兩側各自有一組礦物相是穩定的。後者指在變質反應中,溫度和壓力變化可使礦物的成分發生連續變化。當反應趨向於另一邊時,新生成的礦物是由於反應礦物的組分發生部分遷移所形成,但反應礦物組合本身仍可繼續存在。因此在一定溫度和壓力區間內,反應礦物和生成礦物可以同時存在。
脫碳酸
碳酸鹽岩石在變質過程中釋放出CO2,如 變質反應
變質反應
 變質反應
變質反應但在一般情況下,碳酸鹽岩的反應常為H2O和CO2的混合氣相反應,即 變質反應
變質反應
 變質反應
變質反應 變質反應
變質反應可以單獨成為反應平衡中的強度因素。
固體反應,在反應過程中沒有揮發分參加。又可進一步劃分為以下類型。①同質多象轉變,如 Al2SiO5的3個變體的轉變:紅柱石匑藍晶石匑夕線石,石英匑鱗石英,α-石英匑β-石英等反應。②有序-無序反應:微斜長石匑正長石,在此反應中某些元素(如Al)在低溫時為有序,高溫時變為無序。③混合反應:如高溫時鈉長石和正長石混合形成均勻的鹼性長石固溶體,冷卻時出溶成為兩相交生。④固相之間的反應:如鈉長石→硬玉+石英,在變質岩中這類反應是判別溫度和壓力條件的重要標誌,因為它們不受揮發分(如H2O、CO2等)化學位的影響。
③氧化還原反應。
鐵在潮濕的空氣中可以生成氧化鐵,Fe2O3。
鐵本身是單質。但是在潮濕的空氣中有水和氧,在一起發生變質反應,生成了鐵鏽。
除上述反應外,還有交代反應、重結晶反應等。
