諾和平(地特胰島素注射液),適應症為用於治療糖尿病。
基本介紹
- 藥品名稱:諾和平?
- 藥品類型:處方藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,核准日期,
成份
活性成份:地特胰島素(通過基因重組技術,利用酵母生產的)。1單位(U)相當於0.142mg不含鹽的無水地特胰島素。1單位(U)地特胰島素相當於1國際單位(IU)人胰島素。
化學名稱:賴氨酸[sup]B29[/sup](N[sup]ε[/sup]-十四醯)去(B30)人胰島素
化學結構式:
分子式:C267H402N64O76S6
分子量:5916.9
其他成份:甘露醇、苯酚、間甲酚、醋酸鋅、二水合磷酸氫二鈉、氯化鈉、鹽酸、氫氧化鈉、注射用水。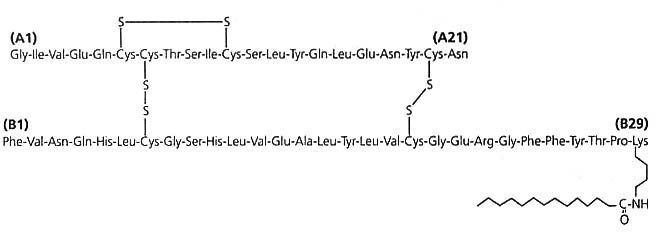
化學名稱:賴氨酸[sup]B29[/sup](N[sup]ε[/sup]-十四醯)去(B30)人胰島素
化學結構式:
分子式:C267H402N64O76S6
分子量:5916.9
其他成份:甘露醇、苯酚、間甲酚、醋酸鋅、二水合磷酸氫二鈉、氯化鈉、鹽酸、氫氧化鈉、注射用水。

性狀
本品為無色澄明液體。
適應症
用於治療糖尿病。
規格
300單位/3ml/支(筆芯)
用法用量
本品是可溶性的基礎胰島素類似物,其作用平緩且效果可以預見,作用持續時間長。
與其他胰島素製劑相比,地特胰島素治療引起的體重增加較少。
與其他胰島素相比較,本品引起夜間低血糖的風險較低,因而可以進行更為積極的劑量調整以實現血糖達標。
以空腹血糖作為評價指標,地特胰島素較人NPH胰島素可以更好地控制血糖。
與口服降糖藥聯合治療時,推薦地特胰島素的初始治療方案為每日一次給藥,起始劑量為10U或0.1-0.2U/kg。
地特胰島素的劑量應根據病情進行個體化的調整。
根據臨床研究結果,推薦以下劑量調整指南:
早餐前平均自測血糖濃度(SMPG) 地特胰島素劑量調整
]10.0mmol/L(180mg/dL) +8
9.1-10.0mmol/L(163-180mg/dL)+6
8.1-9.0mmol/L(145-162mg/dL) +4
7.1-8.0mmol/L(127-144mg/dL) +2
6.1-7.0mmol/L(109-126mg/dL) +2
如果其中一次SMPG測量在此區間
3.1-4.0mmol/L(56-72mg/dL) -2
當地特胰島素作為基礎-餐時胰島素給藥方案的一部分時,應根據患者的病情,每日注射一次或兩次。
本品用量因人而異。應由醫生根據患者的病情,每日注射一次或者兩次。
對於為達到最佳的血糖控制而每日î射兩次的患者,晚間注射可在晚餐時、睡前或者早晨注射12小時後進行。
由其他胰島素轉用本品:
由中效或者長效胰島素轉用本品的患者,可能需要調整î射劑量和注射時間。
和所有的胰島素一樣,在轉用本品期間和在本品開始治療的幾周內,建議密切監測血糖水平。
本品和抗糖尿病藥物同時使用時,可能需要調整同時使用的短效胰島素的劑量和î射時間,或者口服降糖藥的劑量。
本品和所有的胰島素一樣,對於老年患者和腎功能或肝功能不全的患者,應該密切監測血糖水平,並根據每個患者的不同病情調整劑量。
如果患者體力活動增加、日常飲食改變或者在伴發疾病期間,也可能需要調整劑量。
本品經皮下注射,皮下注射部位可選擇大腿、腹壁或者上臂。應在同一注射區域內輪換注射點。
如何使用本品的說明
本品應與諾和諾德胰島素注射系統和諾和針®配合使用。
如患者同時接受本品和另一種胰島素筆芯治療, 應分別使用諾和諾德公司生產的兩個胰島素注射系統,每個注射系統分別用於注射不同種類的胰島素。
本品僅供一人專用。本品不可重新灌裝使用。
使用本品前
• 確認胰島素類型正確。
• 使用前請檢查本品,包括橡皮活塞。如有任何損壞,或者未使用過的筆芯的橡皮活塞與白色條碼帶分離,即兩者之間出現間隙,請不要使用。並將產品退回供應商。
• 使用醫用棉簽消毒橡皮膜。
• 每次注射都應使用新的針頭以避免污染。
不能使用本品的情況
• 胰島素泵。
• 如果筆芯或裝有筆芯的器械發生墜落,損壞或受到擠壓,則有胰島素外漏的危險。
• 如果本品貯藏不當或被冷凍。
• 如果本品不呈無色澄明液體。
如何注射本品
• 本品皮下注射。注射技巧請參照注射系統使用說明。
• 在從皮下拔出針頭之前,應始終按住注射推鍵。注射後針頭應在皮下停留至少6秒,以確保胰島素完全注射入體內。
• 每次注射後必須卸下並丟棄針頭。否則,藥液可能會漏出,導致劑量不準確。
與其他胰島素製劑相比,地特胰島素治療引起的體重增加較少。
與其他胰島素相比較,本品引起夜間低血糖的風險較低,因而可以進行更為積極的劑量調整以實現血糖達標。
以空腹血糖作為評價指標,地特胰島素較人NPH胰島素可以更好地控制血糖。
與口服降糖藥聯合治療時,推薦地特胰島素的初始治療方案為每日一次給藥,起始劑量為10U或0.1-0.2U/kg。
地特胰島素的劑量應根據病情進行個體化的調整。
根據臨床研究結果,推薦以下劑量調整指南:
早餐前平均自測血糖濃度(SMPG) 地特胰島素劑量調整
]10.0mmol/L(180mg/dL) +8
9.1-10.0mmol/L(163-180mg/dL)+6
8.1-9.0mmol/L(145-162mg/dL) +4
7.1-8.0mmol/L(127-144mg/dL) +2
6.1-7.0mmol/L(109-126mg/dL) +2
如果其中一次SMPG測量在此區間
3.1-4.0mmol/L(56-72mg/dL) -2
當地特胰島素作為基礎-餐時胰島素給藥方案的一部分時,應根據患者的病情,每日注射一次或兩次。
本品用量因人而異。應由醫生根據患者的病情,每日注射一次或者兩次。
對於為達到最佳的血糖控制而每日î射兩次的患者,晚間注射可在晚餐時、睡前或者早晨注射12小時後進行。
由其他胰島素轉用本品:
由中效或者長效胰島素轉用本品的患者,可能需要調整î射劑量和注射時間。
和所有的胰島素一樣,在轉用本品期間和在本品開始治療的幾周內,建議密切監測血糖水平。
本品和抗糖尿病藥物同時使用時,可能需要調整同時使用的短效胰島素的劑量和î射時間,或者口服降糖藥的劑量。
本品和所有的胰島素一樣,對於老年患者和腎功能或肝功能不全的患者,應該密切監測血糖水平,並根據每個患者的不同病情調整劑量。
如果患者體力活動增加、日常飲食改變或者在伴發疾病期間,也可能需要調整劑量。
本品經皮下注射,皮下注射部位可選擇大腿、腹壁或者上臂。應在同一注射區域內輪換注射點。
如何使用本品的說明
本品應與諾和諾德胰島素注射系統和諾和針®配合使用。
如患者同時接受本品和另一種胰島素筆芯治療, 應分別使用諾和諾德公司生產的兩個胰島素注射系統,每個注射系統分別用於注射不同種類的胰島素。
本品僅供一人專用。本品不可重新灌裝使用。
使用本品前
• 確認胰島素類型正確。
• 使用前請檢查本品,包括橡皮活塞。如有任何損壞,或者未使用過的筆芯的橡皮活塞與白色條碼帶分離,即兩者之間出現間隙,請不要使用。並將產品退回供應商。
• 使用醫用棉簽消毒橡皮膜。
• 每次注射都應使用新的針頭以避免污染。
不能使用本品的情況
• 胰島素泵。
• 如果筆芯或裝有筆芯的器械發生墜落,損壞或受到擠壓,則有胰島素外漏的危險。
• 如果本品貯藏不當或被冷凍。
• 如果本品不呈無色澄明液體。
如何注射本品
• 本品皮下注射。注射技巧請參照注射系統使用說明。
• 在從皮下拔出針頭之前,應始終按住注射推鍵。注射後針頭應在皮下停留至少6秒,以確保胰島素完全注射入體內。
• 每次注射後必須卸下並丟棄針頭。否則,藥液可能會漏出,導致劑量不準確。
不良反應
患者使用本品時發生的不良反應主要與劑量相關,且與胰島素藥理學作用有關。低血糖是常見的不良反應。如果胰島素使用劑量遠高於需要量,就可能發生低血糖。臨床研究表明,大約有6%的患者在使用本品治療時會發生重度低血糖(指需要他人協助處理的低血糖)。重度低血糖可能導致意識喪失和/或驚厥以及暫時性或永久性腦功能損害甚至死亡。
與人胰島素相比,地特胰島素治療過程中的注射部位反應發生頻率更高。這些反應包括î射部位發紅,炎症,淤血,腫脹和瘙癢。上述反應多為輕微和一過性的,通常在繼續治療幾天至幾周內消失。
據估計,大約有12%的患者在使用本品治療時會發生不良反應。
總結臨床試驗中不良反應的發生頻率,經過總體判斷認為和本品相關的不良反應如下:
代謝和營養失調
常見不良反應(大於1/100,小於1/10)
低血糖:
低血糖症狀通常會突然發生,表現為出冷汗、皮膚蒼白髮冷、疲乏、神經緊é或震顫、焦慮、異常疲倦或衰弱、意識模糊、難以集中注意力、嗜睡、過度飢餓、視覺異常、頭痛、噁心和心悸。重度低血糖可導致意識喪失和/或驚厥及暫時性或永久性腦功能損害甚致死亡。
全身不適和射部位異常
常見不良反應(大於1/100,小於1/10)
注射部位反應:
在胰島素治療期間,可能會發生注射部位局部的過敏反應(如:紅、腫和瘙癢)。上述反應通常為一過性的,在繼續治療的過程中會消失。
少見不良反應(大於1/1,000,小於1/100)
脂肪代謝障礙:
注射部位可能會發生脂肪代謝障礙。通常是由於未在注射區域輪換注射點所致。
水腫:
胰島素治療的初期會出現水腫現象。這種現象通常為一過性的。
免疫系統失調
少見不良反應(大於1/1,000,小於1/100)
過敏反應,潛在的過敏反應,蕁麻疹,皮疹, 出疹。
這些症狀可能是由於全身性過敏反應所致。全身性過敏反應的其他症狀可能包括瘙癢、出汗、胃腸道不適、血管神經性水腫、呼吸困難、心悸與血壓下降。全身性過敏反應有可能危及生命(超敏反應)。
視覺異常
少見不良反應(大於1/1,000,小於1/100)
屈光不正:
胰島素治療的初始階段,可能會出現屈光不正。這種現象通常為一過性的。
糖尿病視網膜病變:
長期血糖水平控制良好可以降低糖尿病視網膜病變的風險。
然而因強化胰島素治療而突然改善血糖水平控制可能會發生糖尿病視網膜病的暫時惡化。
神經系統異常
罕見不良反應(大於1/10,000,小於1/1,000)
周圍神經系統病變:
快速改善血糖水平控制可能發生急性痛性神經病變,這種症狀通常是可逆的。
與人胰島素相比,地特胰島素治療過程中的注射部位反應發生頻率更高。這些反應包括î射部位發紅,炎症,淤血,腫脹和瘙癢。上述反應多為輕微和一過性的,通常在繼續治療幾天至幾周內消失。
據估計,大約有12%的患者在使用本品治療時會發生不良反應。
總結臨床試驗中不良反應的發生頻率,經過總體判斷認為和本品相關的不良反應如下:
代謝和營養失調
常見不良反應(大於1/100,小於1/10)
低血糖:
低血糖症狀通常會突然發生,表現為出冷汗、皮膚蒼白髮冷、疲乏、神經緊é或震顫、焦慮、異常疲倦或衰弱、意識模糊、難以集中注意力、嗜睡、過度飢餓、視覺異常、頭痛、噁心和心悸。重度低血糖可導致意識喪失和/或驚厥及暫時性或永久性腦功能損害甚致死亡。
全身不適和射部位異常
常見不良反應(大於1/100,小於1/10)
注射部位反應:
在胰島素治療期間,可能會發生注射部位局部的過敏反應(如:紅、腫和瘙癢)。上述反應通常為一過性的,在繼續治療的過程中會消失。
少見不良反應(大於1/1,000,小於1/100)
脂肪代謝障礙:
注射部位可能會發生脂肪代謝障礙。通常是由於未在注射區域輪換注射點所致。
水腫:
胰島素治療的初期會出現水腫現象。這種現象通常為一過性的。
免疫系統失調
少見不良反應(大於1/1,000,小於1/100)
過敏反應,潛在的過敏反應,蕁麻疹,皮疹, 出疹。
這些症狀可能是由於全身性過敏反應所致。全身性過敏反應的其他症狀可能包括瘙癢、出汗、胃腸道不適、血管神經性水腫、呼吸困難、心悸與血壓下降。全身性過敏反應有可能危及生命(超敏反應)。
視覺異常
少見不良反應(大於1/1,000,小於1/100)
屈光不正:
胰島素治療的初始階段,可能會出現屈光不正。這種現象通常為一過性的。
糖尿病視網膜病變:
長期血糖水平控制良好可以降低糖尿病視網膜病變的風險。
然而因強化胰島素治療而突然改善血糖水平控制可能會發生糖尿病視網膜病的暫時惡化。
神經系統異常
罕見不良反應(大於1/10,000,小於1/1,000)
周圍神經系統病變:
快速改善血糖水平控制可能發生急性痛性神經病變,這種症狀通常是可逆的。
禁忌
以下患者禁用:
• 對地特胰島素或者本品中任何其他成份過敏者。
• 對地特胰島素或者本品中任何其他成份過敏者。
注意事項
本品注射劑量不足或治療中斷時,可能導致高血糖和糖尿病酮症酸中毒(特別是在1型糖尿病患者中易發生)。通常在幾小時到幾天內高血糖的首發症狀逐漸出現。症狀包括口渴、尿頻、噁心、嘔吐、嗜睡、皮膚乾紅、口乾、食欲不振和呼氣中有丙酮氣味。在1型糖尿病患者中,出現高血糖事件若不予以治療,最終可能導致有潛在致死性的糖尿病酮症酸中毒。
如果胰島素的用量遠高於胰島素的需要量時可能出現低血糖。漏餐或進行無計畫、高強度的體力活動, 可導致低血糖。
血糖控制有顯著改善的患者(如接受胰島素強化治療的患者),其低血糖的先兆症狀會有所改變,應提醒患者注意。對於病程長的糖尿病患者,常見的低血糖的先兆症狀可能會消失。
伴有其他疾病,特別是感染和發熱,通常患者的胰島素需要量會增加。
患者換用不同品牌或類型的胰島素製劑,必須在嚴格的醫療監控下進行。以下方面的變化均可能導致患者所需劑量改變:胰島素規格、品牌(生產商)、類型、種類(動物、人胰島素或人胰島素類似物)和/或生產工藝(基因重組或動物胰島素)。患者從其日常使用的胰島素轉用本品時,可能需要調整劑量。劑量調整可能在首次注射或開始治療的幾周或幾個月內進行。
和所有的胰島素治療一樣,使用本品可能會發生注射部位的反應,包括疼痛,瘙癢,蕁麻疹,腫脹和炎症。
在指定注射區域連續輪換注射點有助於減少或避免這些反應。這些反應通常在幾天或幾星期內消失。在罕見情況下,注射部位反應可能需要停止注射地特胰島素。
由於可能導致重度低血糖,本品絕不能靜脈注射。
與皮下注射相比較,肌肉注射吸收更快,吸收量更大。
如果本品與其他胰島素製劑混合使用,其中之一或者兩者的作用特性將會改變。與單獨注射相比較,本品與快速起效的胰島素類似物(如門冬胰島素)同時使用,其最大作用將會降低和延遲。
本品不能用於胰島素泵。
運動員慎用。
對駕駛和機械操作能力的影響
低血糖可能會降低患者的注意力和反應能力。在這些能力異常重要的情況下(如在駕駛汽車和操作機械的過程中),可能會存在風險。
應特別提醒患者注意避免在駕駛時出現低血糖,尤其是低血糖先兆症狀不明顯或缺乏或既往經常發生低血糖的患者。在上述情況下,應首先考慮患者能否安全操作。
如果胰島素的用量遠高於胰島素的需要量時可能出現低血糖。漏餐或進行無計畫、高強度的體力活動, 可導致低血糖。
血糖控制有顯著改善的患者(如接受胰島素強化治療的患者),其低血糖的先兆症狀會有所改變,應提醒患者注意。對於病程長的糖尿病患者,常見的低血糖的先兆症狀可能會消失。
伴有其他疾病,特別是感染和發熱,通常患者的胰島素需要量會增加。
患者換用不同品牌或類型的胰島素製劑,必須在嚴格的醫療監控下進行。以下方面的變化均可能導致患者所需劑量改變:胰島素規格、品牌(生產商)、類型、種類(動物、人胰島素或人胰島素類似物)和/或生產工藝(基因重組或動物胰島素)。患者從其日常使用的胰島素轉用本品時,可能需要調整劑量。劑量調整可能在首次注射或開始治療的幾周或幾個月內進行。
和所有的胰島素治療一樣,使用本品可能會發生注射部位的反應,包括疼痛,瘙癢,蕁麻疹,腫脹和炎症。
在指定注射區域連續輪換注射點有助於減少或避免這些反應。這些反應通常在幾天或幾星期內消失。在罕見情況下,注射部位反應可能需要停止注射地特胰島素。
由於可能導致重度低血糖,本品絕不能靜脈注射。
與皮下注射相比較,肌肉注射吸收更快,吸收量更大。
如果本品與其他胰島素製劑混合使用,其中之一或者兩者的作用特性將會改變。與單獨注射相比較,本品與快速起效的胰島素類似物(如門冬胰島素)同時使用,其最大作用將會降低和延遲。
本品不能用於胰島素泵。
運動員慎用。
對駕駛和機械操作能力的影響
低血糖可能會降低患者的注意力和反應能力。在這些能力異常重要的情況下(如在駕駛汽車和操作機械的過程中),可能會存在風險。
應特別提醒患者注意避免在駕駛時出現低血糖,尤其是低血糖先兆症狀不明顯或缺乏或既往經常發生低血糖的患者。在上述情況下,應首先考慮患者能否安全操作。
孕婦及哺乳期婦女用藥
本品尚無治療妊娠或哺乳期婦女的臨床經驗。
動物生殖研究表明:在胚胎毒性和æ畸性方面,本品與人胰島素沒有差異。
建議患有糖尿病的妊娠婦女在整個妊娠期間和計畫妊娠時採用強化血糖控制和監測的方式è療。胰島素的需要量通常在妊娠早期減少;而在隨後的妊娠中、晚期逐漸增加。分娩後胰島素的需要量通常迅速回到妊娠前的水平。哺乳期婦女可能需要調整胰島素用量和飲食。
動物生殖研究表明:在胚胎毒性和æ畸性方面,本品與人胰島素沒有差異。
建議患有糖尿病的妊娠婦女在整個妊娠期間和計畫妊娠時採用強化血糖控制和監測的方式è療。胰島素的需要量通常在妊娠早期減少;而在隨後的妊娠中、晚期逐漸增加。分娩後胰島素的需要量通常迅速回到妊娠前的水平。哺乳期婦女可能需要調整胰島素用量和飲食。
兒童用藥
本品尚未在6歲以下兒童中進行有效性和安全性的研究。曾在1型糖尿病兒童(6-12歲)和青少年(13-17歲)中進行了本品的藥代動力學研究,並與患有1型糖尿病的成人進行了比較。其藥代動力學在這些人群中沒有差別。
老年用藥
在老年受試者與青年受試者ã間,本品的藥代動力學沒有與臨床相關的差異。
藥物相互作用
已知有多種藥物會影響葡萄糖代謝。
可能會減少胰島素需要量的藥物:
口服降糖藥,單胺氧化酶抑制劑(MAOI),非選擇性β阻滯劑,血管緊張素轉換酶(ACE)抑制劑,水楊酸鹽和酒精。
可能會加胰島素需要量的藥物:
噻嗪類藥物、糖皮質激素、甲狀腺激素和β-擬交感神經藥、生長激素和達那唑。
β阻滯劑可能掩蓋低血糖症狀,並且延遲低血糖的恢復。
奧曲肽/蘭瑞肽可能既會增加也會減少胰島素的需要量。
酒精可以加劇和延長胰島素導致的低血糖。
配伍禁忌
本品中加入其他化學物質可能導致地特胰島素的降解(如含有巰基或亞硫酸鹽的藥物)。本品不能用於靜脈輸液。
可能會減少胰島素需要量的藥物:
口服降糖藥,單胺氧化酶抑制劑(MAOI),非選擇性β阻滯劑,血管緊張素轉換酶(ACE)抑制劑,水楊酸鹽和酒精。
可能會加胰島素需要量的藥物:
噻嗪類藥物、糖皮質激素、甲狀腺激素和β-擬交感神經藥、生長激素和達那唑。
β阻滯劑可能掩蓋低血糖症狀,並且延遲低血糖的恢復。
奧曲肽/蘭瑞肽可能既會增加也會減少胰島素的需要量。
酒精可以加劇和延長胰島素導致的低血糖。
配伍禁忌
本品中加入其他化學物質可能導致地特胰島素的降解(如含有巰基或亞硫酸鹽的藥物)。本品不能用於靜脈輸液。
藥物過量
長期臨床試驗表明,地特胰島素治療過程中空腹血糖日間變異性比人NPH胰島素低。
在2型糖尿病患者中進行的基礎胰島素聯合口服降糖藥治療的研究表明,地特胰島素對血糖的控制(HbA1c)與人NPH胰島素和甘精胰島素相當,且體重增加較少(見表1):
口服降糖藥與胰島素聯合治療的試驗結果顯示,地特胰島素治療較人NPH胰島素è療,輕度夜間低血糖的風險降低了61-65%。
在長期在治療試驗(≥6個月)中,本品作為基礎胰島素,較人NPH胰島素更好地改善1型糖尿病患者的空腹血糖,其中包括6-17歲的兒童和青少年。地特胰島素對血糖的控制(HbA1c)與人NPH胰島素相當,夜間低血糖的風險更低,且不會發生體重增加。與人NPH胰島素相比, 本品的夜間葡萄糖曲線更平坦、平穩,因此夜間低血糖的風險更低。地特胰島素使用過程中曾觀察到抗體的形成,但這並未影響血糖的控制。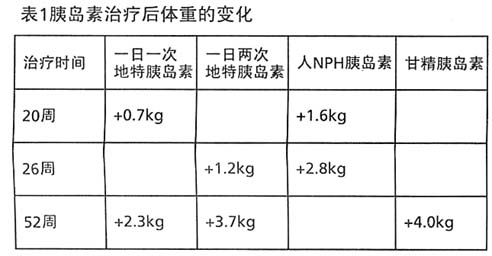
在2型糖尿病患者中進行的基礎胰島素聯合口服降糖藥治療的研究表明,地特胰島素對血糖的控制(HbA1c)與人NPH胰島素和甘精胰島素相當,且體重增加較少(見表1):
口服降糖藥與胰島素聯合治療的試驗結果顯示,地特胰島素治療較人NPH胰島素è療,輕度夜間低血糖的風險降低了61-65%。
在長期在治療試驗(≥6個月)中,本品作為基礎胰島素,較人NPH胰島素更好地改善1型糖尿病患者的空腹血糖,其中包括6-17歲的兒童和青少年。地特胰島素對血糖的控制(HbA1c)與人NPH胰島素相當,夜間低血糖的風險更低,且不會發生體重增加。與人NPH胰島素相比, 本品的夜間葡萄糖曲線更平坦、平穩,因此夜間低血糖的風險更低。地特胰島素使用過程中曾觀察到抗體的形成,但這並未影響血糖的控制。

藥理毒理
藥物治療組:抗糖尿病藥物。長效、注射用胰島素及其類似物,ATC代碼:A10AE05。
地特胰島素是可溶性的、長效基礎胰島素類似物,其作用平緩且作用持續時間長。
與人NPH胰島素和甘精胰島素(insulin glargine) 相比較,本品的時間作用曲線的變異性顯著降低。
本品的長效作用是通過在注射部位地特胰島素分子之間強大的自身聚合以及通過脂肪酸側鏈與白蛋白相結合而實現的。與人NPH胰島素相比,地特胰島素分子向外周靶組織的分布更為緩慢。這些延長機制的結合使本品的吸收和作用曲線比人NPH胰島素更易重複,即變異度小。
地特胰島素的降血糖作用是通過地特胰島素分子與肌肉和脂肪細胞上的胰島素受體結合後,促進細胞對葡萄糖的吸收利用,同時抑制肝å葡萄糖的輸出來實現的。
本品每日注射一次或者兩次,依劑量不同,最長作用持續時間可達24小時。如果每日注射兩次,則可以在注射2至3次後達到穩態。當劑量為0.2-0.4U/kg時,î射3-4小時後,效應已超過最大效應的50%,作用持續約為14小時。
本品皮下注射後,觀察到劑量與效應(最大效應、作用持續時間、總藥效)呈現比例關係。
臨床前安全性研究
人體細胞系體外試驗表明,地特胰島素與胰島素和胰島素樣生長因子-1(IGF-1) 兩種受體的親和力小於人胰島素,而且對細胞生長的影響也小於人胰島素。
安全性藥理學,多次給藥毒性,遺傳毒性,潛在致癌性和生物毒性等常規臨床前研究數據顯示,地特胰島素對人體沒有特殊危害。
地特胰島素是可溶性的、長效基礎胰島素類似物,其作用平緩且作用持續時間長。
與人NPH胰島素和甘精胰島素(insulin glargine) 相比較,本品的時間作用曲線的變異性顯著降低。
本品的長效作用是通過在注射部位地特胰島素分子之間強大的自身聚合以及通過脂肪酸側鏈與白蛋白相結合而實現的。與人NPH胰島素相比,地特胰島素分子向外周靶組織的分布更為緩慢。這些延長機制的結合使本品的吸收和作用曲線比人NPH胰島素更易重複,即變異度小。
地特胰島素的降血糖作用是通過地特胰島素分子與肌肉和脂肪細胞上的胰島素受體結合後,促進細胞對葡萄糖的吸收利用,同時抑制肝å葡萄糖的輸出來實現的。
本品每日注射一次或者兩次,依劑量不同,最長作用持續時間可達24小時。如果每日注射兩次,則可以在注射2至3次後達到穩態。當劑量為0.2-0.4U/kg時,î射3-4小時後,效應已超過最大效應的50%,作用持續約為14小時。
本品皮下注射後,觀察到劑量與效應(最大效應、作用持續時間、總藥效)呈現比例關係。
臨床前安全性研究
人體細胞系體外試驗表明,地特胰島素與胰島素和胰島素樣生長因子-1(IGF-1) 兩種受體的親和力小於人胰島素,而且對細胞生長的影響也小於人胰島素。
安全性藥理學,多次給藥毒性,遺傳毒性,潛在致癌性和生物毒性等常規臨床前研究數據顯示,地特胰島素對人體沒有特殊危害。
藥代動力學
吸收
本品注射後6-8小時達到最大血清濃度。當每日注射兩次時,注射2-3次後達到穩態血清濃度。本品吸收的個體內變異,要低於其他基礎胰島素製劑。本品的藥代動力學特點在不同性別之間沒有與臨床相關的差異。
分布
本品表觀分布容積(大約0.1L/kg),表明大部分地特胰島素分布在血液中。
代謝
本品的降解與人胰島素類似,所有形成的代謝物都是沒有活性的。體外和體內蛋白結合研究的結果表明,在本品與脂肪酸或者其他蛋白結合藥物ã間沒有臨床上的有關相互作用。
消除
地特胰島素皮下注射的終末半衰期是由皮下組織的吸收速率決定的。根據劑量的不同,終末半衰期在5-7小時之間。
線性
皮下注射後,觀察到本品劑量與血清濃度(最大濃度、吸收程度)成比例關係。在腎功能或者肝功能不全的受試者與健康受試者之間,本品的藥代動力學沒有與臨床相關的差異。
本品注射後6-8小時達到最大血清濃度。當每日注射兩次時,注射2-3次後達到穩態血清濃度。本品吸收的個體內變異,要低於其他基礎胰島素製劑。本品的藥代動力學特點在不同性別之間沒有與臨床相關的差異。
分布
本品表觀分布容積(大約0.1L/kg),表明大部分地特胰島素分布在血液中。
代謝
本品的降解與人胰島素類似,所有形成的代謝物都是沒有活性的。體外和體內蛋白結合研究的結果表明,在本品與脂肪酸或者其他蛋白結合藥物ã間沒有臨床上的有關相互作用。
消除
地特胰島素皮下注射的終末半衰期是由皮下組織的吸收速率決定的。根據劑量的不同,終末半衰期在5-7小時之間。
線性
皮下注射後,觀察到本品劑量與血清濃度(最大濃度、吸收程度)成比例關係。在腎功能或者肝功能不全的受試者與健康受試者之間,本品的藥代動力學沒有與臨床相關的差異。
貯藏
正在使用的本品不要放於冰櫃中。
正在使用的本品或者隨身攜帶的備用品可在室溫下(不超過30°C)存放6周。
尚未使用的本品應冷藏於2-8°C冰櫃中(勿接近冰櫃的冷凍室)。
不可冷凍。
筆芯保存在外包裝盒內以避光。
每次注射後必須卸下並丟棄針頭。否則,藥液可能會漏出,導致劑量不準確。
正在使用的本品或者隨身攜帶的備用品可在室溫下(不超過30°C)存放6周。
尚未使用的本品應冷藏於2-8°C冰櫃中(勿接近冰櫃的冷凍室)。
不可冷凍。
筆芯保存在外包裝盒內以避光。
每次注射後必須卸下並丟棄針頭。否則,藥液可能會漏出,導致劑量不準確。
包裝
筆芯由1型玻璃製成,內有一個活塞(溴丁基橡膠),並由橡膠膜(溴丁基橡膠/聚異戊二烯橡膠)密封。
每盒1支。
每盒1支。
有效期
24個月。
執行標準
進口藥品註冊標準:JS20050023
批准文號
進口藥品註冊證號:S20090064
分包裝批准文號:國藥準字J20090101
分包裝批准文號:國藥準字J20090101
生產企業
丹麥諾和諾德公司
核准日期
2009年6月26日
