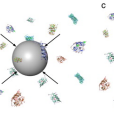
蛋白冠(protein corona)是指納米材料進入生物環境之後,如含血清培養基或血液等體液,其表面吸附的一層或多層蛋白所組成的結構(圖1)。儘管隨著研究的深入,科學家們發現納米材料在生物環境中所吸附的不僅僅是蛋白質分子,但仍然沿用“蛋白冠”這一術語來描述納米材料表面的這一層生物結構。
簡介,形成原理,組成,生物效應,研究意義,
簡介
蛋白冠最早在2007年由愛爾蘭都柏林大學KA Dawson等描述[2],他們發現納米顆粒與血清接觸後,納米顆粒表面可以吸附大量的蛋白質。蛋白冠的存在可以逆轉帶正電荷納米顆粒的電荷狀態,並且影響納米顆粒在生物環境中的分散。實際上,細胞所面對的不是簡單的納米材料本身,而是納米材料與蛋白冠構成的一個整體(圖2)。

圖2 蛋白冠的形成對納米材料生物效應的影響[3]。
形成原理
納米材料的相對比表面積大且具有很高的表面自由能,因此容易吸附蛋白和其它大分子。介導蛋白冠形成的驅動力主要包括金屬原子(貴金屬納米材料)與巰基之間的相互作用、靜電吸附作用和疏水相互作用等非共價相互作用。研究發現,蛋白冠的形成非常迅速,在引入培養基中的30秒內,納米材料表面即可以形成蛋白冠結構[4]。
組成
蛋白冠由許多種蛋白分子組成。通常可以利用蛋白組學的研究方法來鑑定蛋白冠的組成。將納米顆粒表面吸附的蛋白分離後,利用SDS-PAGE和質譜等方法可以鑑定蛋白冠中的蛋白組份和比例。根據與納米顆粒的結合強弱,蛋白冠可以分為恆定蛋白冠(hard corona)和動態蛋白冠(soft corona);其中恆定蛋白冠更貼近於納米顆粒表面,其蛋白組成相對比較穩定,不容易與環境中其它蛋白進行相互交換,而動態蛋白冠相對遠離納米顆粒表面,其蛋白組成變化較大,所組成的蛋白容易與生物環境中的其它蛋白或大分子進行交換和相互作用[5]。蛋白冠的蛋白組成也隨納米顆粒所處的環境而發生變化。當納米材料由血清環境進入細胞質後,其表面的蛋白組成會發生變化,但仍然可以部分保留血清環境中形成的蛋白冠成分,因此有科學家提出鑑定蛋白冠的組成可以推測納米材料進入細胞的定位過程[6]。
生物效應
利用螢光標記蛋白與納米材料形成的蛋白冠,科學家發現蛋白冠與納米材料一起經內吞途徑進入細胞。進入細胞後,蛋白冠在溶酶體內降解[7-8]。蛋白冠的存在可以有效介導細胞對納米材料的吞噬,並緩解正電性納米材料的急性細胞毒性[8]。蛋白冠中蛋白的糖基化修飾可以介導納米材料與細胞之間的相互作用,如影響細胞內吞和相關信號通路等[9]。蛋白冠的形成可以影響納米材料的特性,如蛋白冠的存在可以阻礙轉鐵蛋白修飾納米顆粒的靶向作用[10]。對納米材料進行修飾後,如利用聚乙二醇修飾納米材料,可以有效減少納米材料表面蛋白的吸附,保持納米材料的靶向性[11]。另外,納米材料本身可以誘導所吸附蛋白的結構發生變化,從而介導不同的生物效應[12] 。
研究意義
研究蛋白冠有助於深入理解納米材料在生物套用中發揮功能的過程和機理,從而通過調控蛋白冠來降低納米材料引起的負面作用及改善納米材料在生物醫藥套用中的功效。