艾恆(注射用奧沙利鉑),適應症為適用於經過氟尿嘧啶治療失敗後的結、直腸癌轉移的患者,可單獨或聯合氟尿嘧啶使用。
基本介紹
- 藥品名稱:艾恆?
- 藥品類型:處方藥、基本藥物、醫保工傷用藥
- 用途分類:細胞毒性藥物
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,核准日期,修訂日期,
成份
本品主要成份為奧沙利鉑。其化學名稱為:(1R-反式)-(1,-2環己二胺-N,N’)[草酸(2-)-O,O’]合鉑。
其結構式為:
分子式:C8H14N2O4Pt
分子量:397.29
其輔料為乳糖。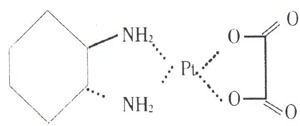
其結構式為:
分子式:C8H14N2O4Pt
分子量:397.29
其輔料為乳糖。

性狀
本品為白色或類白色疏鬆塊狀物或無定形固體或粉末。
適應症
適用於經過氟尿嘧啶治療失敗後的結、直腸癌轉移的患者,可單獨或聯合氟尿嘧啶使用。
規格
(1)50mg (2)0.1g
用法用量
在單獨或聯合用藥時,推薦劑量為按體表面積一次130mg/m[sup]2[/sup],加入250~500ml 5%葡萄糖溶液中輸注2~6小時。沒有主要毒性出現時,每3周(21天)給藥1次。劑量的調整應以安全性,尤其是神經學的安全性為依據。
不良反應
1.血液學方面的不良反應主要是:貧血、白細胞減少、粒細胞減少及血小板減少。
2.非血液學方面的不良反應主要是:噁心、嘔吐、腹瀉。
3.神經系統:以末梢神經為主要表現,有時可伴有口腔周圍、上呼吸道和上消化道的痙攣及感覺障礙。
2.非血液學方面的不良反應主要是:噁心、嘔吐、腹瀉。
3.神經系統:以末梢神經為主要表現,有時可伴有口腔周圍、上呼吸道和上消化道的痙攣及感覺障礙。
禁忌
1.對鉑類衍生物有過敏者禁用;
2.妊娠及哺乳期間慎用。
2.妊娠及哺乳期間慎用。
注意事項
1.奧沙利鉑應在具有抗癌化療經驗的醫師的監督下使用。特別是與具有潛在性神經毒性的藥物聯合用藥時,應嚴密監測奧沙利鉑神經學安全性。
2.應給予預防性或治療性的止吐用藥。
3.當出現血液毒性時(白細胞<2000/mm[sup]3[/sup]或血小板<50000/mm[sup]3[/sup]〉,應推遲下一周期用藥,直到恢復。
4.在每一療程之前應進行血液計數和分類,在每治療開始之前應進行神經學檢查,之後應定期進行。
5.患者在兩個療程之間持續存在疼痛性感覺異常或/和功能障礙時,本品用量應減少25%,調整劑量後若症狀仍存在或加重,應停藥。
6.不要與鹼性的藥物或介質、氯化合物、鹼性製劑等一起使用,也不要用含鋁的靜脈注射器具。
2.應給予預防性或治療性的止吐用藥。
3.當出現血液毒性時(白細胞<2000/mm[sup]3[/sup]或血小板<50000/mm[sup]3[/sup]〉,應推遲下一周期用藥,直到恢復。
4.在每一療程之前應進行血液計數和分類,在每治療開始之前應進行神經學檢查,之後應定期進行。
5.患者在兩個療程之間持續存在疼痛性感覺異常或/和功能障礙時,本品用量應減少25%,調整劑量後若症狀仍存在或加重,應停藥。
6.不要與鹼性的藥物或介質、氯化合物、鹼性製劑等一起使用,也不要用含鋁的靜脈注射器具。
孕婦及哺乳期婦女用藥
未進行該項試驗且無可靠參考文獻。
兒童用藥
未進行該項試驗且無可靠參考文獻。
老年用藥
未進行該項試驗且無可靠參考文獻。
藥物相互作用
未進行該項試驗且無可靠參考文獻。
藥物過量
未進行該項試驗且無可靠參考文獻。
藥理毒理
本品屬於新的鉑類衍生物,其中央鉑原子被-草酸和1,2-二氨環已烷包圍,呈反式構象,是一個立體異構體。象其他鉑類衍生物一樣,奧沙利鉑通過產生烷化結合物作用於DNA,形成鏈內和鏈間交聯,從而抑制DNA的合成及複製。奧沙利鉑與DNA結合迅速,最多需15分鐘,而順鉑與DNA結合分為兩個時相,其中包括一個48小時後的延遲相。在人體內給藥一小時之後,通過測定白細胞內的加合物,可顯示其存在。複製過程中的DNA合成,其後NDA的分離、RNA及細胞蛋白質的合成均被抑制。某些對順鉑耐藥的細胞系,奧沙利鉑治療均有效。
藥代動力學
以130mg/m[sup]2[/sup]的劑量連續滴注2小時,其血漿總鉑達峰值5.1±0.8mg/ml/h,模擬的曲線下面積為189±45mg/ml/h。
當輸液結束時,50%的鉑與紅細胞結合,而另外50%存在於血漿中。25%的血漿鉑呈游離態,另外75%血漿鉑與蛋白質結合。蛋白質結合鉑逐步升高,於給藥第五天后穩定於95%的水平。藥物的清除分為兩個時相,其清除相半衰期約為40小時。多達50%的藥物在給藥48小時之內由尿排出(55%的藥物在6天之後清除)。由糞便排出的藥量有限(給藥11天后僅有5%經糞便排出)。
在腎功能衰竭的病人中,僅有可過濾性鉑的清除減少,而並不伴有毒性的增加,因此並不需要調整用藥劑量。
與紅細胞結合的鉑清除很慢。在給藥後的第22天,紅細胞結合鉑的水平為血漿峰值的50%,而此時大多數的總血漿鉑已被清除。在以後的用藥周期中,總的或不被離心的血漿鉑水平並無顯著升高;而紅細胞結合鉑出現明顯的早期累積現象。
當輸液結束時,50%的鉑與紅細胞結合,而另外50%存在於血漿中。25%的血漿鉑呈游離態,另外75%血漿鉑與蛋白質結合。蛋白質結合鉑逐步升高,於給藥第五天后穩定於95%的水平。藥物的清除分為兩個時相,其清除相半衰期約為40小時。多達50%的藥物在給藥48小時之內由尿排出(55%的藥物在6天之後清除)。由糞便排出的藥量有限(給藥11天后僅有5%經糞便排出)。
在腎功能衰竭的病人中,僅有可過濾性鉑的清除減少,而並不伴有毒性的增加,因此並不需要調整用藥劑量。
與紅細胞結合的鉑清除很慢。在給藥後的第22天,紅細胞結合鉑的水平為血漿峰值的50%,而此時大多數的總血漿鉑已被清除。在以後的用藥周期中,總的或不被離心的血漿鉑水平並無顯著升高;而紅細胞結合鉑出現明顯的早期累積現象。
貯藏
密閉,在25℃以下保存。
包裝
西林瓶,1/瓶/盒。
有效期
(1) 50mg 24個月 (2)0.1g 暫定24個月。
執行標準
(1) 50mg YBH04792011
(2) 0.1g YBH08102004
(2) 0.1g YBH08102004
批准文號
(1)50mg 國藥準字H20000337
(2)0.1g 國藥準字H20040817
(2)0.1g 國藥準字H20040817
生產企業
江蘇恆瑞醫藥股份有限公司
核准日期
2007年01月05日
修訂日期
2007年11月27日 2011年12月16日 2012年03月16日
