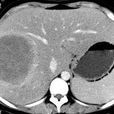
肝糖原累積症(glycogenstoragedisease,GSD) 為一組較少見的嬰幼兒先天性隱形遺傳性糖原代謝紊亂性疾病,同胞子女發生率明顯增加。肝糖原累積症是糖原累積症較常見的類型。多數由於糖原代謝酶的缺陷而導致糖原分解或合成障礙,從而產生不同組織器官中糖原或異型糖原的過多累積,主要受累的器官有肝、腎、肌肉、腦和小腸等。由於不同酶缺陷而分為1-6型。肝糖原累積症是糖原累積症最常見的類型,是因肝內葡萄糖-6-磷酸酶缺乏所致。
基本介紹
- 中文名:肝糖原累積症
- 外文名:glycogen storage disease,GSD
- 科室:肝病科
病因和發病機制,病理,臨床發現,診斷,治療,預後,產前診斷,
病因和發病機制
葡糖-6-磷酸酶是所有參與糖代謝途徑的酶中惟一存在於細胞微粒體(內質網)內的酶,其編碼基因(G6PT)位於第17號染色體。葡糖6-磷酸酶系統由以下成分組成:①分子量為36.ku的多肽,是酶的活性單位;②分子量為21ku的具保護酶活性的“穩定蛋白”,sp;③使6-磷酸葡萄糖進入內質網腔的轉運蛋白,T1;④使磷酸鹽通過內質網膜的轉運蛋白T2β;⑤使葡萄糖釋出內質網的轉運蛋白,GLUT7。由遺傳導致的上述系統任一組分的缺陷即可使酶系統活力受損、造成Ⅰ型糖原累積病,依次定名為la、IaSPIb、Ic和Id型。I型糖原累積病是由於肝、腎等組織中葡糖-6-磷酸酶系統活力缺陷所造成,是糖原累積病中最為多見者,約占總數的25%,本節以敘述其中常見的Ia型為主。
在正常人體中,由糖原分解或糖原異生過程所產生的6-磷酸葡萄糖和必須經葡糖-6-磷酸酶系統水解以獲得所需的葡萄糖,該酶系統可提供由肝糖原分解所得的90%葡萄糖,在維持血糖穩定方面起主導作用。當酶缺乏時,機體僅能獲得由脫枝酶分解糖原1,6糖苷鍵所產主的少量葡萄糖分子(約8%),所以必然造成嚴重空腹低血糖。正常人在血糖過低時.其胰高糖素分泌隨即增高以促進肝糖原分解和葡糖異生過程、生成葡萄糖使血糖保持穩定。Ⅰ型GSD患兒則由於葡糖-6-磷酸酶系統的缺陷,6-磷酸葡萄糖不能進一步水解成葡萄糖,因此由低血糖刺激分泌的胰高糖素不僅不能提高血糖濃度,卻使大量糖原分解所產生的部分6-磷酸葡萄糖進入糖酵解途徑;同時,由於6-磷酸葡萄糖的累積,大部分1-磷酸葡萄糖又重新再合成糖原;而低血糖又不斷導致組織蛋白分解,向肝臟輸送萄糖異生原料。這些異常代謝都加速了肝糖原的合成。糖代謝異常同時還造成了脂肪代謝紊亂,亢進的葡糖異生和糖酵解過程不僅使血中丙酮酸和乳酸含量增高導致酸中毒,還生成了大量乙醯輔酶A,為脂肪酸和膽固醇的合成提供了原料;同時還產生了合成脂肪的和膽固醇所必需的還原型輔酶Ⅰ(煙醯胺腺瞟吟二核苷酸,NADH)和還原型輔酶Ⅱ(煙醯胺腺瞟吟二核苷酸磷酸,NADPH);此外,低血糖還使胰島素水平降低,促進外周脂肪組織分解,使游離脂肪酸水平增高。這些代謝改變最終造成了三酸甘油脂和膽固醇等脂質合成旺盛,臨床表現為高脂血症和肝脂肪變性。
Ⅰ型GSD 常伴有高尿酸血症,這是由於患兒嘌呤合成代謝亢進所致:6-磷酸葡萄糖的累積促進了戊糖旁路代謝、生成過量的5-磷酸核糖,進而合成磷酸核糖焦磷酸。再在谷氨醯胺磷酸核糖焦磷酸氨基轉移酶的作用下轉化成為1-氨基-5-磷酸核糖苷,從而促進嘌呤代謝並使其終末代謝產物尿酸增加。
病理
肝細胞染色較淺,漿膜明顯,因胞漿內充滿糖原而腫脹且含有中等或大的脂肪滴,其細胞核亦因富含糖原而特別增大。細胞核內糖原累積、肝脂肪變性明顯但無纖維化改變是本型突出的病理變化,有別於其他各型糖原累積病。
臨床發現
臨床表現輕重不一:重症在新生兒期即可出現嚴重低血糖、酸中毒、呼吸困難和肝腫大等症狀;輕症病例則常在嬰幼兒期因生長遲緩、腹部膨脹等就診。由於慢性乳酸酸中毒和長期胰島素/胰高糖素例失常,患兒身材明顯矮小,骨齡落後,骨質疏鬆。腹部因肝持續增大而膨隆顯著。肌肉鬆弛,四肢伸側皮下常有黃色瘤可見。但身體各部比例和智慧型等都正常。患兒時有低血糖發作和腹瀉發生。少數幼嬰在重症低血糖時尚可伴發驚厥.但亦有血糖降至0.56mmol/L(10mg/dl)以下而無明顯症狀者。隨著年齡的增長,低血糖發作次數可減少。由於血小板功能不良,患兒常有流鼻血等出血傾向。
診斷
病史、體徵和血生化檢測可供作出初步臨床診斷。糖代謝功能試驗可能有助診斷:如糖耐量試驗中因患兒胰島素分泌不足,呈現典型糖尿病特徵;胰高糖素素或腎上腺素試驗亦不能使患兒血糖明顯上升,且注射胰高糖素後,血乳酸明顯增高;由於患兒不能使半乳糖或果糖轉化為葡萄糖,因此在半乳糖或果糧耐量試驗中血葡萄糖水平不升高。這類功能試驗雖有避免作肝組織活體檢查的優點,但由於本病患兒對此類試驗反應的個體變異較大,故仍應以肝組織的糖原定量和葡萄糖-6-磷酸酶活性測定作為確診依據。
治療
本病的病理生理基礎是在空腹低血糖時,由於胰高糖素的代償分泌促進了肝糖原分解,導致了患兒體內6-磷酸葡萄糖累積和由此生成過量的乳酸、三酸甘油酯和膽固醇等一系列病理生化過程。因此,從理論上講,任何可以保持正常血糖水平的方法即可阻斷這種異常的生化過程,減輕臨床症狀。
Folkman等在1972年首次證實全靜脈營養(TPN)療法可以糾正本病的異常生化改變和改善臨床症狀。嗣後,臨床即廣泛使用日間多次少量進食和夜間使用鼻飼管持續點滴高碳水化合物液的治療方案,以維持血糖水平在4~5mmol/L。這種治療方法不僅可以消除臨床症狀,並且還可使患兒獲得正常的生長發育。為避兔長期鼻飼的困難,也可用每4~6小時口服生玉米澱粉 2g/kg混懸液的替代方法,效果同樣良好。
預後
未經正確治療的本病患兒因低血糖和酸中毒發作頻繁常有體格和智慧型發育障礙。伴有高尿酸血症患者常在青春期並發痛風。患者在成年期的心血管疾病、胰腺炎和肝臟腺瘤(或腺癌)的發生率高於正常人群,少數患者可並發進行性腎小球硬化症。
自從套用上述飲食療法以來,已有不少患兒在長期治療後獲得正常生長發育,即使在成年後停止治療亦不再發生低血糖等症狀,但更長期的追蹤隨訪仍屬必要。
產前診斷
可通過胎兒肝活檢測定葡糖-6-磷酸酶活力進行,通常在孕18~22周進行。