播散性血管內凝血(disseminated intravascular coagulation,DIC)不是一個獨立的疾病,而是許多疾病發展過程中的一個重要的中間過程,其特徵為血管內凝血被激活,微循環血栓形成,大量消耗凝血因子和血小板,導致繼發性纖溶酶大量生成,臨床出現出血、臟器功能障礙、微血管病性溶血及休克等症狀。
簡介
發病原因
儘管有許多疾病可並發DIC,但臨床最常見於產科合併症、全身重度感染、嚴重創傷、轉移性腫瘤等。
發病機制
 老年播散性血管內凝血
老年播散性血管內凝血治療
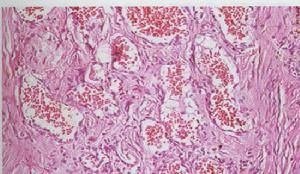 老年播散性血管內凝血
老年播散性血管內凝血2.改善微循環擴容,吸氧,糾正酸中毒,給予血管擴張劑等等。
3.抗凝治療適時套用抗凝,減輕器官損傷並改善其功能,特別是在病因持續存在的情況下。
(1)肝素:臨床多套用肝素鈉,其作用機制是增強AT-Ⅲ的抗凝活性,故給藥的前提條件是體內有足夠的AT-Ⅲ。用藥時應結合補充凝血因子。
劑量:按每公斤體重5~10U/h靜脈滴注,如治療後APTT縮短,FDP和D-二聚體水平下降,纖維蛋白原上升,說明抗凝有效;如上述指標無改善,需加大肝素用量,直至出現滿意效果;如套用後APTT反而延長,應減少肝素用量。肝素治療應持續至原發病清除或得到控制。
肝素鈣抑制凝血酶的作用弱而抑制Ⅹa的作用較強。注入體內後不與內皮細胞膜結合,皮下注射後生物利用度較高。LMWH能促使內皮細胞釋放TFPI,對AT-Ⅲ的依賴性較小,出血的副作用較少,半衰期長,一般不需檢測。但本藥排泄主要通過腎,腎功能不全患者藥物清除半衰期延長,故需謹慎套用,腎衰患者套用劑量可酌減至正常的1/3。LMWH(速必凝)正常劑量0.3~0.5ml,皮下注射,2次/d。
禁忌證:①DIC晚期,明顯纖溶亢進;②活動性出血,如潰瘍病出血,肺結核空洞咯血;③有出血傾向的嚴重肝病或高血壓腦病;④手術後或創面未經良好止血者。
肝素套用時的檢測:普通肝素套用時凝血時間(CT,試管法)不應超過30min;控制APTT不超過60~100s。肝素過量可用硫酸魚精蛋白(魚精蛋白)拮抗,一般可按1∶1用藥,每次不宜超過50mg。1mg硫酸魚精蛋白(魚精蛋白)中和肝素100U。
(2)低分子右旋糖酐500~1000ml/d,可解除紅細胞和血小板聚集,並可疏通微循環,擴充血容量,用於早期DIC及輕症患者。
(3)AT-Ⅲ:可加強肝素的抗凝效果,文獻報導可按AT-Ⅲ30U/(kg·d),1~2次/d用藥,連用數天。
4.補充凝血因子及血小板由於凝血因子和血小板消耗性減少導致機體廣泛出血,故輸注凝血因子和血小板,同時套用肝素是安全的。目前多用成分輸血,常用的有:
(1)新鮮冰凍血漿(FFP):含有豐富的凝血因子。
(2)血小板濃縮液:血小板計數低於20×109/L,或有顱內出血傾向時應及時補充血小板。
(3)凍乾人纖維蛋白原(纖維蛋白原):可每次2~4g,因半衰期長,可每2~3天輸1次,達到正常水平即可停用。但有人主張不用,因為DIC時是多個凝血因子缺乏,只給凍乾人纖維蛋白原(纖維蛋白原)不但不能止血,反而影響病理觀察。
5.纖溶抑制劑只可用於纖溶亢進期,如氨甲環酸(止血環酸)100~200mg,2~3次/d,靜脈輸注。
6.抗血小板藥物DIC時均有血小板凝集活化,使用肝素時聯合套用抗血小板藥有利於阻斷DIC的進展。常用的藥物有噻氯匹定250mg,2次/d。
7.腎上腺皮質激素DIC時無常規套用指征,應視原發病情況而定。對各種變態反應性疾病或合併有腎上腺皮質功能不全者可套用。
