糠酸莫米松鼻噴霧劑,處方藥,由默沙東公司(在美國和加拿大被稱為默克)研發、生產。
糠酸莫米松鼻噴霧劑適用於預防和治療成人、青少年和3至11歲兒童季節性或常年性鼻炎。其起效迅速,顯著改善各種鼻部症狀以及眼部症狀。且是無味劑型,對鼻黏膜刺激更小,病人依從性良好。
在2008及2010年的“過敏性鼻炎及其對哮喘的影響”(Allergic Rhinitis and its Impact on Asthma,ARIA)指南中均被強烈推薦:鼻用糖皮質激素是治療變應性鼻炎的一線用藥。尤其在ARIA2010年修訂版中明確指出:除糠酸莫米松外,沒有其它鼻用激素與安慰劑療效對比的系統回顧。
基本介紹
- 中文名:糠酸莫米松鼻噴霧劑
- 外文名:Mometasone Furoate Aqueous Nasal Spray
- 主要成分:糠酸莫米松
- 有效期:24個月
藥品信息,基本信息,適應症,用法用量,不良反應,禁忌,注意事項,藥物相互作用,藥物過量,藥理毒理,藥代動力學,鼻用糖皮質激素治療機制,大事記,指南推薦,
藥品信息
基本信息
【中文商品名】內舒拿®/NASONEX®
【通用名稱】糠酸莫米松鼻噴霧劑
【英文名稱】Mometasone Furoate Aqueous Nasal Spray
【漢語拼音】kang suan mo mi song bi pen wu ji
【主要成分】糠酸莫米松
【規格】
(1)每瓶60撳,每撳含糠酸莫米松50μg,藥物濃度為0.05%(g/g)
(2)每瓶140撳,每撳含糠酸莫米松50μg,藥物濃度為0.05%(g/g)
【貯藏】在2℃至25℃保存。
【包裝】本品包裝於高密度聚乙烯瓶中。1瓶/盒。
【有效期】24個月
【執行標準】進口藥品註冊標準JX20080020
【批准文號】進口藥品註冊證號:H20130182
【生產企業】
公司名稱:MSD Belgium BVBA/SPRL
地址:Clos du Lynx, 5, 1200 Brussels, Belgium
生產廠名稱:Schering-Plough Labo N.V.
地址:Industriepark 30, 2220 Heist-op-den-Berg,Belgium
【主要成分】糠酸莫米松
化學名稱:9α,21-二氯-11β,17-羥基-16α-甲基孕甾-1,4-二烯-3,20-_二酮17-(2-糠酸酯)
分子式:C27H30Cl2O6
分子量:521.43
化學結構式:

【性狀】糠酸莫米松鼻噴霧劑是一種定量手撳式噴霧裝置,內容物為白色至類白色混懸劑。
適應症
本品適用於治療成人、青少年和3至11歲兒童季節性或常年性鼻炎,對於曾有中至重度季節性過敏性鼻炎症狀的患者,主張在花粉季節開始前2-4周用本品作預防性治療。
用法用量
季節過敏性或常年性鼻炎
通常先手撳噴霧器6~7次作為啟動,直至看到均勻的噴霧,然後鼻腔給藥,每撳噴出糠酸莫米松混懸液約100μg,內含糠酸莫米松一水合物,相當於糠酸莫米松50μg,如果噴霧器停用14日或14日以上,則在下一次套用時應重新啟動。
在每次用藥前充分振搖容器。
成人(包括老年患者)和青年:用於預防和治療的常用推薦量為每側鼻孔2撳(每撳為50μg),一日1次(總量為200μg),一旦症狀被控制後,劑量可減至每側鼻孔1撳(總量100μg),即能維持療效。
如果症狀未被有效控制,可增加劑量至每側鼻孔4撳的最大每日劑量,一日1次(總量400μg),在症狀控制後減小劑量。
在首次給藥後12小時即能產生明顯的臨床效果。
3至11歲兒童:常用推薦量為每側鼻孔1撳(每撳為50μg),一日1次(總量為100μg)。
不良反應
季節過敏性或常年性鼻炎
在臨床研究中報導與本品有關的局部不良反應(成人及青少年患者)包括頭疼(8%),鼻出血如明顯出血、帶血粘液和血斑(8%),咽炎(4%),鼻灼熱感(2%),鼻部刺激感(2%)及鼻潰瘍(1%),這些不良反應常見於使用糖皮質激素類鼻噴霧劑時。鼻出血一般具有自限性,同時程度較輕,與安慰劑(5%)相比發生率較高,但與陽性對照的鼻腔用糖皮質激素(15%)相比發生率接近或較低,其他反應均與安慰劑相當。
在小兒患者中,不良反應如頭疼(3%),鼻出血(6%),鼻部刺激感(2%)及流涕(2%)的發生率均與安慰劑相當。
鼻腔吸入糠酸莫米松一水合物很少發生即刻過敏反應,極少有過敏反應和血管性水腫的報導。
罕有味覺及嗅覺干擾的報導。
禁忌
對本品中任何成份(活性成份:糠酸莫米松一水合物;非活性成份:纖維素、甘油、檸檬酸鈉二水合物、檸檬酸水化物、聚山梨醇酯80、苯扎氯銨、純水)過敏者禁用。
注意事項
禁止刺穿噴嘴。
鼻噴霧器的清潔:常規清潔鼻噴霧劑非常重要,否則將影響鼻噴霧劑的正常工作。清潔時,取下防塵帽,輕輕取下噴嘴,在溫水中清洗噴嘴和防塵帽,然後在流動的水流下沖洗。禁止插入針或其他尖銳的器具刺穿噴嘴,此操作會損壞噴嘴,導致無法釋放正確劑量的藥物。清洗後可將本品放置於溫暖的空間乾燥,將噴嘴還原與瓶身相連,並蓋上防塵帽。清洗後首次使用時需手撳噴霧劑2次以重新啟動。
對於涉及鼻黏膜的未經治療的局部感染,不應使用本品。
由於糖皮質激素具有抑制傷口癒合的作用,因而對於新近接受鼻部於術或受外傷的患者,在傷口癒合前不應使用鼻腔用糖皮質激素。
使用本品治療12個月後未見鼻黏膜萎縮,同時糠酸莫米松可使鼻黏膜恢復至正常組織學表現。與仟何一種藥物長期使用時一樣,對於使用本品達數月或更長時間的患者,應定期檢查鼻黏膜,如果鼻咽部發生局部真菌感染,則應停用本品或需給予適當治療,持續存在鼻咽部刺激可能是停用本品的一項指征。
對於活動性或靜止性呼吸道結核感染、未經治療的真菌、細菌、全身性病毒感染或眼單純皰疹的患者慎用本品。
長期使用本品後未見下丘腦-垂體-腎上腺(HPA)軸受到抑制,但對於原先長期使用全身作用糖皮質激素而換用本品的患者,需加仔細注意。這些患者可因停止全身用糖皮質激素而造成腎卜腺功能不全,需經數月後HPA軸功能才得以恢復。如果這些患者出現腎上腺功能不全的症狀和體徵時,應恢復全身套用糖皮質激素,並給予其他治療和採取適宜措施。
在安慰劑對照臨床試驗中,小兒患者使用本品每日100μg長達一年,末發現其減慢生長發育速度。
在全身用糖皮質激素換用本品時,某些患者儘管鼻部症狀有所緩解,但可發生全身用藥時糖皮質激素的停藥症狀如最初的關節和(或)肌肉痛、乏力及抑鬱,這時需鼓勵患者繼續使用本品治療。此外全身用激素轉為鼻腔局部套用時亦可暴露出原先存在的過敏性疾病,如過敏性結膜炎和濕疹,這些病症在全身用藥時受到抑制。
接受糖皮質激素治療的患者,免疫功能可能受到抑制,故應警惕面臨某些感染(如水痘、麻疹)的危險,如果發生這種情況,得到醫生指導是重要的。
在鼻腔內氣霧吸入糖皮質激素後,罕有報導鼻中隔穿孔或眼內壓升高的病例。
孕婦和哺乳期婦女用藥
對於孕婦尚未進行足夠或良好的對照研究。
如同其他鼻腔用糖皮質激素製劑,對於孕婦、乳母或育齡婦女,只有在用藥後對母體、胎兒或嬰兒的益處超過可能產牛的危害時才可使用本品。對母親在孕期接受糖皮質激素診治的嬰兒需注意觀察是否存在腎上腺功能減退。
兒童用藥
臨床對照研究表明鼻腔用糖皮質激素可能導致兒童患者生長速度減慢。在缺乏下丘腦-垂體-腎上腺(HPA)軸抑制實驗室證據的情況下,觀察到的此種現象提示,對於兒童患者全身糖皮質激素暴露,與通常所採用的HPA軸功能測試相比,增長速度是更敏感的指示劑。這種與鼻腔用糖皮質激素相關的生長速度減慢的長期影響(包括對成年後身高的影響)還是未知的。停止鼻腔用糖皮質激素治療後對生長的潛在影響還未進行充分的研究。對接受鼻腔用糖皮質激素的兒童患者(包括本品50μg)應進行例行檢測(如身高檢查)。延長治療對生長的潛在影回響與獲得的臨床益處和可替代的非糖皮質激素治療的安全性和有效性相衡量。為減少鼻腔用糖皮質激素給藥(包括本品50μg)的全身影響,應測定每位患者的最低有效量。
在臨床對照研究中,720名3至11歲的過敏性鼻炎患者使用本品50μg治療(100μg/天給藥)。在另一項臨床對照研究中,對28名2至5歲的過敏性鼻炎患者使用本品50μg治療(100μg /天給藥)以評價安全性。小於2歲的過敏性鼻炎患者的安全性與有效性還沒有建立。
一項對過敏性鼻炎兒童患者(3至9歲)進行的為期一年的臨床研究評價本品50μg(100μg/天)用藥對增長速度的影響。與安慰劑相比,沒有觀察到本品50μg對增長速度有顯著的影響。30分鐘替可克肽(Cosyntropin)灌輸後,未觀察到與HPA軸抑制相關的臨床跡象。
本品50μg或更高劑量對免疫缺乏患者的生長抑制的潛在影響未被排除。
老年用藥
老年患者:總計203名64歲以上(64到86歲)患者接受本品治療,50μg共3個月。此人群中被報導的不良反應在類型和影響範圍上與年輕患者群中報導的不良反應類似。
藥物相互作用
本品與氯雷他定合用,對氯雷他定及其主要代謝物的血漿濃度未見明顯影響。試驗採用定量限(LLOQ)為50 pg/ml的試驗方法未能檢出糠酸莫米松的血漿濃度,兩藥合用的耐受情況良好。
藥物過量
由於本品的全身生物利用度<1%(採用定量限為0.25 pg/ml的敏感分析方法),因而發生藥物過量時除觀察外不需任何治療,以後可重新使用適宜劑量的藥物。
吸入或口服過量的糖皮質激素對下丘腦垂體腎上腺軸的功能有抑制作用。
藥理毒理
糠酸莫米松是一種局部用糖皮質激素,發揮局部抗炎作用的劑量並不引起全身作用。
藥代動力學
吸收:
鼻噴霧單獨給藥後,儘管使用了較低定量檢測限(LOQ)(50pcg/mL)的靈敏分析方法,在成人及兒童受試者血漿中均未檢測出糠酸莫米松。
分布:
糠酸莫米松5~500nl/mL濃度範圍內,體外蛋白結合率為98%~99%。
代謝:
研究表明糠酸莫米松經鼻部吸收及吞咽的所有藥物經歷強代謝後代謝為多種代謝物。在血漿中未檢測出主要代謝物,在體外培養中,次要代謝物之一為6β-羥基-糠酸鹽。在人肝微粒體中,本品的代謝物受細胞色素P-450 3A4 (CYP3A4)的影響。
清除:
靜脈給藥後,糠酸莫米松有效血漿清除半衰期是5.8小時。吸收的藥物大部分作為代謝物通過膽汁排泄,少數通過尿液排泄。
特殊人群
對糠酸莫米松在腎損、肝損患者及不同年齡和不同性別患者中的藥代動力學,還未進行充分研究。
鼻用糖皮質激素治療機制
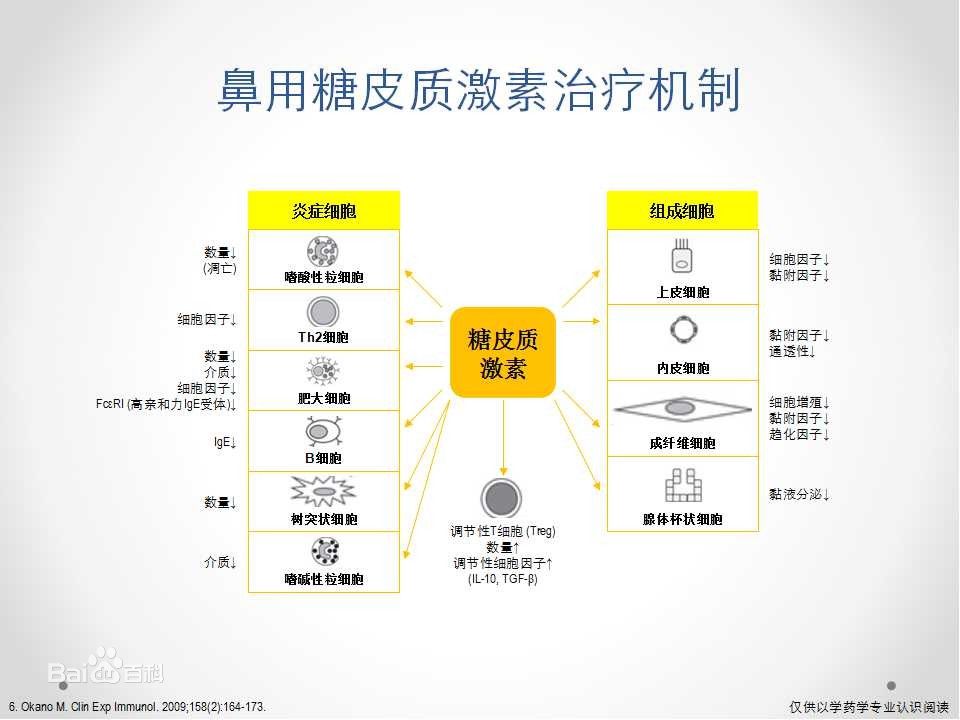
大事記
1997年10月1日,美國FDA批准內舒拿上市。
2004年8月26日,先靈葆雅公司宣布,美國FDA已經批准50Mcg糠酸莫米松一水化物(mometasone furoate monohydrate,NASONEX)產品的無味新劑型。還是唯一一個獲準用於治療2歲過敏性鼻炎患者的固醇類鼻吸入劑。
2004年11月和12月,歐盟和美國藥監部門分別批准了內舒拿(Nasonex)用於治療鼻息肉。
2006年12月6日,加拿大衛生部批准其糠酸莫米松內舒拿用於治療18歲及其以上、包括老年患者的鼻息肉,從而為他們提供了一種有效的替代手術的治療手段。
指南推薦
2008ARIA指南推薦:鼻用糖皮質激素用於治療變應性鼻炎

ARIA Guideline: 2010年修訂版

