粘土礦物主要是指那些粒級為粘土級的層狀含水鋁矽酸鹽礦物。粘土礦有兩個明顯的特點:一是這類礦物的晶體都很細小,從而具有較大的比表面能;二是它們的晶體結構是層狀的,並都含有“水”。粘土礦物的一切性質幾乎都與這兩個特點有關。在粘土礦物的所有性質中,最引人注目的是它的膨潤性(或膨脹性),吸附離子的可交換性,催化性和可塑性等。
基本介紹
- 中文名:粘土礦物性質
- 外文名:clay mineral property
- 學科:工程地質學
- 主要組成:含鋁、鎂等為主的含水矽酸鹽礦物
- 特點:晶體都很細小、較大的比表面能
- 性能:潤濕性
結構特徵,礦物類型,膨潤性,吸附離子的可交換性,
結構特徵
地層中粘土礦物由很小的結晶顆粒組成,根據晶體結構可以分成幾組粘土礦物。對石油工業有重要意義的粘土礦物主要有高嶺石、蒙脫石、伊利石、綠泥石以及這些礦物組成的混層礦物,這些礦物屬於含水層狀矽酸鹽,其主要構造單元為二維排列的矽氧四面體和二維排列的鋁或鎂-氧-氫八面體。在粘土礦物的結構單元層中,矽氧四面體中的Si4+可能被Al3+取代,八面體中的Al3+可能被Mg2+、Fe2+取代,此時結構單元層中就出現了負電荷,為平衡多餘的層電荷,必然出現層間陽離子。粘土礦物的層間陽離子有“固定的”和“可交換的”的兩種類型。
礦物類型
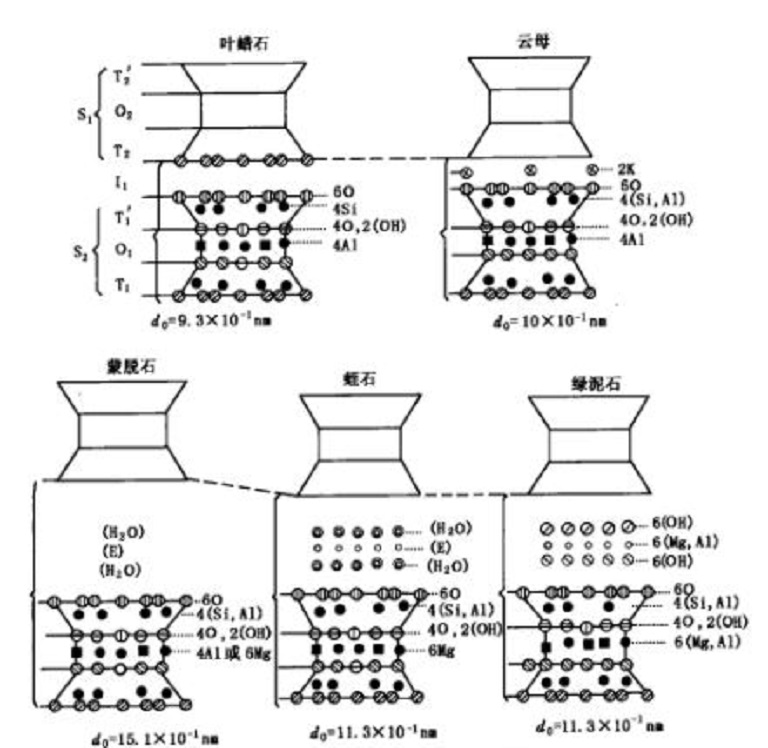
高嶺石屬1:1型二八面體層狀矽酸鹽,晶層問通過范德華力和氫鍵聯結,晶層間聯結緊密,無層間物質,晶層間距小,這類粘土礦物水化膨脹能力差。伊利石組粘土礦物的基本結構單元由兩個矽氧四面體層與夾在它們之間的八面體組成。同晶置換主要發生在四面體中,由此產生的負電荷被層間K+平衡。層間K+對晶層起固著作用,與溶液中陽離子交換很難,只有外表稜角上的K+易同其他陽離子交換,但交換能力低,遇水後晶層間膨脹小。綠泥石在結構上與2:1型層狀粘土相似,不同的是層間陽離子被一層八面體氫氧化物片替代,並且這個八面體片的正電荷與晶層負電荷相平衡,在2:1型晶層與氫氧化物片之間除靜電引力外,還有氫氧鍵聯結,晶層間結合緊密,遇水後水化膨脹能力弱。
蒙脫石的基本結構單元與伊利石相似,屬2:1型,其差異在於蒙脫石層間電荷比伊利石少,層間陽離子不是K+,而是Ca+,Mg2+、Na+等交換性陽離子。交換性陽離子與晶層通過靜電引力聯結,聯結弱,易被置換,水和其他極性分子能夠滲入結構單位層之間,並引起晶格沿縱軸方向膨脹。特別是Na+為其主要吸附的陽離子時,吸水後有較高的水化膨脹性能,其晶層軸間距可達40A。。
膨潤性
粘土礦物因吸水(溶液)而體積增大的現象,即稱為粘土礦物的膨潤性。粘土礦物的膨潤性有內部膨潤和外部膨潤兩種。在追加水分的條件下,水被粘土礦物吸入結構單位層之間,在水分子沿層面層層展鋪疊置的同時,瞬間與粘土礦物形成平行連晶,從而使原層間距(d)擴大,此即為內部膨潤;發生在粘土礦物晶粒間的膨大,是為外部膨潤。
吸附離子的可交換性
膠體質點的性質相似,粘土礦物的顆粒表面也是帶電的,其帶電原因為:
(1)因粘土礦物顆粒表面有未中和的酸基或鹼基而帶電,其所荷電性,視酸基或鹼基而定;
(2)因結構單位層中的高價離子被低價離子類質同象代替而帶電,其電性為負;
(3)因結構單位層邊緣上出現的破鍵而帶電,其電性視介質的pH值而定。