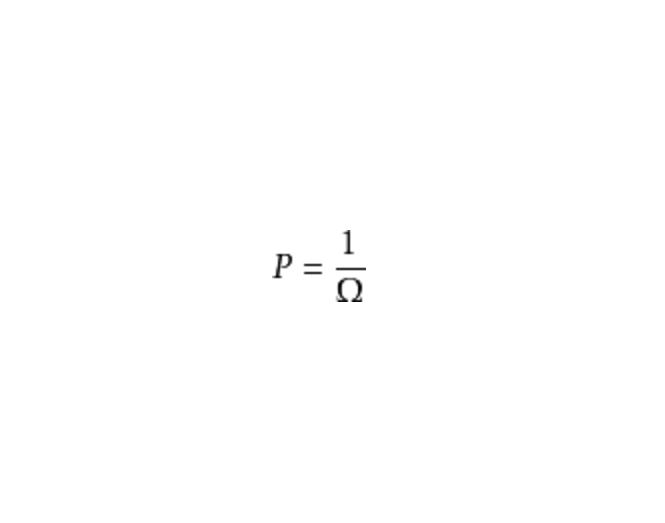機率
在所有可能發生的事件(變數)中,某種事件(變數)發生可能性(或出現相對機會)的大小稱為該事件發生的機率。如果在N次(N很大)試驗中,某事件X出現了Ni次,則比值Ni/N就叫X事件出現的機率,用
表示。例如,我們做拋擲硬幣的試驗,共拋擲了10000次,其中出現正面的次數接近5000次,則出現正面的機率p
正=5000/10000=1/2。由於各種可能發生事件的總數
,所以
即各種可能發生事件的機率之和等於1。這一結論稱為機率的歸一化條件。
如果表示事件X的量 x 可以連續變化,我們就說 x 具有連續值譜。這時,x 出現在某一間隔 Δx 內的機率Δp(x) 應與這一間隔的位置 x 及大小Δx 有關。變數在 x 附近單位間隔內出現的機率稱為
機率密度,用 f(x) 表示,於是便有Δp(x)=f(x)Δx。當Δx→0 時,Δp(x) 應寫成微分式
機率密度 f(x) 反映了事件機率隨 x 而分布的規律,所以又叫
機率分布函式。
等機率假設
根據
氣體動理論,當氣體處於平衡態時,雖然其巨觀態可以確定,但其微觀態卻仍不能確定(一切分子都處於永不停息的無規則運動中),而且也找不到任何理由來說明,某些微觀態要比另一些微觀態優越。基於這樣的事實,1871年,
玻耳茲曼提出了著名的等機率假設:當系統處於平衡態時,其各個可能的微觀態出現的機率相等。對於氣體而言,等機率假設也可以這樣來表述:當氣體處於平衡態時,其分子向各個方向運動的機率相等。
等機率假設是平衡態
統計理論的基礎,其正確性雖然不能直接由實驗來驗證,但由它所得到的許多推論都與客觀事實相符,因而便間接地證明了等機率假設是正確的。
在統計熱力學中的表達
所有能級分布
微觀狀態數之和構成了系統的總微管狀態數,簡稱總微態數,用 Ω 表示
N、U、V確定的粒子系統,可能的能級分布方式D及其微管狀態數WD是確定的,系統的總微觀狀態數Ω也是確定的。也就是說,Ω是N、U、V的函式
統計熱力學假設:對於N、U、V確定的粒子系統,每種微觀狀態出現的數學機率相等,均等於總
微觀狀態數的倒數
該假設稱為等機率假設,是統計熱力學的基本假設。統計熱力學認為在任意短的觀測時間(Δt
min→0)內,粒子系統將經歷所有可能的微觀狀態,系統的巨觀熱力學性質正是所有這些可能微觀狀態統計平均的結果,而每一種微觀狀態在統計平均中的貢獻是相等的。等機率假設的正確性無法證明,但它顯然是合理的,因為我們找不到任何理由相信兩種微觀狀態出現的數學機率會不同。