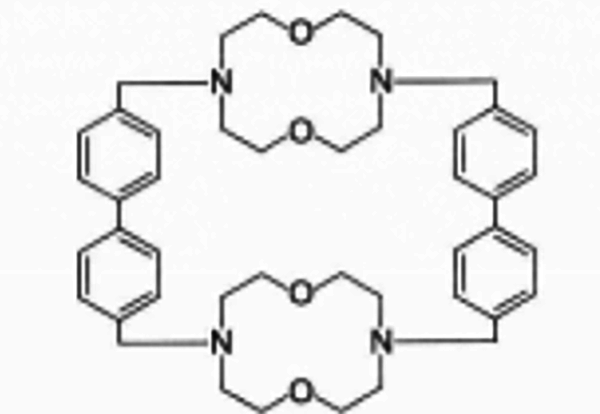
基本介紹
舉例及命名,由來及特點,配合物,
舉例及命名
如18-冠醚-6,“18”表示環原子總數,“6”表示能和金屬離子結合形成配位化合物的氧原子數。在鹼金屬離子中,銣太大,鋰太小,它只能選擇性地和鉀離子結合,因而能從混合物中單一地萃取鉀。由於形成的配位化合物外觀似皇冠,故名“冠醚”。環聚醚的氧原子可為氮或硫原子等取代。這些穴合劑和金屬離子結合時,選擇性極高,形成的穴合物穩定性差別極大,有潛在的套用價值。如作為選擇性極高的催化劑或從海水中單一地提取鈾或金等貴金屬。
由來及特點
穴狀化合物(CryPtate)是巨多環的絡合物,這方面的研究在70年代有了迅速的發展。巨多環作為配體有特別高的選擇性,與金屬形成的絡合物特別穩定.最簡單的是單環(圖7(a1)),較複雜的為雙環(圖7(a1))、三環(圖7(a3))和四環(圖7(a4))。它們的形狀可以是柱狀,也可以是球狀等。最初研究的是聚醚(圖7(b))。雙環聚醚與鹼金屬離子形成穴合物都比較穩定。但對各個鹼金屬離子化合物的穩定性則因環的大小不同而有很大的差別。如雙環聚醚2.1.1的鈉絡合物最穩定,而雙環聚醚2.2.2的鉀絡合物最穩定。因此,它們可用作製備鹼金屬離子選擇性電極的原材料。聚醚與鹼土金屬離子也形成較穩定的穴合物。
 穴狀化合物
穴狀化合物聚醚的氧原子可為N或S原子所取代。取代後與鹼金屬和鹼土金屬離子所形成的穴合物即不穩定。但與其他類離子如Ag+、Ti+、Cd2+、Pb2+的化合物的穩定性則增高。例如,把聚醚2.2.2的一個“=O”改為“=NCH3”,Pb(Ⅱ)絡合物的穩定性就提高103倍,Cd(Ⅱ)絡合物的穩定性提高105倍。從上述可見,穴合物的選擇性和所形成的穴合物的穩定性是受穴合物環的多寡、大小、配位原子(O、S、N或P)和連於配位原子的取代基團等因素的顯著影響的。因此,有人認為調節這些因素應可能使穴合劑的選擇性達到如此高的地步,以致能夠從海水中提取鈾或金等貴重元素。總之,穴合物無論從基礎理論的研究或實際套用,都是一類前途未可限量的化合物。
配合物
三環穴狀配體具有10個結合位點和球形的空腔。另一個具有球形空腔的分子(但是它不是一個穴狀配體),能與Li+和Na+複合(更易與Na+複合),但不與K+、Mg2+或Ca2+結合。像這些分子,它們的空腔只能被球形的實體占據,被稱為球形配體(spherand)。其它的類型還有杯芳烴(calixarene)。在杯[4]芳烴中,苯酚OH存在大量的氫鍵,但是隨著杯芳烴環增大,空腔增大,氫鍵會消失。此外杯[4]芳烴存在構象異構體的平衡(錐形互變),有時可以將二者分離出來,如杯[8]芳烴和氮雜杯芳烴口。應當指出的是,在未取代的問位加入取代基,可使杯[4]芳烴結構更固定,也可大大減少杯[8]芳烴的構象可變性。人們已經知道有醯胺橋連的杯[4]芳烴、杯[4]薁和醌橋連的杯[4]芳烴,杯[4]芳烴二銨鹽也被製得。對映體純的杯[4]間苯二酚芳烴衍生物已有報導,水溶性的杯[4]芳烴也已被製備出。此外,還有各種各樣的杯[n]冠醚,其中有些是穴狀配位體。