化合物簡介,基本信息,理化性質,藥典標準,來源,性狀,鑑別,檢查,含量測定,類別,貯藏,製劑,藥品簡介,所屬類別,適應症,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,
化合物簡介
基本信息
化學式:C19H28N4O6S2
分子量:472.579
CAS號:33075-00-2
EINECS號:278-355-8
理化性質
密度:1.45g/cm
折射率:1.652
藥典標準
來源
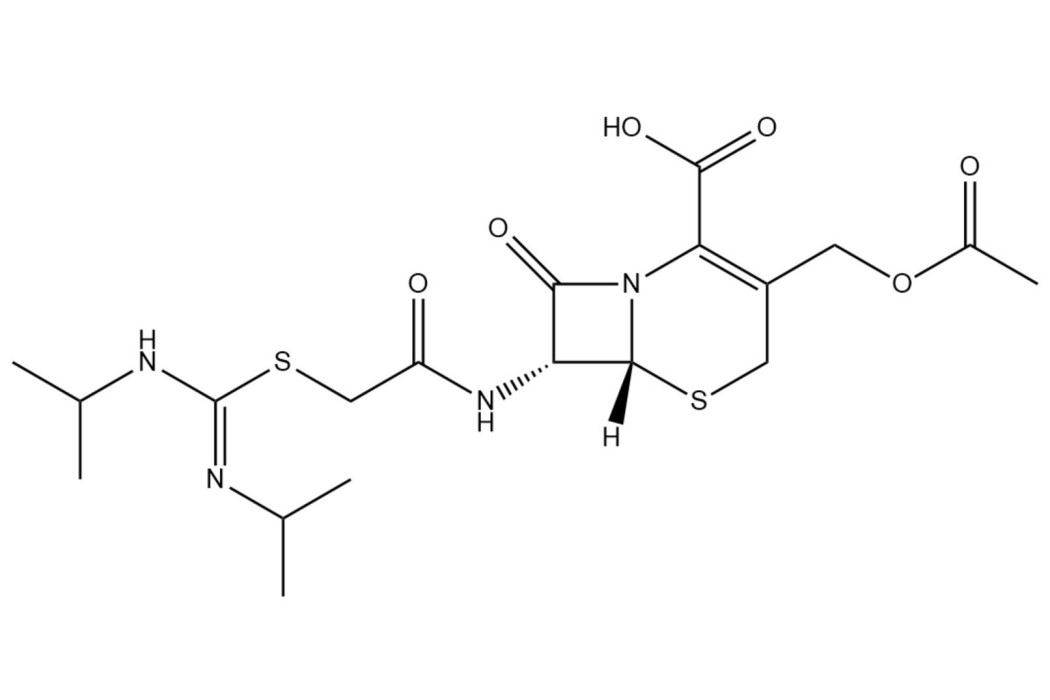
本品為(6R,7R)-3-[(乙醯氧基)甲基]-7-[α-(N,N-二異丙基脒硫基)乙醯氨基]-8-氧代-5-硫雜-1-氮雜雙環[4.2.0]辛-2-烯-2-甲酸內銨鹽,按無水物計算,含C19H28N4O6S2不得少於97.0%。
性狀
本品為白色或類白色結晶性粉末,幾乎無臭,有引濕性。
本品在水中極易溶解,在乙醇中微溶,在丙酮、三氯甲烷或乙醚中不溶。
比旋度
取本品,精密稱定,加水溶解並定量稀釋製成每1mL中約含10mg的溶液,依法測定,比旋度為+135°至+145°。
鑑別
1、照薄層色譜法(通則0502)試驗。
供試品溶液:取本品適量,加水溶解並稀釋製成每1mL中約含20mg的溶液。
對照品溶液:取頭孢硫脒對照品適量,加水溶解並稀釋製成每1mL中約含20mg的溶液。
系統適用性溶液:取對照品溶液和供試品溶液等量混合。
色譜條件:採用矽膠G薄層板[取矽膠G2.5g,加含1%羧甲基纖維素鈉的磷酸鹽緩衝液(pH5.8)適量,調漿制板,經105℃活化1小時,放入乾燥器中備用],以新鮮製備的甲醇-異丙醇-磷酸鹽緩衝液(pH5.8)(7:2:1)濾過後為展開劑。
測定法:吸取上述三種溶液各1µL,分別點於同一薄層板上,展開,晾乾,100℃加熱30分鐘,置碘蒸氣中顯色。
系統適用性要求:系統適用性溶液應顯單一斑點。
結果判定:供試品溶液所顯主斑點的位置和顏色應與對照品溶液主斑點的位置和顏色相同。
2、在含量測定項下記錄的色譜圖中,供試品溶液主峰的保留時間應與對照品溶液主峰的保留時間一致。
3、本品的紅外光吸收圖譜應與對照的圖譜(光譜集924圖)一致。
以上1、2兩項可選做一項。
檢查
結晶性
取本品少許,依法檢查(通則0981),應符合規定。
酸度
取本品,加水製成每1mL中含0.1g的溶液,依法測定(通則0631),pH值應為4.0~6.0。
溶液的澄清度與顏色
取本品5份,分別加水製成每1mL中含0.1g的溶液,溶液應澄清無色,如顯渾濁,與1號濁度標準液比較,均不得更濃,如顯色,與黃色或黃綠色6號標準比色液(通則0901第一法)比較,均不得更深。
有關物質
照高效液相色譜法(通則0512)測定。
供試品溶液:取本品適量,加流動相溶解並稀釋製成每1mL中約含0.5mg的溶液。
對照溶液:精密量取供試品溶液適量,用流動相定量稀釋製成每1mL中約含5µg的溶液。
雜質C對照品溶液:取雜質C對照品適量,加流動相溶解並定量稀釋製成每1mL中約含0.25µg的溶液。
系統適用性溶液:取頭孢硫脒對照品適量,加水溶解並定量稀釋製成每1mL中約含0.5mg的溶液,在90℃水浴中加熱30分鐘,放冷。
靈敏度溶液:精密量取對照溶液適量,用流動相定量稀釋製成每1mL中約含0.5µg的溶液。
色譜條件:用十八烷基矽烷鍵合矽膠為填充劑(Kromasil 100-5 Cl8,4.6mm×250mm,5µm或效能相當的色譜柱),以磷酸鹽緩衝液(取無水磷酸氫二鈉2.76g,枸櫞酸酸1.29g,加水溶解並稀釋成1000mL)-乙腈(86:14)為流動相,檢測波長為254nm,進樣體積10µL。
系統適用性要求:系統適用性溶液色譜圖中,雜質D峰(相對保留時間約為0.9)與頭孢硫脒峰之間的分離度應符合要求。靈敏度溶液色譜圖中,主成分色譜峰峰高的信噪比應大於10。
測定法:精密量取供試品溶液、對照溶液與雜質C對照品溶液,分別注入液相色譜儀,記錄色譜圖至主成分峰保留時間的2.5倍。
限度:供試品溶液色譜圖中如有雜質峰,雜質C峰面積不得大於對照溶液主峰面積的0.1倍(0.1%),其他單個雜質峰面積不得大於對照溶液主峰面積的0.5倍(0.5%),各雜質峰面積的和不得大於對照溶液主峰面積的1.5倍(1.5%),小於靈敏度溶液主峰面積0.5倍的峰忽略不計。
殘留溶劑
照殘留溶劑測定法(通則0861第二法)測定。
供試品溶液:取本品0.2g,精密稱定,置頂空瓶中,精密加水2mL使溶解,密封。
對照品溶液:取甲醇、乙醇、丙酮、 二氯甲烷各適量,精密稱定,加水定量稀釋製成每1mL中含甲醇0.3mg、乙醇0.5mg、丙酮0.5mg、二氯甲烷0.06mg的混合溶液,精密量取2mL置頂空瓶中,密封。
色譜條件:以6%氰丙基苯基-94%二甲基聚矽氧烷(或極性相近)為固定液的毛細管柱為色譜柱,起始溫度為40℃,待二氯甲烷洗脫後,以每分鐘30℃的速率升溫至150℃,維持5分鐘,進樣口溫度為200℃,檢測器溫度為250℃,頂空瓶平衡溫度為80℃,平衡時間為30分鐘。
系統適用性要求:對照品溶液色譜圖中,各峰間的分離度均應符合要求 。
測定法:取供試品溶液與對照品溶液分別頂空進樣,記錄色譜圖。
限度:按外標法以峰面積計算,甲醇、乙醇、丙酮與二氯甲烷的殘留量均應符合規定。
水分
取本品,照水分測定法(通則0832第一法1)測定,含水分不得過1.5%。
可見異物
取本品5份,每份各2.0g,加微粒檢查用水溶解,依法檢查(通則0904),應符合規定。(供無菌分裝用)
不溶性微粒
取本品,加微粒檢查用水製成每1mL中含80mg的溶液,依法檢查(通則0903),每1g樣品中含10μm及10μm以上的微粒不得過6000粒,含25μm及25μm以上的微粒不得過600粒。(供無菌分裝用)
細菌內毒素
取本品,依法檢查(通則1143),每1mg頭孢硫脒中含內毒素的量應小於0.075EU。(供注射用)
無菌
取本品,用適宜溶劑溶解並稀釋後,經薄膜過濾法處理,依法檢查(通則1101),應符合規定。(供無菌分裝用)
含量測定
照高效液相色譜法(通則0512)測定。
供試品溶液
取本品適量,精密稱定,加水溶解並定量稀釋製成每1mL中約含0.1mg的溶液。
對照品溶液
取頭孢硫脒對照品適量,精密稱定,加水溶解並定量稀釋製成每1mL中約含0.1mg的溶液。
系統適用性溶液
見有關物質項下 。
色譜條件
用十八烷基矽烷鍵合矽膠為填充劑,以磷酸鹽緩衝液(取無水磷酸氫二鈉2.76g、枸櫞酸1.29g,加水溶解並稀釋成1000mL)-乙腈(80:20)為流動相,檢測波長為254nm,進樣體積10μL。
系統適用性要求
系統適用性溶液色譜圖中,頭孢硫脒峰與雜質D峰(相對保留時間約為1.3)之間的分離度應大於2.0。
測定法
精密量取供試品溶液與對照品溶液,分別注入液相色譜儀,記錄色譜圖。按外標法以峰面積計算。
類別
β-內醯胺類抗生素,頭孢菌素類。
貯藏
密封,在冷暗乾燥處保存。
製劑
注射用頭孢硫脒。
藥品簡介
所屬類別
化藥及生物製品 >> 抗微生物藥 >> 抗細菌藥 >> 抗生素類
適應症
用於敏感菌所引起呼吸系統、肝膽系統、五官、尿路感染及心內膜炎、敗血症。
用法用量
用法:肌內注射或靜脈注射。
臨用前加滅菌注射用水或氯化鈉注射液適量溶解,再用生理鹽水或5%葡萄糖注射液250mL稀釋。藥液宜現用現配,配製後不宜久置。
用量:
肌肉注射: —次0.5g~1.0g(0.5g:1~2支;1.0g:1/2~1支),一日4次:小兒按體重一日50mg~100mg/kg,分3~4次給藥。
靜脈注射:一次2g(0.5g:4支;1.0g:2支),一日2~4次,小兒按體重一日50mg~100mg/kg,分2~4次給藥。
不良反應
主要不良反應蕁麻疹、哮喘、皮膚瘙癢,寒戰高熱、血管神經性水腫等。偶見治療後血尿素氮、谷丙轉氨酶、鹼性磷酸酶升高。少數患者用藥後可能出現中性粒細胞減少,念珠菌、葡萄球菌等二重感染。
禁忌
對頭孢菌素類抗生素過敏者禁用,有青黴素過敏性休克史者。
注意事項
1、交叉過敏反應:套用本品前須詳細詢問頭孢菌素類及青黴素類的藥物過敏史,對一種頭孢菌素或頭黴素(cephamycin)過敏者對其他頭孢菌素或頭黴素也可能過敏。對青黴素類、青黴素衍生物或青黴胺過敏者也可能對頭孢菌素或頭黴素過敏。對青黴素過敏病人套用頭孢菌素時發生過敏反應者達5%~7%;如做免疫反應測定時,則對青黴素過敏病人對頭孢菌素過敏者達20%。
2、對青黴素過敏病人套用本品時應根據病人情況充分權衡利弊後決定。有青黴素過敏性休克或即刻反應者,不宜再選用頭孢菌素類。
3、有胃腸道疾病史者,特別是潰瘍性結腸炎、局限性腸炎或抗生素相關性結腸炎(頭孢菌素類少產生偽膜性結腸炎)者應慎用。
4、腎功能減退病人套用本品須適當減量。
5、對診斷的干擾:套用本品的病人抗球蛋白試驗可出現陽性;孕婦產前套用本品,此陽性反應也可出現於新生兒。
6、長期用藥應監測肝、腎功能和血象。
孕婦及哺乳期婦女用藥
懷孕早期應慎用。哺乳期婦女套用頭孢菌素類雖尚未見發生問題的報導,其套用仍須權衡利弊。
兒童用藥
未進行該項實驗且無可靠參考文獻。
老年用藥
老年患者腎功能減退,套用時須適當減量。
藥物相互作用
本品肌內注射合用丙磺舒1 g後,12小時尿排泄量降為給藥量的65.7%。
藥物過量
尚不明確。如出現藥物過量,一般應採用對症治療和支持治療。
藥理毒理
藥理作用
對
革蘭陽性菌及部分陰性菌有抗菌活性,對革蘭陽性球菌的作用尤強。體外抗菌活性試驗表明:對
肺炎球菌、
化膿性鏈球菌、
金黃色葡萄球菌(MSSA菌株)、表皮葡萄球菌(MSSE菌株)和卡他布蘭漢菌有較強的抗菌活性,對肺炎鏈球菌MIC90為0.25μg/mL,對其他3種細菌的MIC90均小於8.0μg/mL,對流感嗜血桿菌亦有較強的抗菌活性,MIC90為2.0μg/mL。對腸球菌亦顯示有很強的體外抗菌活性,MIC90為2.0μg/mL。對草綠色鏈球菌、溶血性鏈球菌、非溶血性鏈球菌、白喉桿菌、產氣莢膜桿菌、破傷風桿菌和炭疽桿菌均有良好抗菌作用。對金黃色葡萄球菌(MRSA菌株)、表皮葡萄球菌(MRSE菌株)的體外抗菌活性不如萬古黴素。本品作用機制為抑制敏感菌的細胞壁合成,而產生殺菌作用。
毒理研究
本品小鼠靜脈注射的LD50為(1.02±0.04) g/kg,腹腔注射的LD50為(1.26±0.23) g/kg生殖毒性試驗中,試驗組小鼠的胎仔死亡率明顯高於對照組(p<0.01)。
藥代動力學
本品口服不吸收,靜脈滴注1.0g後,血藥峰濃度(cmax)為(68.93±6.86) mg/L,血消除半衰期(t1/2β)為(1.19+0.12)h,血藥濃度-時間曲線下面積(AUC)為(94.7±9.8)mg/(L·h),12小時尿藥累計排泄率為93.1土3.2%。肌肉注射1.0g後,血藥峰濃度(cmax)為(35.12土4.34)mg/L,達峰時間為(0.78±0.08)h,血清除半衰期(t1/2β)為(1.38土0.21)h,血藥濃度-時間曲線下面積(AUC)為(85.3±8.0)mg/(L·h),12小時尿中藥累計排泄率為84.2±5.9%。與靜脈滴注相比,肌肉注射絕對生物利用度為90.3±6.4%。
本品注射後在體內組織分布廣泛,以膽汁、肝、肺等處含量為高,不透過血-腦脊液屏障。血漿蛋白結合率約23%。在機體內幾乎不代謝,主要從尿中排出,12小時尿中排出給藥量的90%以上。腎功能減退患者,肌肉注射後血清半衰期延長至13.2小時,約為正常半衰期的10倍,24小時尿中僅排出給藥量的3.2%,血液透析可排出給藥量的20%~30%。