《用於合成卡帕芬淨的中間體及其製備方法》是江蘇盛迪醫藥有限公司於2012年3月21日申請的發明專利,該專利的申請號為2012800020220,公布號為CN103003295A,授權公布日為2013年3月27日,發明人是張富堯、神小明、胡高強、孫飄揚。
《用於合成卡帕芬淨的中間體及其製備方法》涉及一種用於合成卡帕芬淨的中間體,以及此中間體的製備方法。通過此中間體可以有效地製備卡帕芬淨。
2019年7月15日,《用於合成卡帕芬淨的中間體及其製備方法》獲第十一屆江蘇省專利項目獎優秀獎。
基本介紹
- 中文名:用於合成卡帕芬淨的中間體及其製備方法
- 公布號:CN103003295A
- 公布日:2013年3月27日
- 申請號:2012800020220
- 申請日:2012年3月21日
- 申請人:江蘇盛迪醫藥有限公司
- 地址:上海市浦東新區張江高科技園區蔡倫路399號
- 發明人:張富堯、神小明、胡高強、孫飄揚
- Int.Cl.:C07K7/56(2006.01)I、C07K1/06(2006.01)I、A61K38/12(2006.01)I、A61P31/10(2006.01)I
- 代理機構:北京戈程智慧財產權代理有限公司
- 代理人:程偉、朱慧寧
- 類別:發明專利
專利背景,發明內容,專利目的,技術方案,權利要求,實施方式,榮譽表彰,
專利背景
卡帕芬淨(caspofungin)是21世紀初開發上市的棘白黴素類抗真菌新型藥物,於2001年2月在美國首次上市,是一種具有全新作用機理的抗真菌藥物,通過阻止真菌細胞壁結構成分β-葡聚糖的合成而達到殺真菌作用。卡帕芬淨具有廣譜抗菌活性,無交叉耐藥性以及未發現明顯毒性問題等優點,適用於治療全身性真菌感染疾病,包括各種侵襲性麴黴菌病與念珠菌病,其療效優於兩性黴素Β,對於常見頑固性念珠菌病的療效尤佳。
卡帕芬淨通過以生物發酵中間體肺念菌素BO(PB0)為原料半合成製得,例如,US5552521,US5936062,US20100168415,WO2002083713,WO2007057141,CN101648994,CN101792486等專利文獻均詳細地描述了各種製備卡帕芬淨的方法,在這些方法中都是以式Γ所示的化合物為重要中間體,所用的離去基團都為巰基取代的芳環化-Ar,例如苯硫酚。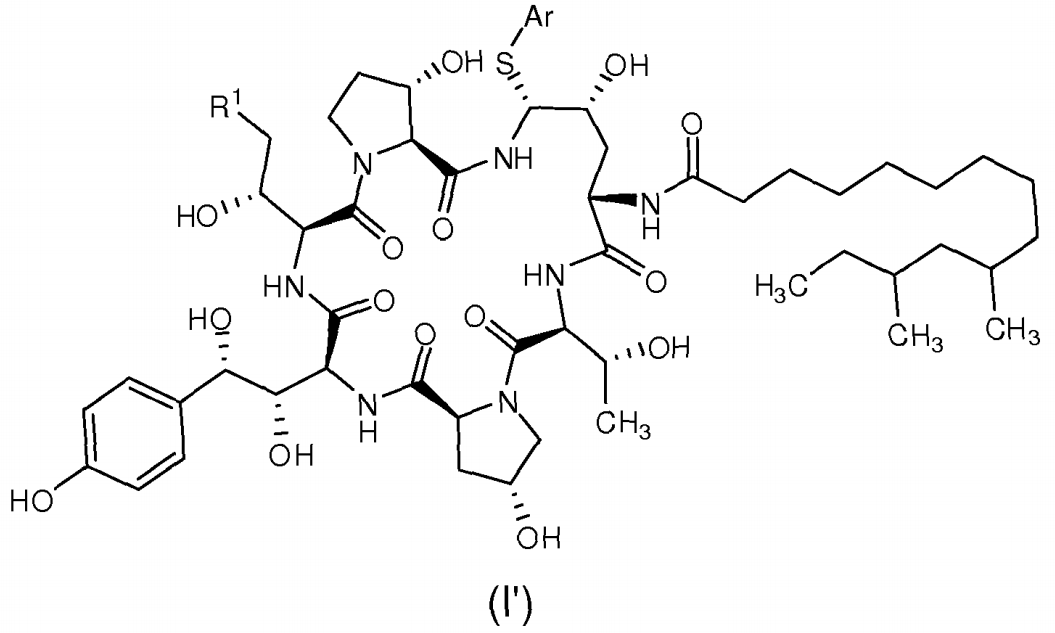

由於巰基取代的芳環化合物在置換過程中存在區域選擇性問題,在製備卡帕芬淨過程中必須使用數個色譜純化步驟分離純化中間體和最終產物,從而導致製備卡帕芬淨的低產率,高成本,操作繁瑣等問題。因此在本領域中仍存在進一步研究開發製備卡帕芬淨的新方法的需求。
發明內容
專利目的
《用於合成卡帕芬淨的中間體及其製備方法》涉及用於合成卡帕芬淨的中間體及其製備方法。通過此中間體,可以簡化合成卡帕芬淨操作過程,提高卡帕芬淨的合成效率。該發明目的在於提供一種如式(I)所示的用於製備卡帕芬淨的中間體,
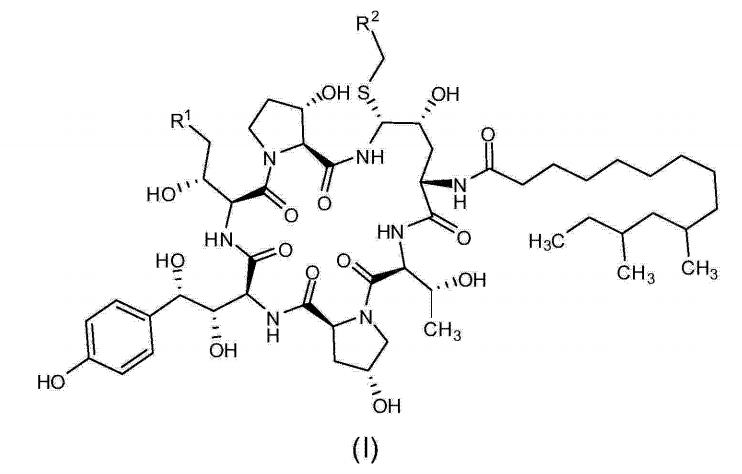
其中,R為C(=0)NH2、CN或CH2NRR;R為CN、CO2R、C(=0)NRR或取代或非取代的C6-10芳基或雜環芳基;R和R各自分別為氫或胺基保護基,例如Boc、Cbz等;R可以為氫、直鏈或支鏈的C1-10垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的Cwo垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;或R、R和氮原子一起形成5-8元雜環,優選五元環和六元環;R和R不能同時為胺基或甲氧基。
優選地,R為C(=0)NH2、CN或CH2NH2;R為CN、CO2H、CO2Me、CO2Et、CO2Bu、CO2Bu、CO2Ph、C(=0)NH2、C(=0)NMe2、C(=0)NHEt、C(=0)NHBu、C(=0)NHCH2CH2NH2、C(=0)NHPr、C(=0)NH'Pr、C(=0)NHPen,C(=0)NHBu、C(=0)NHPh或苯基,更優選R為CO2H、CO2Me或C(=0)NHCH2CH2NH2。
在《用於合成卡帕芬淨的中間體及其製備方法》的一個優選的具體實施方案中,在式(I)中,R為CH2NH2;R為CO2Me。
《用於合成卡帕芬淨的中間體及其製備方法》目的在於提供一種如式I所示的中間體的製備方法,包括將式(II)所示的中間體II在有機硼酸和有機磺酸的作用下與式(III)所示的巰基化合物III反應製得式(I)所示的中間體I;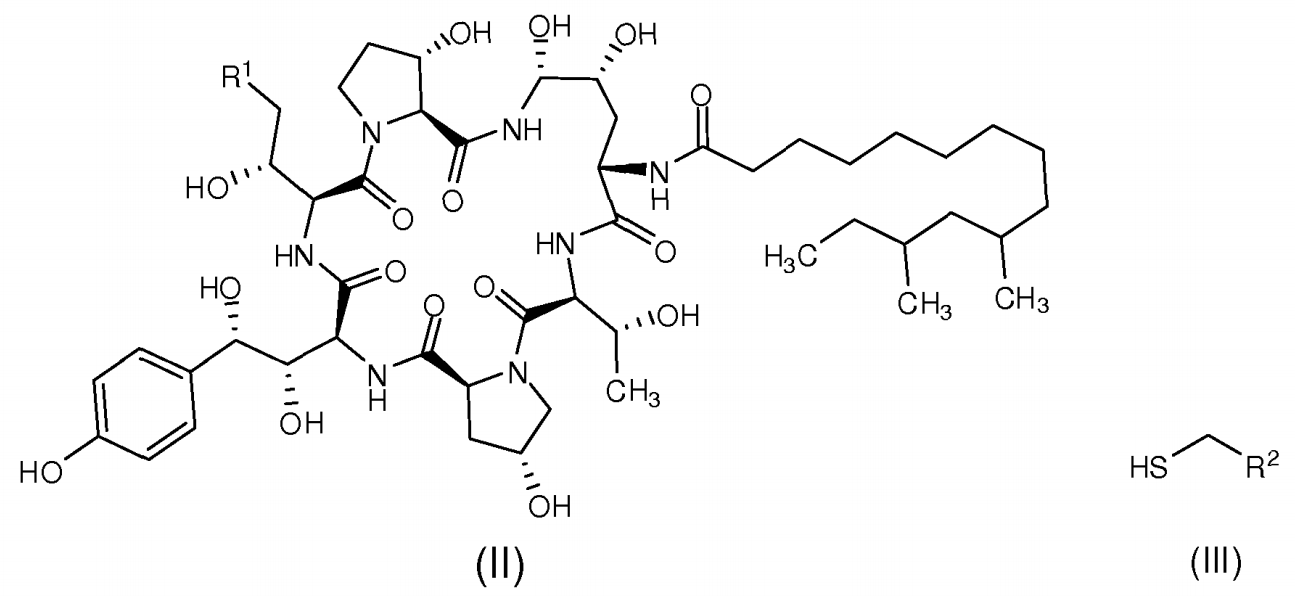

其中,R為C(=0)NH2、CN或CH2NRR;R為CN、CO2R、
C(=0)NRR或取代或非取代的C6-100芳基或雜環芳基;R和R各自分別為氫或胺基保護基,例如Boc、Cbz等;R可以為氫、直鏈或支鏈的C^o垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的Cwo垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;或R、R和氮原子一起形成5-8元雜環,優選五元環和六元環;R和R不能同時為胺基或甲氧基。
技術方案
《用於合成卡帕芬淨的中間體及其製備方法》還提供一種卡帕芬淨的製備方法,包括如下步驟:
1)式(II)所示的中間體II在有機硼酸和有機磺酸的作用下與式(III)所示的巰基化合物III反應製得式(I)所示的中間體I;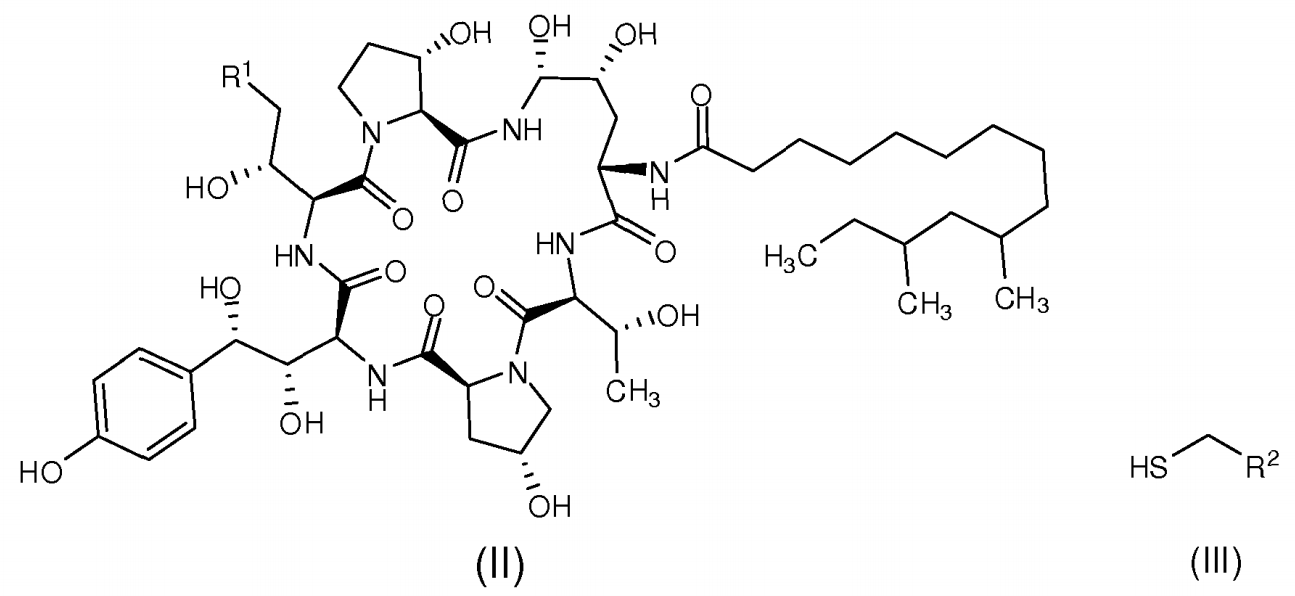

其中,R為C(=0)NH2、CN或CH2NRR;R為CN、CO2R、C(=0)NRR或取代或非取代的C6-10芳基或雜環芳基;R和R各自分別為氫或胺基保護基,例如Boc、Cbz等;R可以為氫、直鏈或支鏈的。垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的C^o垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;或R、R和氮原子一起形成5-8元雜環,優選五元環和六元環;R和R不能同時為胺基或甲氧基;
2)式(I)所示的中間體與乙二胺反應,當式(I)所示的中間體的R不為CH2NHJf,根據需要在與乙二胺反應前或反應後將R還原成CH2NH2或脫去胺基保護基,使得最終得到卡帕芬淨,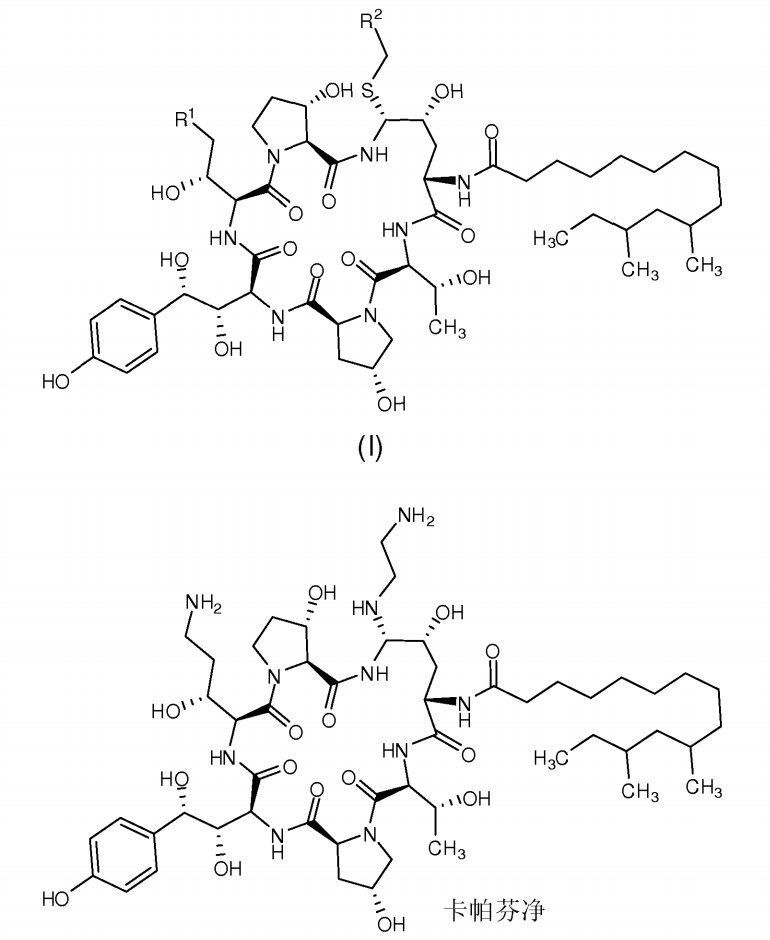

其中,R為C(=0)NH2、CN或CH2NRR;R為CN、CO2R、C(=0)NRR或取代或非取代的C6-10芳基或雜環芳基;R和R各自分別為氫或胺基保護基,所述胺基保護基優選Boc、Cbz;R可以為氫、直鏈或支鏈的垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;或R、R和氮原子一起形成5-8元雜環,優選五元環和六元環;R和R不能同時為胺基或甲氧基。
在《用於合成卡帕芬淨的中間體及其製備方法》優選的具體實施方式中,該方法包括如下步驟:
1)式(IIΑ)所示的中間體IIΑ在有機硼酸和有機磺酸的作用下與式(III)所示的巰基化合物III反應製得式(IA)所示的中間體IA,
2)式(IA)所示的中間體IA與乙二胺反應得到卡帕芬淨。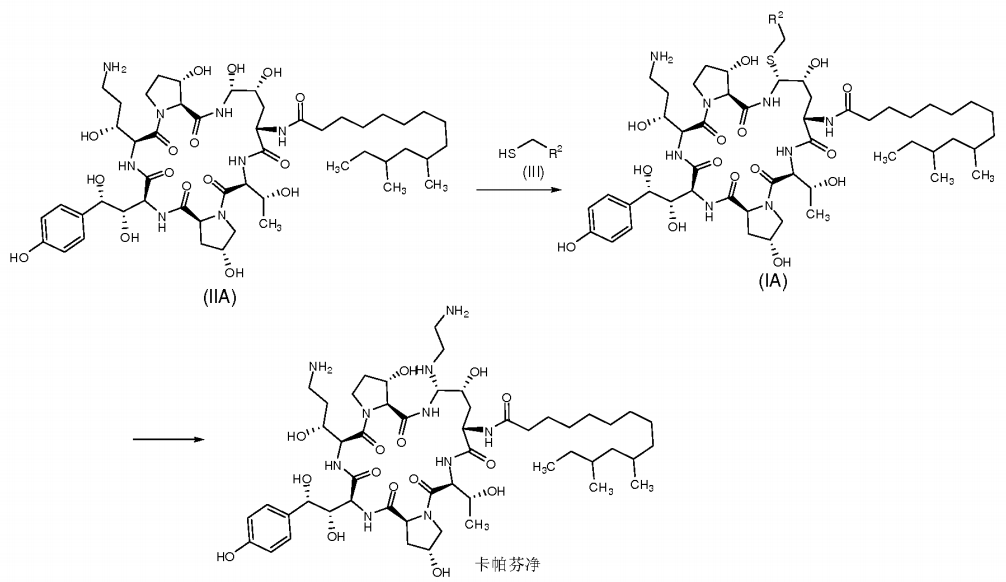

在《用於合成卡帕芬淨的中間體及其製備方法》的另一個優選的實施方式中,該方法包括如下步驟:
1)式(IIΒ)所示的中間體IIΒ在有機ΐ朋酸和有機磺酸的作用下與式(III)所示的巰基化合物III反應製得式(IB)所示的中間體IB,
2)式(IB)所示的中間體IB與乙二胺反應得到式(IVB)所示的中間體IVB,
3)式(IVB)所示的中間體IVB經還原的得到卡帕芬淨。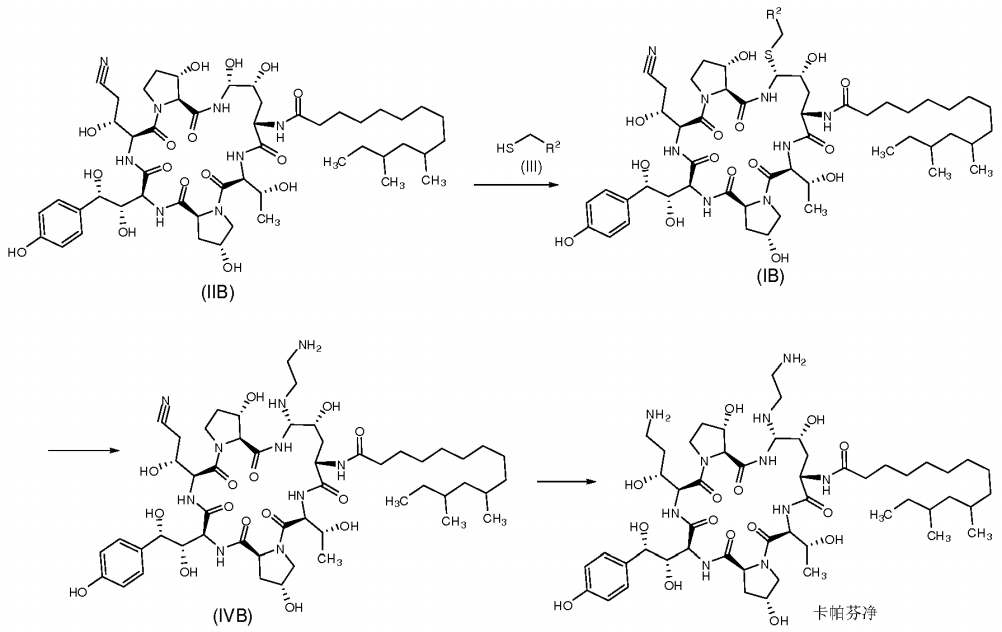

在《用於合成卡帕芬淨的中間體及其製備方法》的又一個優選的實施方式中,該方法包括如下步驟:
1)式(IIC)所示的中間體IIC在有機硼酸和有機磺酸的作用下與式(III)所示的巰基化合物III反應製得式(IC)所示的中間體IC,
2)式(IC)所示的中間體IC與乙二胺反應得到式(IVC)所示的中間體IVC,
3)式(IVC)所示的中間體IVC經還原的得到卡帕芬淨。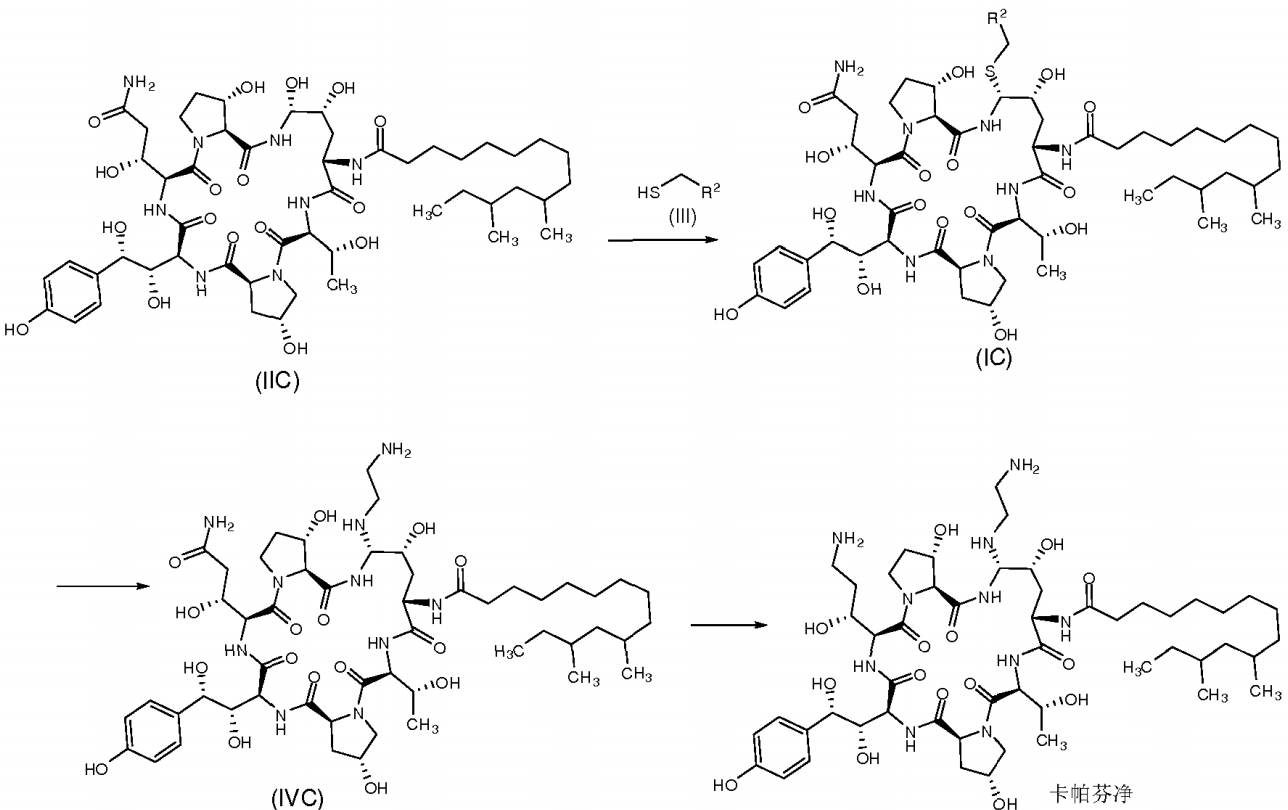

《用於合成卡帕芬淨的中間體及其製備方法》的胺基保護基是本領域已知的適當的用於胺基保護的基團,參見文獻("Protective Groupsin Organic Synthesis",5.Ed.T.W.Greene&RG.M.Wuts)中的胺基保護基團,優選地,所述的胺基保護基為Boc或Cbz。
《用於合成卡帕芬淨的中間體及其製備方法》所述的C6-10芳基可以是單環或稠環、多環,例如可以是苯基,萘基。C6-10芳基可以是取代的或未取代的,當被取代時,取代基優選為一個或多個以下基團,獨立地選自垸基、垸氧基、鹵素、羥基、硝基、氰基、環垸基、雜環基、芳基、雜芳基、-NRR、-C(0)OR、-OC(0)R、-0(CH2)mC(0)OR、-OC(0)NRR、羰基、-S(0)nR8、-OS02R8、-S02NRR、或-NHC(0)R;m可以為0、1或2;n可以為0、1或2。R和R的定義如通式(I)化合物中所述,R可以為直鏈或支鏈的Cwo垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的Cw。芳基或雜環芳基;其中鹵素可以為氟、氯、溴或碘。該發明所述的雜環芳基指包含1至4個雜原子,5至10個環原子的雜芳族體系,其中雜原子包括氧、硫和氮。雜芳基優選為是5元或6元雜芳基。例如呋喃基、噻吩基、吡啶基、吡咯基、N-垸基吡咯基、嘧啶基、吡嗪基、咪唑基、四唑基等。雜芳基可以是取代的或未取代的,當被取代時,取代基優選為一個或多個以下基團,獨立地選自垸基、垸氧基、鹵素、羥基、硝基、氰基、環垸基、雜環基、芳基、雜芳基、-NRR、-C(0)OR、-OC(0)R、-0(CH2)mC(0)OR、-OC(0)NRR、羰基、-S(0)nR8、-OS02R8、-S02NRR、或-NHC(0)R;m可以為0、1或2;n可以為0、1或2。R和R的定義如通式(I)化合物中所述,R可以為直鏈或支鏈的垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;其中鹵素可以為氟、氯、溴或碘。
《用於合成卡帕芬淨的中間體及其製備方法》所述的垸基是指飽和的脂族烴基團,例如甲基、乙基、丙基、2-丙基、正丁基、異丁基、叔丁基或戊基等。更優選的是含有1至4個碳原子的低級垸基,例如甲基、乙基、丙基、2-丙基、正丁基、異丁基或叔丁基等。垸基可以是取代的或未取代的,當被取代時,取代基優選為一個或多個以下基團,獨立地選自垸基、垸氧基、鹵素、羥基、硝基、氰基、環垸基、雜環基、芳基、雜芳基、-NRR、-C(0)OR-OC(0)R、-0(CH2)mC(0)OR、-OC(0)NRR、羰基、-S(0)nR8、-OS02R8、-S02NRR、或-NHC(0)R;m可以為0、1或2;n可以為0、1或2。R和R的定義如通式(I)化合物中所述,R可以為直鏈或支鏈的Cwo垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的Cw。芳基或雜環芳基;其中鹵素可以為氟、氯、溴或碘。
《用於合成卡帕芬淨的中間體及其製備方法》所述的C3-8環垸基是指3至8元全碳單環基團,其中3至8元全碳單環可以含有一個或多個雙鍵,但沒有一個環具有完全共軛的π電子系統。例如環丙基、環丁基、環戊基、環戊烯基、環己垸基、環己二烯基、環庚垸基、環庚三烯基等。環垸基可以是取代或未取代的。當被取代時,取代基優選為一個或多個以下基團,獨立地選自垸基、垸氧基、鹵素、羥基、硝基、氰基、環垸基、雜環基、芳基、雜芳基、-NRR、-C(0)OR、-OC(0)R、-0(CH2)mC(0)OR、-OC(0)NRR、羰基、-S(0)nR8、-OS02R8、-S02NRR、或-NHC(0)R;m可以為0、1或2;n可以為0、1或2。R和R的定義如通式(I)化合物中所述,R可以為直鏈或支鏈的垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-10環垸基或取代或非取代的C6-10芳基或雜環芳基;其中鹵素可以為氟、氯、溴或碘。
該發明所述的c3-10。烯基可以是取代的或未取代的,當被取代時,取代基優選為一個或多個以下基團,獨立地選自垸基、垸氧基、鹵素、羥基、硝基、氰基、環垸基、雜環基、芳基、雜芳基、-NRR、-C(0)OR-OC(0)R、-0(CH2)mC(0)OR、-OC(0)NRR、羰基、-S(0)nR8、-OS02R8、-S02NRR、或-NHC(0)R;m可以為0、1或2;n可以為0、1或2。R和R的定義如通式(I)化合物中所述,R可以為直鏈或支鏈的Cwo垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;其中鹵素可以為氟、氯、溴或碘。
該發明所述的。炔基可以是取代的或未取代的,當被取代時,取代基優選為一個或多個以下基團,獨立地選自垸基、垸氧基、鹵素、羥基、硝基、氰基、環垸基、雜環基、芳基、雜芳基、-NRR、-C(0)OR-OC(0)R、-0(CH2)mC(0)OR、-OC(0)NRR、羰基、-S(0)nR8、-OS02R8、-S02NRR、或-NHC(0)R;m可以為0、1或2;n可以為0、1或2。R和R的定義如通式(I)化合物中所述,R可以為直鏈或支鏈的Cwo垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基;其中鹵素可以為氟、氯、溴或碘。
該發明所述的的有機硼酸為RB(OH)2,R可以為直鏈或支鏈的C^o垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基,例如甲基、乙基、丙基、丁基、苯基、對甲基苯基、對甲氧基苯基、對氯苯基等。
《用於合成卡帕芬淨的中間體及其製備方法》所述的的有機磺酸為RS03H,R可以為取代或非取代的直鏈或支鏈的垸基、直鏈或支鏈的C3-10烯基或C3-10炔基、取代或非取代的C3-8環垸基或取代或非取代的C6-10芳基或雜環芳基,例如甲基、三氟甲基、苯基、對甲基苯基等。
權利要求
1.一種如式(I)所示的用於合成卡帕芬淨的中間體,

其中,R'為C(=0)NH2,CN或CH2NRR;R為CN、CO2R、C(=0)NRR取代或非取代的苯基或萘基;R和R各自分別為氫或胺基保護基,所述胺基保護基選自Boc或Cbz;R為氫、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環烷基、取代或非取代的苯基或萘基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-10環烷基、取代或非取代的苯基或萘基;或R、R和氮原子一起形成5-8元雜環;R和R不能同時為胺基或甲氧基;
當苯基或萘基被取代時,取代基為一個或多個以下基團,獨立地選自鹵素、羥基、硝基、氰基。
2.根據權利要求1所述的如式(I)所示的用於合成卡帕芬淨的中間體,其中R、R和氮原子一起形成五元環或六元環。
3.根據權利要求1所述的用於合成卡帕芬淨的中間體,其中R為C(=0)NH2、CN或CH2NH2;R為CN、CO2H、CO2Me、CO2Et、CO2Bu、CO2Bu、CO2Ph、C(=0)NH2、C(=0)NMe2、C(=0)NHEt、C(=0)NHBu、C(=0)NHCH2CH2NH2、C(=0)NHcPr、C(=0)NHPr、C(=0)NHPen、C(=0)NHPh或苯基。
4.根據權利要求3所述的用於合成卡帕芬淨的中間體,其中R為CO2H、CO2Me、C(=0)NHCH2CH2NH2。
5.根據權利要求4所述的用於合成卡帕芬淨的中間體,其中R為CO2Me。
6.一種式(I)所示的用於合成卡帕芬淨的屮間體的製備方法,其特徵在於,將式(II)所示的中間體與式(III)所示的統基化合物反應製得式(I)所示的中間體: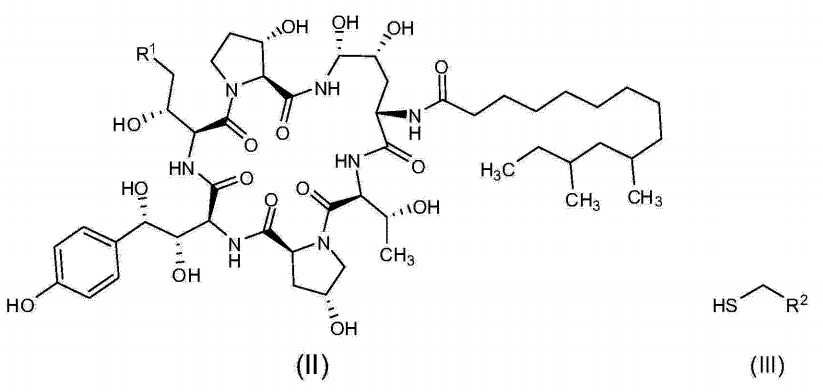

其中,R'為C(=0)NH2,CN或CH2NRR;R為CN、CO2R、C(=0)NRR取代或非取代的苯基或萘基;R和R各自分別為氫或胺基保護基,所述胺基保護基選自Boc或Cbz;R為氫、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環烷基、取代或非取代的苯基或萘基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-10環烷基、取代或非取代的苯基或萘基;或R、R和氮原子一起形成5-8元雜環;R和R不能同時為胺基或甲氧基;
當苯基或萘基被取代時,取代基為一個或多個以下基團,獨立地選自鹵素、羥基、硝基、氰基。
7.根據權利要求6所述的製備方法,其中R、R和氮原子一起形成五元環或六元環。
8.根據權利要求6所述的製備方法,其特徵在於,所述方法在有機硼酸和有機磺酸的作用下進行,所述的有機硼酸為RB(OH)2,R為苯基、對甲基苯基、對甲氧基苯基、對氯苯基、萘基;所述的有機磺酸為RSO3H,R為甲基、三氟甲基、苯基、對甲基苯基。
9.根據權利要求8所述的製備方法,其特徵在於,所述的有機硼酸為苯硼酸,所述的有機磺酸為三氟甲磺酸。
10.一種卡帕芬淨的製備方法,其特徵在於,所述方法包括將權利要求1的式(I)所示的用於合成卡帕芬淨的中間體與乙二胺反應的步驟,其中當式(I)所示的用於合成卡帕芬淨的中間體的R不為CH2NH2時,在與乙二胺反應前或反應後將R還原成CH2NH2或脫去胺基保護基

其中,R'為C(=0)NH2,CN或CH2NRR;R為CN、CO2R、C(=0)NRR取代或非取代的苯基或萘基;R和R各自分別為氫或胺基保護基,所述胺基保護基選自Boc或Cbz;R為氫、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環烷基、取代或非取代的苯基或萘基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-10環烷基、取代或非取代的苯基或萘基;或R、R和氮原子一起形成5-8元雜環;R和R不能同時為胺基或甲氧基;
當苯基或萘基被取代時,取代基為一個或多個以下基團,獨立地選自鹵素、羥基、硝基、氰基。
11.根據權利要求10所述的製備方法,其中R、R和氮原子一起形成五元環或六元環。
12.根據權利要求10所述的製備方法,所述的還原或脫去胺基保護基在如式(I)所示的用於合成卡帕芬淨的中間體與乙二胺反應之後進行。
13.根據權利要求10-12任意一項所述的製備方法,其特徵在於,所述方法還包括將式(II)所示的中間體與式(III)所示的統基化合物反應製得式(I)所示的中間體的步驟;

其中,R'為C(=0)NH2,CN或CH2NRR;R為CN、CO2R、C(=0)NRR取代或非取代的苯基或萘基;R和R各自分別為氫或胺基保護基,所述胺基保護基選自Boc或Cbz;R為氫、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-8環烷基、取代或非取代的苯基或萘基;R和R各自分別為氫、胺基、甲氧基、直鏈或支鏈的C1-10烷基、直鏈或支鏈的C3-10烯基或C3-10炔基、C3-10環烷基、取代或非取代的苯基或萘基;或R、R和氮原子一起形成5-8元雜環;R和R不能同時為胺基或甲氧基;當苯基或萘基被取代時,取代基為一個或多個以下基團,獨立地選自鹵素、羥基、硝基、氰基。
14.根據權利要求13所述的製備方法,其中R、R和氮原子一起形成五元環或六元環。
15.根據權利要求13所述的製備方法,其特徵在於,所述的式(II)所示的中間體與式(III)所示的統基化合物的反應步驟是在有機硼酸和有機磺酸的作用下進行的,所述的有機硼酸為RB(OH)2,R為苯基、對甲基苯基、對甲氧基苯基、對氯苯基、萘基;所述的有機磺酸為RSO3H,R為甲基、三氟甲基、苯基、對甲基苯基。
16.根據權利要求15所述的製備方法,其特徵在於,所述的有機硼酸為苯硼酸,所述的有機酸為三氟甲磺酸。
17.根據權利要求10-12任意一項所述的製備方法,其中R是CN。
18.根據權利要求10-12任意一項所述的製備方法,其中儼是C(=0)NH2。
19.根據權利要求10-12任意一項所述的製備方法,其中R是CH2NRR,R和R,各自分別為氫或胺基保護基,所述胺基保護基選自Boc或Cbz。
實施方式
下表為實施例中所涉及的式(I)所示的中間體的化合物編號: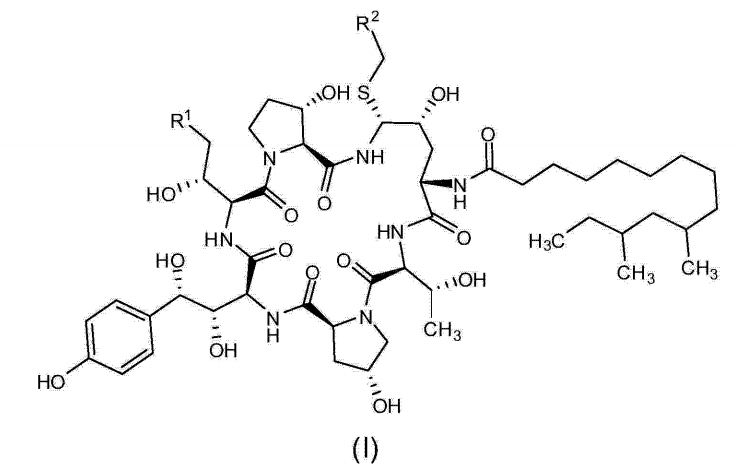

化合物編號 | R | R |
IA1 | CH2NH2 | CO2Me |
IA2 | CH2NH2 | C(=O)NHCH2CH2NH2 |
IA3 | CH2NH2 | C(=O)NMe2 |
IA4 | CH2NH2 | CN |
IB1 | CN | C(=O)NHEt |
IB2 | CN | C(=O)NMe2 |
IB3 | CN | CO2Me |
IB4 | CN | CO2Bu |
IB5 | CN | CO2H |
IB6 | CN | C(=O)NH2 |
IB7 | CN | C(=O)NHBu |
IB8 | CN | 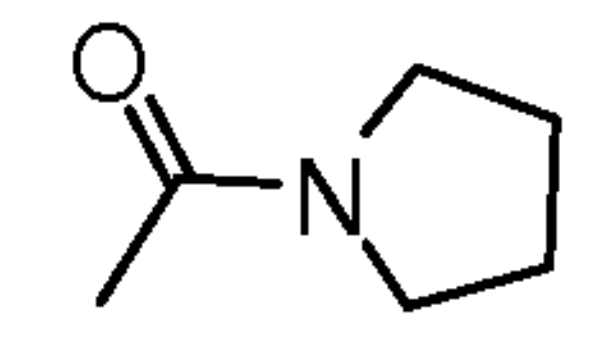 |
IC1 | C(=O)NH2 | CO2Me |
IC2 | C(=O)NH2 | CO2H |
IC3 | C(=O)NH2 | CO2Bu |
IC4 | C(=O)NH2 | CO2Bu |
IC5 | C(=O)NH2 | CO2Pen |
IC6 | C(=O)NH2 | CO2Ph |
IC7 | C(=O)NH2 | C(=O)NH2 |
IC8 | C(=O)NH2 | C(=O)NMe2 |
IC9 | C(=O)NH2 | C(=O)NHEt |
IC10 | C(=O)NH2 | C(=O)NHBu |
IC11 | C(=O)NH2 | 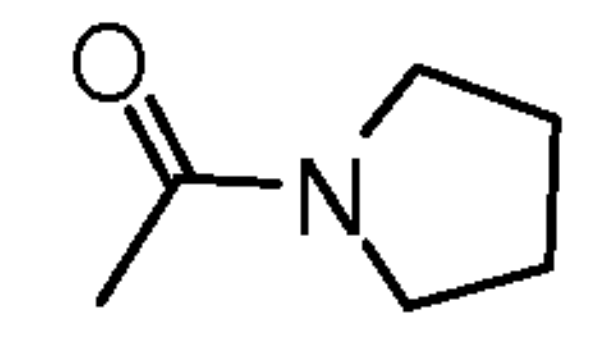 |
IC12 | C(=O)NH2 | C(=O)NHPr |
IC13 | C(=O)NH2 | C(=O)NHPen |
IC14 | C(=O)NH2 | C(=O)NHPr |
IC15 | C(=O)NH2 | C(=O)NHPh |
IC16 | C(=O)NH2 | Ph |
Bu=特丁基;Pr=異丙基;Pr=環丙基;Pen=環戊基。
實施例1:製備化合物IA1
將3克化合物IIA(按文獻US5378804類似方法製備),0.72克苯硼酸加到三口玻璃燒瓶中,加入120毫升乙腈,攪拌得到懸濁液。將懸濁液溫度降到-20°C,加入1克巰基乙酸甲酯,攪拌30分鐘,在-20°C慢慢滴加入1.2克三氟甲磺酸,反應液繼續在-20°C攪拌反應5-6小時,加入乙酸鈉的水溶液,攪拌1-2小時後,過濾,濾餅用乙腈水溶液洗滌,抽乾得到2.8克白色固體產品IA1。
H-NMR(CD30D,400MHz):7.09(d,2H),6.74(d,2H),5.24(d,1H),5.04(d,1H),4.90(d,1H)4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),3.63(s,3H),3.04(t,2H),2.42(dd,1H),2.15-1.99(m,7H),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03Cm),0.91(dt,1H),0.87(d,3H),0.85(d,6H)
MS:1139.61(M+H)
實施例2:製備化合物IA2
將3克化合物IIA,0.72克苯硼酸加到三口玻璃燒瓶中,加入120毫升乙腈,攪拌得到懸濁液。將懸濁液溫度降到-20°C,加入1.26克N-(2-胺基乙基:)巰基乙醯胺,攪拌30分鐘,在-20°C慢慢滴加入1.2克三氟甲磺酸,反應液繼續在-20°C攪拌反應5-6小時,加入乙酸鈉的水溶液,攪拌1-2小時後,過濾,濾餅用乙腈水溶液洗滌,抽乾得到3.1克白色固體產品IA2。
MS:1167.39(M+H)
實施例3:製備化合物IA3
將3克化合物IIA,0.72克苯硼酸加到三口玻璃燒瓶中,加入120毫升乙腈,攪拌得到懸濁液。將懸濁液溫度降到-20°C,加入l.1克N,N-二甲基巰基乙醯胺,攪拌30分鐘,在-20°C慢慢滴加入1.2克三氟甲磺酸,反應液繼續在-20°C攪拌反應5-6小時,加入乙酸鈉的水溶液,攪拌1-2小時後,過濾,濾餅用乙腈水溶液洗滌,抽乾得到3.1克白色固體產品
MS:1152.81(M+H)
實施例4:製備化合物IA4
將3克化合物IIA,0.72克苯硼酸加到三口玻璃燒瓶中,加入120毫升乙腈,攪拌得到懸濁液。將懸濁液溫度降到-20°C,加入1.5克巰基乙腈,攪拌30分鐘,在-20°C慢慢滴加入1.2克三氟甲磺酸,反應液繼續在-20°C攪拌反應5-6小時,加入乙酸鈉的水溶液,攪拌1-2小時後,過濾,濾餅用乙腈水溶液洗滌,抽乾得到3.0克白色固體產品IA4。
H-NMR(CD30D,400MHz):7.15(d,2H),6.79(d,2H),5.34(d,IH),5.04(d,IH),4.64(m,3H)4.53-4.42(m,4H),4.43-4.32(m,3H),4.31-4.25(m,5H),4.23-4.18(m,IH),3.99-3.95(m,lH),3.90-3.8(m,3H),3.73-3.65(m,2H),3.58-3.65(m,2H),3.05-3.18(m,2H),2.40-2.50(m,IH),2.35-2.23(m,4H),2.21-1.98(m,6H),1.97-1.80(m,3H),1.78-1.60(m:2H),1.58-1.41(m,2H),1.40-1.26(m,14H),1.21(d,3H),1.20-1.13(m,3H),0.95-0.85(m,10H),0.68-0.76(dd,2H)
MS:1106.54(M+H)
實施例5:製備化合物IB1
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物IIB(按文獻US5378804類似方法製備),35毫克苯硼酸和68毫克N-乙基2-巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB1。
H-NMR(CD30D,400MHz):7.08(d,2H),6.70(d,2H),5.21(d,IH),4.99(d,IH),4.95(d,IH),4.56-4.47(m,3H),4.39-4.21(m,6H),3.99-3.95(m,IH),3.87-3.83(m,IH),3.80-3.75(m,2H),2.95—2.90(q;2H),2.80-2.64(m,2H),2.46(m,IH),2.42(m,3H),2.26-2.12(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20Cm),1.14(d),1.12-1.03(m),0.91(dt,IH),0.87(m),0.81(m)MS:1148.48(M+H)
實施例6:製備化合物IB2
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物IIB,35毫克苯硼酸和68毫克Ν,Ν-二甲基-2-巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB2。
H-NMR(CD30D,400MHz):7.08(d,2H),6.70(d,2H),5.27(d,IH),4.99(d,IH),4.95(d,IH),4.56-4.47(m,3H),4.39-4.21(m,6H),3.99-3.95(m,IH),3.87-3.83(m,IH),3.80-3.75(m,2H),3.04(s,3H),2.89(s,3H),2.80-2.64(m,2H),2.46(m,IH),2.42(m,3H),2.26-2.12(m)2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20Cm),1.14(d),1.12-1.03(m),0.91(dt,IH),0.87(m),0.81(m)MS:1148.48(M+H)
實施例7:製備化合物IB3
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物IIB,35毫克苯硼酸和61毫克巰基乙酸甲酯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB3。
H-NMR(CD30D,400MHz):7.09(d,2H),6.69(d,2H),5.28(d,1H),4.99(d,1H),4.90(d,1H),4.56-4.47(m,3H),4.39-4.21(m,6H),3.99-3.95(m,1H),3.87-3.83(m,1H),3.80-3.75(m,2H),3.66(,3H),3.56-3.52(dd,lH),3.49-3.39(dd,lH),2.80-2.64(m,2H),2.46(m,1H),2.42(m,3H),2.26-2.12(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,1H),0.87(m),0.81(m)
MS:1135.38(M+H)
實施例8:製備化合物IB4
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物IIB,35毫克苯硼酸和85毫克巰基乙酸丁酯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB4。
H-NMR(CD30D,400MHz):7.08(d,2H),6.70(d,2H),5.29(d,1H),4.99(d,1H),4.95(d,1H),4.56-4.47(m,3H),4.39-4.21(m,6H),3.99-3.95(m,1H),3.87-3.83(m,1H),3.80-3.75(m,2H),3.58〜3.56(t;2H),3.56-3.52(dd,lH),3.49-3.39(dd,lH),2.80-2.64(m,2H),2.46(m,1H),2.42Cm,3H),2.26-2.12(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,1H),0.87(m),0.81(m)
MS:1178.49(M+H)
實施例9:製備化合物IB5
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物IIB,35毫克苯硼酸和60毫克巰基乙酸得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB5。
MS:1121.16(M+H)
實施例10:製備化合物IB6
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物
IIB,35毫克苯硼酸和62毫克巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB6。
MS:1120.44(M+H)
實施例11:製備化合物IB7
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物IIB,35毫克苯硼酸和86毫克N-丁基-2-巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB7。
MS:1176.51(M+H)
實施例12:製備化合物IB8
氮氣保護下,在反應瓶中的8毫升無水乙腈中加入100毫克化合物IIB:35毫克苯硼酸和86毫克巰基乙醯吡咯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(57.3毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,濾餅用乙腈/水洗滌。收集濾餅,乾燥得到產品IB8。
MS:1174.58(M+H)
實施例13:製備化合物IC1
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC(PB0,通過微生物發酵製得),172毫克苯硼酸和299毫克巰基乙酸甲酯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC1。
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.29(d,1H),5.1(d,1H),4.99(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),3.63(s,3H),3.55-3.51(dd,lH),3.36-3.40(dd,lH),2.88(dd,1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,1H),0.87(d,3H),0.85(d,6H)
MS:1153.26(M+H)
實施例14:製備化合物IC2
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和259毫克巰基乙酸得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),2.88(dd1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03Cm),0.91(dt,1H),0.87(d,3H),0.85(d,6H)
MS:1139.18(M+H)
實施例15:製備化合物IC3
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和417毫克巰基乙酸丁酯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品
MS:1195.48(M+H)
實施例16:製備化合物IC4
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和417毫克巰基乙酸特丁酯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC4。
MS:1195.48(M+H)
實施例17:製備化合物IC5
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和431毫克巰基乙酸環戊酯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC5。
MS:1207.49(M+H)
實施例18:製備化合物IC6
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和431毫克巰基乙酸苯酯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品MS:1215.48(M+H)
實施例19:製備化合物IC7
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和259毫克巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),2.88(dd1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03Cm),0.91(dt,1H),0.87(d,3H),0.85(d,6H)
MS:1138.45(M+H)
實施例20:製備化合物IC8
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和336毫克N,N-二甲基巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC8。
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25Cm),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),3.01(s,1H),2.88(s,1H),2.68(dd,1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,1H),0.87(d,3H),0.85(d,6H)MS:1166.52(M+H)
實施例21:製備化合物IC9
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和259毫克N,N-二甲基巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC9。
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,
1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),2.88(dd,2H),2.68(dd,1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,1H),0.87(d,3H),0.85(d,6H)
MS:1166.52(M+H)
實施例22:製備化合物IC10
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和414毫克N,N-二甲基巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC10。
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,
1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),2.94-2.91(t,2H),2.68(dd,1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20Cm),1.14(d),1.12-1.03(m),0.91(dt,2H),0.87(d,6H),0.85(d,6H)
MS:1194.53(M+H)
實施例23:製備化合物IC11
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和410毫克巰基乙醯吡咯得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC11。
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),3.18-3.14(m,4H),2.68(dd,1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.94-1.90(m,4H),1.87-1.85(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,2H),0.87(d,3H),0.85(d,6H)
MS:1192.56(M+H)
實施例24:製備化合物IC12
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和370毫克N-環丙基巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC12。
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,
1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),3.21-3.09(dd,1H),2.68(dd,1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.87-1.85(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20Cm),1.14(d),1.12-1.03(m),0.91(dt,2H),0.87(d,3H),0.85(d,6H)0.68〜0.50(m,4H)
MS:1178.46(M+H)
實施例25:製備化合物IC13
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和450毫克N-環戊基巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC13。
H-NMR(CD30D,400MHz):7.09(d,2H),6.70(d,2H),5.24(d,1H),5.04(d,1H),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),3.21-3.09(dd,1H),2.68(dd,1H),2.46(dd,1H),2.42(dd,1H),2.26-2.18(m),2.10-2.03(m),1.94-1.90(m,4H),1.87-1.85(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,2H),0.89〜0.85(m,15H)
MS:1206.50(M+H)
實施例26:製備化合物IC14
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和370毫克N-異丙基巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC14。
MS:1180.50(M+H)
實施例27:製備化合物IC15
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和370毫克N-苯基巰基乙醯胺得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC15。
MS:1214.65(M+H)
實施例28:製備化合物IC16
氮氣保護下,在反應瓶中的30毫升無水乙腈中加入500毫克化合物IIC,172毫克苯硼酸和350毫克苄硫醇得到懸浮液。將懸浮液冷卻至-15°C。將三氟甲磺酸(282毫克)的乙腈溶液滴加到反應瓶中,維持溫度在-15°C攪拌4-6小時,反應結束。加入乙酸鈉的水溶液,攪拌1-2小時。加入90毫升水,攪拌1小時。過濾,收集濾餅,乾燥得到產品IC16。
H-NMR(CD30D,400MHz):7.30-7.27(d,2H),7.24-7.2(t,3H),7.17-7.15(d,lH),7.09(d,2H),6.70(d,2H),5.24(d,IH),5.04(d,IH),4.90(d,1H),4.56-4.47(m),4.39-4.35(m,2H),4.31-4.25(m),4.23-4.21(m,3H),3.99-3.95(m),3.80-3.75(m),3.63(s,3H),3.55-3.51(dd,lH),3.36-3.40(dd,lH),2.88(dd,IH),2.46(dd,IH),2.42(dd,IH),2.26-2.18(m),2.10-2.03(m),1.97-1.90(m),1.63-1.52(m),1.51-1.46(m),1.45-1.39(m),1.38-1.20(m),1.14(d),1.12-1.03(m),0.91(dt,IH),0.87(d,3H),0.85(d,6H)
MS:1171.10(M+H)
實施例29:製備卡帕芬淨
將70毫克化合物IA1在15°C溶於0.5毫升甲醇中,在5°C下加入0.7毫升乙二胺得到反應液。將反應液加熱到40°C,攪拌反應20小時,減壓濃縮除去甲醇,加入乙腈,攪拌,氮氣保護下過濾,抽乾,得固體粗產品,用C-18矽膠柱純化,蒸乾溶劑得到最終產品-卡帕芬淨。
MS:1093.21(M+H)
實施例30:製備卡帕芬淨
步驟1):將800毫克化合物IB1加到三口玻璃燒瓶中,加入20毫升甲醇,攪拌。將反應瓶內溫度調節到30°C,加入20毫升乙二胺,攪拌18小時得到反應液,將反應液濃縮,加入40毫升乙腈,攪拌20-30分鐘。過濾,收集濾餅,乾燥得到產品IVB。MS:1089.22(M+H)
步驟2):將100毫克化合物IVB溶於9毫升乙醇和l毫升水中,加入l毫升醋酸和50毫克10%Pd/C,在3atm氫氣壓力和20°C下攪拌10小時。過濾除去催化劑,蒸乾溶劑,加入20毫升水,用乙酸乙酯(10毫升×2)提取,收集水層,冷凍乾燥,得到卡帕芬淨粗產品,用C-18矽膠柱純化,蒸乾溶劑得到最終產品-卡帕芬淨。
MS:1093.21(M+H)
實施例31:製備卡帕芬淨
步驟1):將800毫克化合物IC1加到三口玻璃燒瓶中,加入20毫升甲醇,攪拌。將反應瓶內溫度調節到30°C,加入20毫升乙二胺,攪拌18小時得到反應液,將反應液濃縮,加入40毫升乙腈,攪拌20-30分鐘。過濾,收集濾餅,乾燥得到產品IVC。
MS:1107.29(M+H)
步驟2):將100毫克化合物IVC加到三口玻璃燒瓶中,加入20毫升無水THF,攪拌。氮氣保護下,加入33毫克苯硼酸,攪拌過夜。降溫到10°C,加入140毫克雙(三甲基矽垸基)三氟乙醯胺,攪拌3小時。降溫到-15°C。加入1.35毫升1.0M硼垸的THF溶液。在-15°C攪拌6小時,用2毫升的2N的鹽酸淬滅,加入20毫升水,分出水層,水層用乙酸乙酯(10毫升x2)提取,收集水層,冷凍乾燥,得到卡帕芬淨粗產品,用C-18矽膠柱純化,蒸乾溶劑得到最終產品-卡帕芬淨。
MS:1093.21(M+H)
榮譽表彰
2019年7月15日,《用於合成卡帕芬淨的中間體及其製備方法》獲第十一屆江蘇省專利項目獎優秀獎。

