過渡金屬催化的不對稱烯丙基烷基化反應(asymmetric allylic alkylation,簡稱為AAA反應)是構建手性分子重要的方法之一。該類反應在實現醛、酮、1,3-二羰基化合物的不對稱轉化中發揮著重要作用。
基本介紹
- 中文名:烯丙型遷移
- 外文名:asymmetric allylic alkylation
- 別稱:AAA反應
- 意義:構建手性分子重要的方法
- 領域:有機合成
反應機理,烯丙基化反應的立體選擇性,現狀與發展,
反應機理
1994年,chan等人提出了金屬催化烯丙基化反應可能的機理。他認為該反應是一個單電子轉移的反應。
然而對於烯丙基化錮中間過渡產物的性質卻所知甚少,這是由於有機銦化合物極易被水解。Whitesidess,Arkai和chan等人曾對有機錮過渡態化合物做了一些探索並取得了一些進展,但對於這類化合物在反應中存在的確切結構及其性質還不是非常明確,有待於進一步的研究。
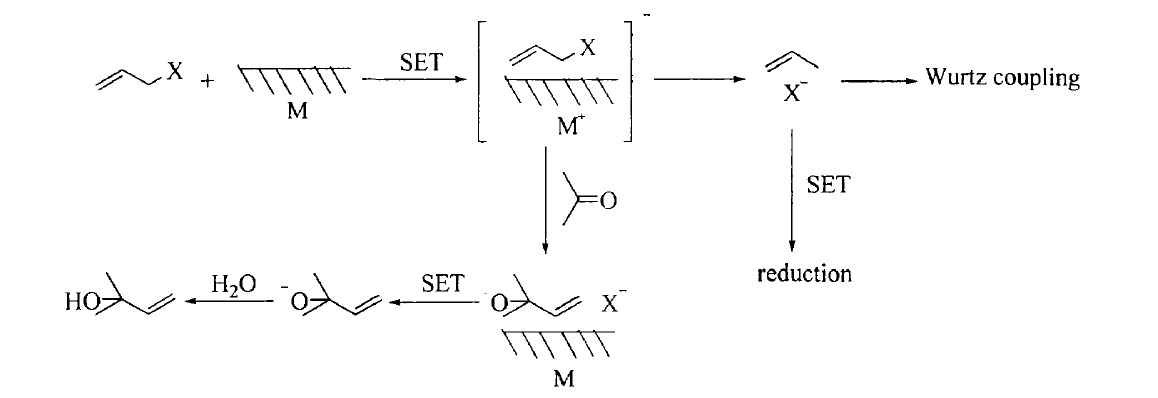 可能的反應機理
可能的反應機理烯丙基化反應的立體選擇性
在銦催化的烯丙基化反應中,如果使用簡單的醛作為反應底物,則其產物以反式結構產物為主,並且其反式產物的比例隨著醛的R基團的增大而增加。這個結果可以通過反應中所形成的六元環狀的中間過渡態來解釋。
L.A.Paquett和Mori等人對銦催化的烯丙基化反應的立體選擇性作了更進一步的研究,他們發現當使用α-或β-羥基醛做為反應底物,在水相介質中,其烯丙基化產物的立體結構主要由水相中羥基和銦通過鰲合作用所形成的鰲合物中間過渡態決定。α-羥基醛在上述條件下發生烯丙基化反應時主要以順式的產物為主,而β-羥基醛則以反式產物為主。但值得注意的是,當α-或β-羥基被保護時,隨著保護基團的增大,其鰲合作用則越弱,反應的立體選擇性也就越不明顯。
現狀與發展
目前AAA反應主要面臨著兩個挑戰:
(1)如何將親核試劑拓展到α-H酸性較弱的羧酸衍生物;
(2)如何在非環體系中構建季碳手性中心。
實現該類反應的關鍵是構建立體構型確定的四取代烯醇化物及其羧酸氧化態的等價體。
Evans等人從α-二取代的腈類化合物出發,通過形成N-鋰化的前手性陰離子作為羧酸衍生烯醇化物的等價體實現了AAA反應。侯雪龍等人從包含二苯基胺的醯胺出發,經由四取代的烯醇化物實現了AAA過程。Stoltz和Marek等人從炔基氨基甲酸酯類化合物出發,經順式的碳金屬化、氧化以及O-烯丙氧基羰基化生成四取代的O-烯丙氧基羰基烯醇化物,隨後經羥基保護、鈀催化的脫羧AAA反應生成醯胺α位烯丙基化的產物。儘管目前該領域已經取得了不少的進展,但仍然面臨著官能團兼容性較差以及原子經濟性不高等局限。

