雷貝拉唑鈉腸溶膠囊,本品適用於:1、活動性十二指腸潰瘍;2、良性活動性胃潰瘍;3、伴有臨床症狀的侵蝕性或潰瘍性的胃-食管返流徵(GERD);4、與適當的抗生素合用,可根治幽門螺旋桿菌陽性的十二指腸潰瘍;5、侵蝕性或潰瘍性胃-食管返流徵的維持期治療。目前療程超過12個月的藥效尚未進行評估。
基本介紹
- 藥品名稱:雷貝拉唑鈉腸溶膠囊
- 藥品類型:工傷醫保乙類雙跨
- 用途分類:抑制胃酸分泌藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,
成份
雷貝拉唑鈉
化學名稱:2-[[[4-(3-甲氧基丙氧基)-3-甲基-2-吡啶基]-甲基]亞磺醯基]-1H-苯並咪唑鈉
化學結構式:
化學名稱:2-[[[4-(3-甲氧基丙氧基)-3-甲基-2-吡啶基]-甲基]亞磺醯基]-1H-苯並咪唑鈉
化學結構式:
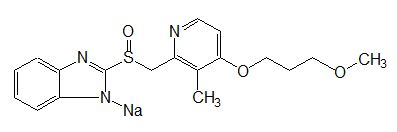
分子式:C18H20N3NaO3S
分子量:381.43

性狀
本品為腸溶膠囊,內容物為類白色或淡黃色粉末。
適應症
本品適用於:
1、活動性十二指腸潰瘍;
2、良性活動性胃潰瘍;
3、伴有臨床症狀的侵蝕性或潰瘍性的胃-食管返流徵(GERD);
4、與適當的抗生素合用,可根治幽門螺旋桿菌陽性的十二指腸潰瘍;
5、侵蝕性或潰瘍性胃-食管返流徵的維持期治療。目前療程超過12個月的藥效尚未進行評估。
1、活動性十二指腸潰瘍;
2、良性活動性胃潰瘍;
3、伴有臨床症狀的侵蝕性或潰瘍性的胃-食管返流徵(GERD);
4、與適當的抗生素合用,可根治幽門螺旋桿菌陽性的十二指腸潰瘍;
5、侵蝕性或潰瘍性胃-食管返流徵的維持期治療。目前療程超過12個月的藥效尚未進行評估。
規格
(1)20mg (2)10mg
用法用量
本品不能咀嚼或壓碎服用,應整粒吞服。
1、成年人/老年患者的用藥
A、活動性十二指腸潰瘍和良性活動性胃潰瘍患者:20mg,1次/日,晨服。
大多數活動性十二指腸潰瘍患者在用藥4周后痊癒。但有2%的患者還需要繼續用藥4周才能達痊癒。
一些十二指腸潰瘍患者對晨服10mg,1次/日的治療量即有反應。
大多數良性活動性胃潰瘍需在用藥6周后痊癒。但有9%的患者還需繼續用藥6周才可達痊癒。
B、侵蝕性或潰瘍性的胃-食管返流徵(GERD)患者:20mg,1次/日,療程為4-8周。
C、胃-食管返流徵(GERD)的長期治療方案的維持治療:療程為12個月,維持治療量為10mg或20mg,1次/日。一些患者對10mg/日的維持治療量即有反應。
D、幽門螺旋桿菌的根治性治療:
與適當的抗生素合用,可用於根治幽門螺旋桿菌陽性的十二指腸潰瘍。
本品應在早晨、餐前服用,儘管用藥時間及攝食對雷貝拉唑鈉藥效無影響,但此種給藥方式更有利於治療的進行。
2、肝腎功能不全患者的用藥
肝腎功能不全患者在用藥過程中無需進行劑量調節。但在對有嚴重的肝功能不全患者用藥時,應參見“不良反應及注意事項”。
1、成年人/老年患者的用藥
A、活動性十二指腸潰瘍和良性活動性胃潰瘍患者:20mg,1次/日,晨服。
大多數活動性十二指腸潰瘍患者在用藥4周后痊癒。但有2%的患者還需要繼續用藥4周才能達痊癒。
一些十二指腸潰瘍患者對晨服10mg,1次/日的治療量即有反應。
大多數良性活動性胃潰瘍需在用藥6周后痊癒。但有9%的患者還需繼續用藥6周才可達痊癒。
B、侵蝕性或潰瘍性的胃-食管返流徵(GERD)患者:20mg,1次/日,療程為4-8周。
C、胃-食管返流徵(GERD)的長期治療方案的維持治療:療程為12個月,維持治療量為10mg或20mg,1次/日。一些患者對10mg/日的維持治療量即有反應。
D、幽門螺旋桿菌的根治性治療:
與適當的抗生素合用,可用於根治幽門螺旋桿菌陽性的十二指腸潰瘍。
本品應在早晨、餐前服用,儘管用藥時間及攝食對雷貝拉唑鈉藥效無影響,但此種給藥方式更有利於治療的進行。
2、肝腎功能不全患者的用藥
肝腎功能不全患者在用藥過程中無需進行劑量調節。但在對有嚴重的肝功能不全患者用藥時,應參見“不良反應及注意事項”。
不良反應
1、偶見(不良反應發生率在0.1~5%):光敏性反應、頭痛、噁心、嘔吐、便秘、腹瀉、皮疹;紅細胞減少、白細胞減少、白細胞增多、嗜酸性粒細胞增多、嗜中性粒細胞增多、淋巴細胞減少;ALT、AST、ALP、γ-GTP、LDH、總膽紅素、總膽固醇、BUN升高;蛋白尿等不良反應。
2、罕見(不良反應發生率<0.1%)休克、心悸、心動過緩、消化不良、胸痛、肌痛、視力障礙、失眠、睏倦、握力低下、口齒不清、步態蹣跚、溶血性貧血等。
2、罕見(不良反應發生率<0.1%)休克、心悸、心動過緩、消化不良、胸痛、肌痛、視力障礙、失眠、睏倦、握力低下、口齒不清、步態蹣跚、溶血性貧血等。
禁忌
對雷貝拉唑鈉、苯並咪唑替代品或對該製劑製備中使用的任何賦形劑過敏的患者禁用。
注意事項
1、用本品開始治療之前應排除存在癌症的可能性。儘管在年齡和性別匹配的輕中度肝臟損傷患者與正常者的對照研究中,未見到明顯與藥物相關的安全問題,但是重度肝損傷患者初次使用本品治療時,醫生建議要特別注意。
2、服用本品時,應定期進行血液檢查及血液生化學(如肝酶檢查),發現異常,即停止用藥,並進行及時處理。
3、肝功能損傷的患者慎用。
4、如果患者長期服用質子泵抑制劑,在用藥過程中,要注意可能出現的骨折風險(尤其是老年患者),定期監測血鎂水平,防止低鎂血症的出現。
5、由於質子泵抑制劑與氯吡格雷存在相互作用,建議正在使用氯吡格雷類的患者在治療前,與醫生就用藥安全性問題進行交流,以確保用藥安全。
6、藥物不要放在孩童可觸及的地方。
7、廢棄藥品包裝不應隨意丟棄。
2、服用本品時,應定期進行血液檢查及血液生化學(如肝酶檢查),發現異常,即停止用藥,並進行及時處理。
3、肝功能損傷的患者慎用。
4、如果患者長期服用質子泵抑制劑,在用藥過程中,要注意可能出現的骨折風險(尤其是老年患者),定期監測血鎂水平,防止低鎂血症的出現。
5、由於質子泵抑制劑與氯吡格雷存在相互作用,建議正在使用氯吡格雷類的患者在治療前,與醫生就用藥安全性問題進行交流,以確保用藥安全。
6、藥物不要放在孩童可觸及的地方。
7、廢棄藥品包裝不應隨意丟棄。
孕婦及哺乳期婦女用藥
1、對於孕婦或有可能妊娠的婦女,只有在其治療有益性大於危險性的前提下方可使用。
2、本品可能通過乳汁分泌,故避免用於哺乳期婦女,不得已而必須用藥時,則應暫停給嬰兒哺乳。
2、本品可能通過乳汁分泌,故避免用於哺乳期婦女,不得已而必須用藥時,則應暫停給嬰兒哺乳。
兒童用藥
目前尚無兒童服用本品的安全性和有效性資料。
老年用藥
臨床研究表明,未見65歲以上患者與年青患者在療效與安全性方面有差異,但不排除某些老年患者的敏感性更強。由於本藥主要在肝臟代謝,而老年患者肝功能低下者居多,有時可出現不良反應。因此,當出現消化系統不良反應(參照“不良反應”項)時,應謹慎給予,必要時應停止用藥。
藥物相互作用
雷貝拉唑通過細胞色素P450(CYP450)代謝酶系統進行代謝。健康試驗者研究表明,雷貝拉唑鈉臨床上沒有明顯的與其他的通過CYP450系統代謝的藥物有相互作用。
雷貝拉唑鈉能夠產生持續性的抑制胃酸分泌的作用。由於雷貝拉唑鈉使酸度下降,因此,與那些吸收與胃pH值有關的藥物有相互作用。例如,正常受試者如果每天同時服用酮康唑與20mg雷貝拉唑鈉,會使酮康唑的生物利用度減少大約30%;同時服用地高辛,會使地高辛的AUC和Cmax值分別增加19%和29%。因此,病人在同時服用上述藥物和雷貝拉唑鈉時應進行監測。雷貝拉唑鈉與抗酸劑同時服用以及在服用抗酸劑1小時後再服用時,雷貝拉唑的平均血漿中濃度曲線下面積分別下降8%和6%。
雷貝拉唑鈉能夠產生持續性的抑制胃酸分泌的作用。由於雷貝拉唑鈉使酸度下降,因此,與那些吸收與胃pH值有關的藥物有相互作用。例如,正常受試者如果每天同時服用酮康唑與20mg雷貝拉唑鈉,會使酮康唑的生物利用度減少大約30%;同時服用地高辛,會使地高辛的AUC和Cmax值分別增加19%和29%。因此,病人在同時服用上述藥物和雷貝拉唑鈉時應進行監測。雷貝拉唑鈉與抗酸劑同時服用以及在服用抗酸劑1小時後再服用時,雷貝拉唑的平均血漿中濃度曲線下面積分別下降8%和6%。
藥物過量
無已知的特效解毒劑。
服用本品過量時,應按患者的臨床症狀和體徵,採用適當的支持療法。
服用本品過量時,應按患者的臨床症狀和體徵,採用適當的支持療法。
藥理毒理
藥理作用
雷貝拉唑為苯並咪唑類化合物,是第二代質子泵抑制劑,通過特異性地抑制胃壁細胞H+-K+-ATP酶系統而阻斷胃酸分泌的最後步驟。該作用呈劑量依賴性,並可使基礎胃酸分泌和刺激狀態下的胃酸分泌均受抑制。本品對膽鹼和組胺H2受體無拮抗作用。
毒理研究
遺傳毒性:本品鼠傷寒沙門氏菌回復突變(Ames)試驗、中國倉鼠卵細胞基因突變試驗、小鼠淋巴瘤細胞基因突變試驗結果均呈陽性;其去甲基代謝物在試驗中也呈陽性;本品體外倉鼠肺細胞染色體畸變試驗、小鼠微核試驗和體內、體外肝程式外DNA合成(UDS)試驗結果均為陰性。
生殖毒性:大鼠靜脈給予雷貝拉唑50mg/kg/天(血漿AUC約為患者臨床推薦劑量時的13倍)和兔靜脈給予本品50mg/kg/天(血漿AUC約為患者臨床推薦劑量時的8倍),其生育力和生殖行為未見明顯異常,對動物胎仔未見損傷。尚無懷孕婦女給藥的充分和嚴格對照的臨床研究,由於動物生殖毒性並不總能預測藥物對人體的影響,故懷孕期間僅在確實需要時才能使用本品。
大鼠在妊娠後期和哺乳期經口給予雷貝拉唑400mg/kg/天,可導致動物體重增長減慢。由於許多藥物可經乳汁分泌,且可能對哺乳嬰兒產生毒副作用,故應考慮藥物對母親的重要性,決定在此期間是否停止哺乳還是停止用藥。
致癌性:採用CD-1小鼠進行88/104周試驗,雷貝拉唑經口給藥劑量高達100mg/kg/天時未表現出腫瘤發生率增加,此時血藥濃度為患者推薦劑量下的1.6倍。採用SD大鼠進行了給藥104周的致癌性試驗研究,其中雄性大鼠口服劑量5,15,30,60mg/kg/天,雌性大鼠口服劑量5,15,30,60和120mg/kg/天,結果所有劑量組雌、雄動物均出現胃腸嗜鉻細胞樣(ELC)增生,雌性動物所有劑量組都出現胃腸嗜鉻細胞樣(ELC)良性腫瘤。雄性動物即使在最高劑量組(血藥濃度相當於臨床推薦劑量下的0.2倍)下,也未見與藥物有關的腫瘤產生。
雷貝拉唑為苯並咪唑類化合物,是第二代質子泵抑制劑,通過特異性地抑制胃壁細胞H+-K+-ATP酶系統而阻斷胃酸分泌的最後步驟。該作用呈劑量依賴性,並可使基礎胃酸分泌和刺激狀態下的胃酸分泌均受抑制。本品對膽鹼和組胺H2受體無拮抗作用。
毒理研究
遺傳毒性:本品鼠傷寒沙門氏菌回復突變(Ames)試驗、中國倉鼠卵細胞基因突變試驗、小鼠淋巴瘤細胞基因突變試驗結果均呈陽性;其去甲基代謝物在試驗中也呈陽性;本品體外倉鼠肺細胞染色體畸變試驗、小鼠微核試驗和體內、體外肝程式外DNA合成(UDS)試驗結果均為陰性。
生殖毒性:大鼠靜脈給予雷貝拉唑50mg/kg/天(血漿AUC約為患者臨床推薦劑量時的13倍)和兔靜脈給予本品50mg/kg/天(血漿AUC約為患者臨床推薦劑量時的8倍),其生育力和生殖行為未見明顯異常,對動物胎仔未見損傷。尚無懷孕婦女給藥的充分和嚴格對照的臨床研究,由於動物生殖毒性並不總能預測藥物對人體的影響,故懷孕期間僅在確實需要時才能使用本品。
大鼠在妊娠後期和哺乳期經口給予雷貝拉唑400mg/kg/天,可導致動物體重增長減慢。由於許多藥物可經乳汁分泌,且可能對哺乳嬰兒產生毒副作用,故應考慮藥物對母親的重要性,決定在此期間是否停止哺乳還是停止用藥。
致癌性:採用CD-1小鼠進行88/104周試驗,雷貝拉唑經口給藥劑量高達100mg/kg/天時未表現出腫瘤發生率增加,此時血藥濃度為患者推薦劑量下的1.6倍。採用SD大鼠進行了給藥104周的致癌性試驗研究,其中雄性大鼠口服劑量5,15,30,60mg/kg/天,雌性大鼠口服劑量5,15,30,60和120mg/kg/天,結果所有劑量組雌、雄動物均出現胃腸嗜鉻細胞樣(ELC)增生,雌性動物所有劑量組都出現胃腸嗜鉻細胞樣(ELC)良性腫瘤。雄性動物即使在最高劑量組(血藥濃度相當於臨床推薦劑量下的0.2倍)下,也未見與藥物有關的腫瘤產生。
藥代動力學
據國外文獻報導:該藥是經胃後在腸道內才開始被吸收的。在20mg劑量組,在用藥後3.5小時達到血藥濃度峰值。在10mg~ 40mg 劑量範圍內,血藥濃度峰值和曲線下面積與劑量呈線性關係。口服20mg劑量組的絕對生物利用度約為52%。重複用藥後生物利用度不升高。健康受試者的藥物半衰期約為1小時(在0.7~1.5範圍內),體內藥物清除率為283±98ml/min。在慢性肝病患者體內,血藥濃度的曲線下面積提高2-3倍。
雷貝拉唑鈉的血漿蛋白結合率為97%,主要的代謝產物為硫醚(M1)和羧酸(M6)。次要代謝物還有碸(M2)、乙基硫醚(M4)和硫醚氨酸(M5)。只有乙基代謝物(M3)具有少量抑制分泌的活性,但不存在於血漿中。該藥90%主要隨尿排出,其他代謝物隨糞便排出。在需要血液透析的晚期穩定的腎衰患者體內(肌酐清除率≤5ml/min/1.73m2 ),雷貝拉唑鈉的分布與在健康受試者體內的分布相似。此藥用於老年患者時,藥物清除率有所降低。當老年患者用雷貝拉唑鈉20mg,1次/日,連續7天,出現血藥濃度的曲線下面積加倍,血藥濃度峰值相對於年輕健康受試者升高60%。另外,此藥在體內無累積現象。
雷貝拉唑鈉的血漿蛋白結合率為97%,主要的代謝產物為硫醚(M1)和羧酸(M6)。次要代謝物還有碸(M2)、乙基硫醚(M4)和硫醚氨酸(M5)。只有乙基代謝物(M3)具有少量抑制分泌的活性,但不存在於血漿中。該藥90%主要隨尿排出,其他代謝物隨糞便排出。在需要血液透析的晚期穩定的腎衰患者體內(肌酐清除率≤5ml/min/1.73m2 ),雷貝拉唑鈉的分布與在健康受試者體內的分布相似。此藥用於老年患者時,藥物清除率有所降低。當老年患者用雷貝拉唑鈉20mg,1次/日,連續7天,出現血藥濃度的曲線下面積加倍,血藥濃度峰值相對於年輕健康受試者升高60%。另外,此藥在體內無累積現象。
貯藏
密封,在陰涼乾燥處(不超過20℃)保存。
包裝
(1)包裝材料:藥用高密度聚乙烯瓶;包裝規格:每瓶7粒或每瓶14粒或每瓶28粒;
(2)包裝材料:鋁箔+藥用複合硬片;包裝規格:每板7粒,每盒1板或每盒2板或每盒4板。
(2)包裝材料:鋁箔+藥用複合硬片;包裝規格:每板7粒,每盒1板或每盒2板或每盒4板。
有效期
暫定24個月
執行標準
(1)20mg:國家食品藥品監督管理局標準(試行)YBH11022004;
(2)10mg:國家食品藥品監督管理局標準YBH34632005
(2)10mg:國家食品藥品監督管理局標準YBH34632005
