潘美路(注射用泮托拉唑鈉),適應症為適用於十二指腸潰瘍、胃潰瘍、急性胃黏膜病變、複合性胃潰瘍等所致急性上消化道出血。
基本介紹
- 藥品名稱:潘美路
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:抑制胃酸分泌藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,
成份
本品由一瓶凍乾粉和一支安瓿專用溶劑組成,活性成份為泮托拉唑鈉,專用溶劑為氯化鈉的等滲滅菌水溶液。
輔料:乳糖。
活性成份的化學名稱:5-二氟甲氧基-2-[[(3,4-二甲氧基-2-吡啶基)-甲基]亞磺醯基]-1H-苯並咪唑鈉一水合物。
其結構式為:
分子式:C16H14F2N3NaO4S·H2O
分子量:423.38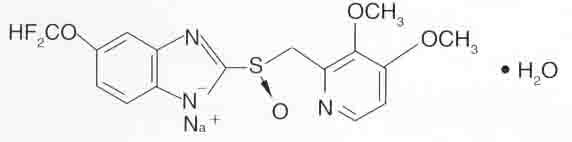
輔料:乳糖。
活性成份的化學名稱:5-二氟甲氧基-2-[[(3,4-二甲氧基-2-吡啶基)-甲基]亞磺醯基]-1H-苯並咪唑鈉一水合物。
其結構式為:
分子式:C16H14F2N3NaO4S·H2O
分子量:423.38

性狀
注射用泮托拉唑鈉為白色或類白色疏鬆塊或粉末,專用溶媒為無色的澄明液體。
適應症
適用於十二指腸潰瘍、胃潰瘍、急性胃黏膜病變、複合性胃潰瘍等所致急性上消化道出血。
規格
(1)40mg(以泮托拉唑計):10ml專用溶劑。
(2)80mg(以泮托拉唑計):10ml專用溶劑。
(2)80mg(以泮托拉唑計):10ml專用溶劑。
用法用量
靜脈滴注,一次40~80mg.每日1~2次,臨用前將10ml專用溶劑注入凍乾粉小瓶內,將上述溶解後的藥液加入0.9%氯化鈉注射液100~250ml中稀釋後供靜脈滴注。靜脈滴注時間要求15~60分鐘內滴完。本品溶解和稀釋後必須在4小時內用完,禁止用其它溶劑或其它藥物溶解和稀釋。
不良反應
偶見頭暈、失眠、嗜睡、噁心、腹瀉、便秘、皮疹和肌肉疼痛等症狀。大劑量使用時可出現心律不齊,轉氨酶升高,腎功能改變,粒細胞降低等。
禁忌
對本品過敏者、哺乳期婦女及孕婦禁用。
注意事項
1、當懷疑胃潰瘍時,應首先排除癌症的可能性。因為本品治療可減輕其症狀,從而延誤診斷。
2、肝腎功能不全者慎用。因本品經肝臟代謝,腎臟排出,故肝功能損害患者若使用本品應減量使用,同時監測肝臟酶譜的變化,若測定值升高則應停止用藥。腎功能受損的患者對此藥代謝的影響不太明顯,但也應控制日使用劑量不超過40mg。
3、療程一般可持續7天,最長不超過2周。
2、肝腎功能不全者慎用。因本品經肝臟代謝,腎臟排出,故肝功能損害患者若使用本品應減量使用,同時監測肝臟酶譜的變化,若測定值升高則應停止用藥。腎功能受損的患者對此藥代謝的影響不太明顯,但也應控制日使用劑量不超過40mg。
3、療程一般可持續7天,最長不超過2周。
孕婦及哺乳期婦女用藥
妊娠期與哺乳期婦女禁用。
兒童用藥
尚無兒童靜脈套用注射用泮托拉唑鈉的經驗。
老年用藥
老年人用藥劑量無需調整。
藥物相互作用
當與吸收取決於pH值的藥物(如酮康唑)同時使用時,應考慮到本藥對其吸收的影響。
本品在肝臟內通過細胞色素P450酶系代謝,因此凡能過該酶系代謝的其他藥物均不能除外與之產生相互作用的可能性。然而專門檢測許多這類藥物,如安定、新雙香豆素、茶鹼、苯妥英、地高辛和避孕藥卻未觀察到它們間有明顯臨床意義的相互作用。本品與同時使用的抗 酸藥也沒有相互作用。
本品在肝臟內通過細胞色素P450酶系代謝,因此凡能過該酶系代謝的其他藥物均不能除外與之產生相互作用的可能性。然而專門檢測許多這類藥物,如安定、新雙香豆素、茶鹼、苯妥英、地高辛和避孕藥卻未觀察到它們間有明顯臨床意義的相互作用。本品與同時使用的抗 酸藥也沒有相互作用。
藥物過量
未進行該項實驗且無可靠參考文獻。
藥理毒理
藥理作用
泮托拉唑為質子泵抑制劑,通過與胃壁細胞的H+-K+ATP酶系統的兩個位點共價結合而抑制胃酸產生的最後步驟。該作用呈劑量依賴性並使基礎和刺激狀態下的胃酸分泌均受抑制。本品與H+-K+ATP酶的結合可導致其抗胃酸分泌作用持續24小時以上。
毒理研究
遺傳毒性
泮托拉唑的人淋巴細胞染色體畸變試驗、中國倉鼠卵巢細胞/HGPRT正向突變試驗及二次小鼠微核試驗中的一次結果均為陽性,而大鼠肝臟DNA共價結合試驗結果難以判斷。Ames試驗、大鼠肝細胞程式外DNA合成試驗(UDS)、AS52/GPT哺乳動物細胞正向基因突變試驗、小鼠淋巴瘤L5178Y細胞胸腺嘧啶激酶突變試驗及體內大鼠骨髓細胞染色體畸變試驗結果均為陰性。
生殖毒性
雄性大鼠經口給予泮托拉唑500mg/kg/d(按體表面積折算為臨床推薦口服劑量的98倍),雌性大鼠經口給予泮托拉唑450mg/kg/d(按體表面積折算為臨床推薦口服劑量的88倍)時,生育力及生殖行為未見明顯異常。
大鼠靜脈給予泮托拉唑20mg/kg/d(按體表面積折算為臨床推薦口服劑量的4倍),家兔靜脈給予泮托拉唑15mg/kg/d(按體表面積折算為臨床推薦口服劑量的6倍),對生育力和胎仔均未見明顯損害。泮托拉唑及其代謝產物可以從家兔乳汁中分泌。
致癌性
SD大鼠連續24個月經口給予泮托拉唑0.5~200mg/kg/d,胃底出現劑量依賴性的腸嗜鉻樣細胞增生及良性和惡性的神經內分泌細胞瘤。當劑量為50和200mg/kg/d(按體表面積折算為臨床推薦口服劑量的10和40倍)時,前胃出現良性鱗狀細胞乳頭狀瘤和惡性鱗狀細胞癌。泮托拉唑還導致極少數大鼠出現胃腸道腫瘤,包括50mg/kg/d劑量時偶爾出現十二指腸腺癌,以及200mg/kg/d劑量時胃底出現良性息肉和腺癌。泮托拉唑給藥劑量0.5~200mg/kg/d時,大鼠劑量依賴性地出現肝細胞腺瘤和肝癌,200mg/kg/d劑量還可使大鼠甲狀腺囊泡細胞瘤和囊泡細胞癌的發生率增加。SD大鼠6個月和12個月的毒性研究中也偶見肝細胞腺瘤和肝癌。
Fischer344大鼠連續24個月經口給予泮托拉唑5~50mg/kg/d(按體表面積折算為臨床推薦口服劑量的1~10倍),胃底劑量依賴性出現腸嗜鉻樣細胞增生及良性和惡性的神經內分泌細胞瘤。但該試驗的劑量選擇不足以支持對泮托拉唑潛在致癌性的充分評價。
B6C3F1小鼠連續24個月經口給予泮托拉唑5~150mg/kg/d(按體表面積折算為臨床推薦口服劑量的0.5~15倍),同樣出現胃底腸嗜鉻樣細胞增生;雌鼠在150mg/kg/d劑量時,肝細胞腺瘤和肝癌的發生率升高。
上述嚙齒類動物的致癌性研究結果提示本品具有一定的致癌性,但此結果與臨床的相關性尚不清楚。
泮托拉唑為質子泵抑制劑,通過與胃壁細胞的H+-K+ATP酶系統的兩個位點共價結合而抑制胃酸產生的最後步驟。該作用呈劑量依賴性並使基礎和刺激狀態下的胃酸分泌均受抑制。本品與H+-K+ATP酶的結合可導致其抗胃酸分泌作用持續24小時以上。
毒理研究
遺傳毒性
泮托拉唑的人淋巴細胞染色體畸變試驗、中國倉鼠卵巢細胞/HGPRT正向突變試驗及二次小鼠微核試驗中的一次結果均為陽性,而大鼠肝臟DNA共價結合試驗結果難以判斷。Ames試驗、大鼠肝細胞程式外DNA合成試驗(UDS)、AS52/GPT哺乳動物細胞正向基因突變試驗、小鼠淋巴瘤L5178Y細胞胸腺嘧啶激酶突變試驗及體內大鼠骨髓細胞染色體畸變試驗結果均為陰性。
生殖毒性
雄性大鼠經口給予泮托拉唑500mg/kg/d(按體表面積折算為臨床推薦口服劑量的98倍),雌性大鼠經口給予泮托拉唑450mg/kg/d(按體表面積折算為臨床推薦口服劑量的88倍)時,生育力及生殖行為未見明顯異常。
大鼠靜脈給予泮托拉唑20mg/kg/d(按體表面積折算為臨床推薦口服劑量的4倍),家兔靜脈給予泮托拉唑15mg/kg/d(按體表面積折算為臨床推薦口服劑量的6倍),對生育力和胎仔均未見明顯損害。泮托拉唑及其代謝產物可以從家兔乳汁中分泌。
致癌性
SD大鼠連續24個月經口給予泮托拉唑0.5~200mg/kg/d,胃底出現劑量依賴性的腸嗜鉻樣細胞增生及良性和惡性的神經內分泌細胞瘤。當劑量為50和200mg/kg/d(按體表面積折算為臨床推薦口服劑量的10和40倍)時,前胃出現良性鱗狀細胞乳頭狀瘤和惡性鱗狀細胞癌。泮托拉唑還導致極少數大鼠出現胃腸道腫瘤,包括50mg/kg/d劑量時偶爾出現十二指腸腺癌,以及200mg/kg/d劑量時胃底出現良性息肉和腺癌。泮托拉唑給藥劑量0.5~200mg/kg/d時,大鼠劑量依賴性地出現肝細胞腺瘤和肝癌,200mg/kg/d劑量還可使大鼠甲狀腺囊泡細胞瘤和囊泡細胞癌的發生率增加。SD大鼠6個月和12個月的毒性研究中也偶見肝細胞腺瘤和肝癌。
Fischer344大鼠連續24個月經口給予泮托拉唑5~50mg/kg/d(按體表面積折算為臨床推薦口服劑量的1~10倍),胃底劑量依賴性出現腸嗜鉻樣細胞增生及良性和惡性的神經內分泌細胞瘤。但該試驗的劑量選擇不足以支持對泮托拉唑潛在致癌性的充分評價。
B6C3F1小鼠連續24個月經口給予泮托拉唑5~150mg/kg/d(按體表面積折算為臨床推薦口服劑量的0.5~15倍),同樣出現胃底腸嗜鉻樣細胞增生;雌鼠在150mg/kg/d劑量時,肝細胞腺瘤和肝癌的發生率升高。
上述嚙齒類動物的致癌性研究結果提示本品具有一定的致癌性,但此結果與臨床的相關性尚不清楚。
藥代動力學
本品具有較高的生物利用度,靜脈注射與口服給藥的生物利用度比值為1.2。約80%靜注本品的代謝物經尿中排泄,腎功能不全不影響藥代動力學,肝功能不全時可延緩清除。T1/2、清除率和表觀分布容積與給藥劑量無關。
貯藏
密閉,遮光保存。
包裝
西林瓶一瓶,專用溶劑一支。
有效期
24個月
執行標準
《中國藥典》2010年版二部
批准文號
(1)40mg:國藥準字H19990171
(2)80mg:國藥準字H20068732
(2)80mg:國藥準字H20068732
生產企業
江蘇奧賽康藥業有限公司
