氯化銨,簡稱氯銨。是指鹽酸的銨鹽,多為制鹼工業的副產品。含氮24%〜26%,呈白色或略帶黃色的方形或八面體小結晶,有粉狀和粒狀兩種劑型,粒狀氯化銨不易吸濕,易儲存,而粉狀氯化銨較多用作生產復肥的基礎肥料。屬生理酸性肥料,因含氯較多而不宜在酸性土和鹽鹼土上施用,不宜用作種肥、秧田肥或葉面肥,也不宜在忌氯作物(如菸草、馬鈴薯、柑橘、茶樹等)上施用。氯化銨用於稻田肥效較高而且穩定,因為C1既可抑制稻田硝化作用,又有利於水稻莖稈纖維形成,增加韌性,減少水稻倒伏和病蟲侵襲。
基本介紹
- 中文名:氯化銨
- 英文名:ammonium chloride
- 別稱:電鹽、電氣藥粉、鹽精、硇砂
- 化學式:NH4Cl
- 分子量:53.49
- CAS登錄號:12125-02-9
- EINECS登錄號:235-186-4
- 熔點:340 °C (subl.)(lit.)
- 沸點:520℃
- 水溶性:易溶
- 密度:1.527g/cm3
- 外觀:白色
性質,物理化學性狀,性狀,化學性質,製法,質量指標,用途處理,用途,危險性概述,個人防護,急救措施,消防措施,泄漏應急處理,生產方法,廢處理,離子型,儲運,醫藥套用,適應症,禁用慎用,給藥說明,不良反應,相互作用,工業用,性 質,技術條件,包裝,用途,常見四種,四丁基氯化銨,四戊基氯化銨,四丙基氯化銨,四乙基氯化銨,農業利用,
性質
水溶液呈弱酸性,加熱時酸性增強。對黑色金屬和其它金屬有腐蝕性,特別對銅腐蝕更大,對生鐵無腐蝕作用。
該產品主要有兩種生產工藝:一是用中國著名科學家侯德榜發明的侯氏制鹼法,同時生產純鹼和氯化銨兩種產品;二是生產碳酸鉀等鉀鹽的副產品。氯化銨很容易結塊,通常用添加防結塊劑的方式來防止產品結塊。
氯化銨在水中溶解度列表:
溫度/℃ | 溶解度/g |
0 | 29.4 |
10 | 33.3 |
20 | 37.2 |
30 | 41.4 |
40 | 45.8 |
50 | 50.4 |
60 | 55.2 |
70 | 60.2 |
80 | 65.6 |
90 | 71.3 |
100 | 77.3 |
將氨氣與氯化氫氣體混合,會有白煙生成,白煙即為氯化銨。
受熱易分解:
NH4Cl==△==NH3↑+HCl↑兩種物質在反應同時又會再度結合為氯化銨。
與硫酸反應:
NH4Cl+H2SO4====NH4HSO4+HCl↑
物理化學性狀
化學式:NH4Cl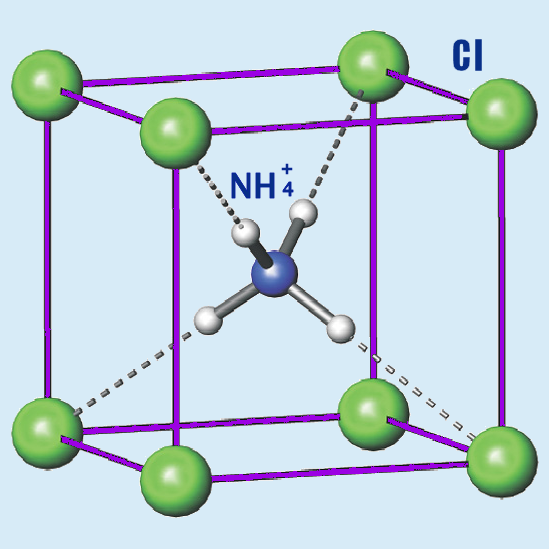 晶體結構
晶體結構
 晶體結構
晶體結構電子式:
相對分子質量:53.49
性狀
無色晶體或白色顆粒性粉末,是一種強電解質,溶於水電離出銨根離子和氯離子,氨氣和氯化氫化合生成氯化銨時會有白煙。無氣味。味鹹涼而微苦。吸濕性小,但在潮濕的陰雨天氣也能吸潮結塊。粉狀氯化銨極易潮解,合格品尤甚,吸濕點一般在76%左右,當空氣中相對濕度大於吸濕點時,氯化銨即產生吸潮現象,容易結塊。能升華(實際上是氯化銨的分解和重新生成的過程)而無熔點。相對密度1.5274。折光率1.642。低毒,半數致死量(大鼠,經口)1650mg/kg。有刺激性。加熱至350℃升華,沸點520℃。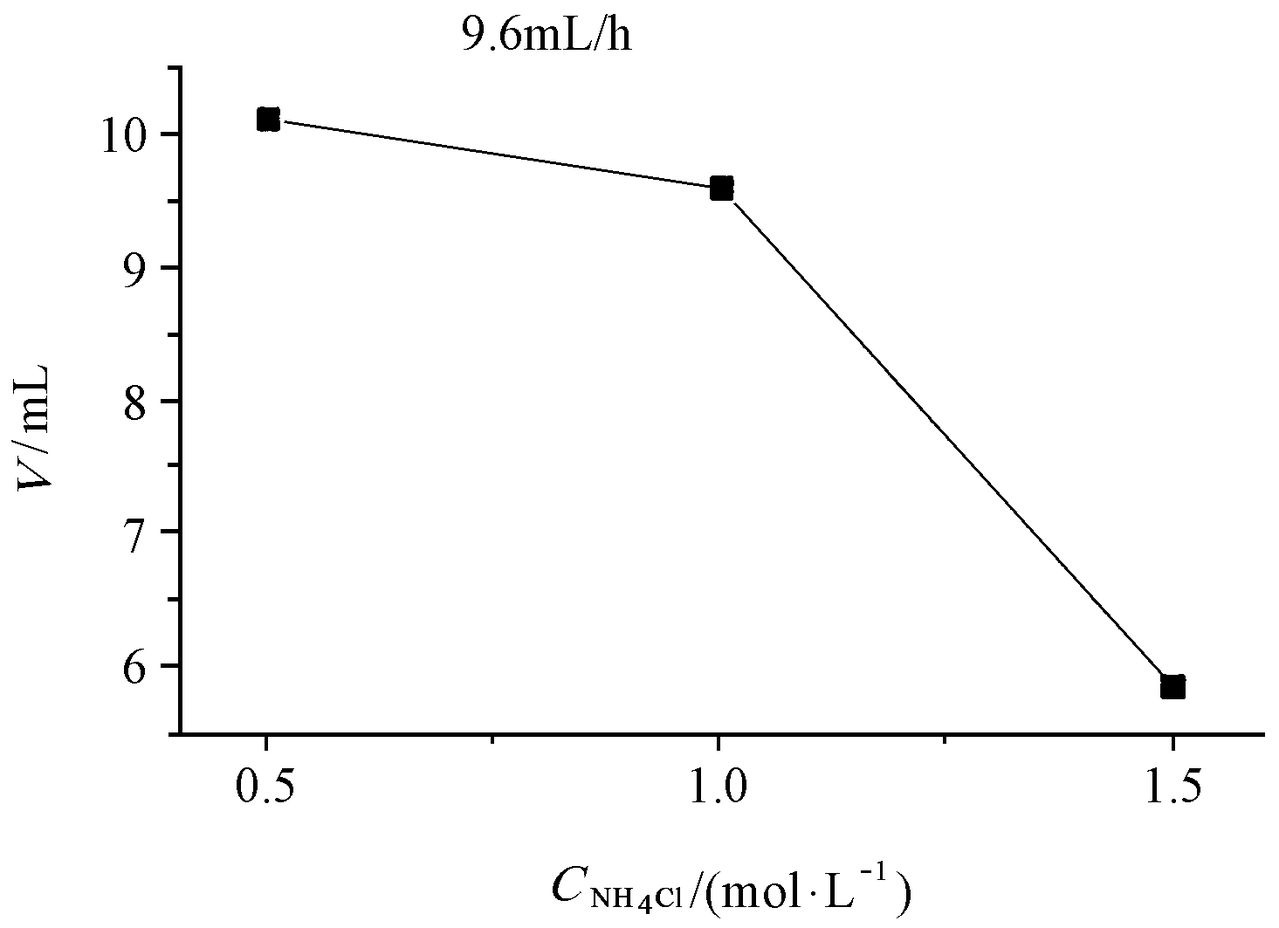 氯化銨
氯化銨
 氯化銨
氯化銨易溶於水,微溶於乙醇,溶於液氨,不溶於丙酮和乙醚。鹽酸和氯化鈉能降低其在水中的溶解度,其水中溶解度在0℃時為29.4g,10℃為33.2g,20℃為37.2g,30℃為41.4g,40℃為45.8g,50℃為50.4g,60℃為55.3g,70℃為60.2g,80℃為65.6g,90℃為71.2g,100℃為77.3g)。加熱至100℃時開始分解,337.8℃時可以完全分解為氨氣和氯化氫氣體,遇冷後又重新化合生成顆粒極小的氯化銨而呈現為白色濃煙,不易下沉,也極不易再溶解於水。
水溶液的pH:因為在水中電離出的銨根離子水解使溶液顯酸性,常溫下飽和氯化銨溶液PH值一般在5.6左右。25℃時,1%為5.5,3%為5.1,10%為5.0。氯化銨本身可以作為鉍、銻的穩定試劑(提供氯離子進行配位,使用時將其化合物與氯化銨共溶於稀鹽酸中)。
化學性質
1.水溶液呈弱酸性,加熱時酸性增強。對黑色金屬和其它金屬有腐蝕性,特別對銅腐蝕更大,對生鐵無腐蝕作用;將氨氣與氯化氫氣體混合,會有白煙生成,白煙即為氯化銨;
2.受熱易分解:
NH4Cl====NH3↑+HCl↑此反應為可逆反應,兩種物質在反應同時又會再度結合為氯化銨。
與硫酸反應:
NH4Cl+H2SO4====NH4HSO4+HCl↑
製法
1.重結晶法:將粗品氯化銨加入溶解器,通人蒸汽溶解,經過濾,將濾液冷卻結晶、離心分離、乾燥,製得工業氯化銨成品。離心分離的母液返回溶解器使用;
2.複分解法:首先將氯化銨母液加入反應器中加熱至105℃後,加入硫酸銨和食鹽,於117℃進行複分解反應,生成氯化銨溶液和硫酸鈉結晶,經過濾分離除去硫酸鈉,將氯化銨飽和溶液送至冷卻結晶器,冷卻至32~35℃析出結晶,過濾,把結晶分別用4種不同濃度的氯化銨溶液進行淋洗,控制Fe<0.008%,SO42-<0.001%,淋洗至合格後,再用氯化銨溶液重新將結晶調成漿狀,送入離心機分離脫水,再經熱風乾燥,製得工業氯化銨成品。母液送至複分解反應器循環使用。過濾分離的硫酸鈉用於生產元明粉;
3.氣液相合成法將氯化氫氣體從湍流吸收塔的底部通入,與塔頂噴淋的循環母液接觸,生成飽和氯化氫的氯化銨母液流入反應器,與通入氨氣進行中和反應,生成氯化銨飽和溶液。送至冷卻結晶器,經冷卻至30~45℃,析出過飽和的氯化銨晶體。把結晶器上部氯化銨溶液送至風冷器冷卻並循環至結晶器;下部晶漿經稠厚器增稠後再離心分離,製得氯化銨成品。經離心分離的母液送至湍流吸收塔循環使用;
質量指標
工業氯化銨的質量指標:
指標名稱 一等品 二等品
氯化銨(NH4Cl)(以乾基計)的質量分數/%≥ 99.3 99.0
水分/%≤ 1.0 1.0
氯化鈉(以乾基計)/%≤ 0.2 0.3
水不溶物/%≤ 0.02 0.03
硫酸鹽/%≤ 0.02 0.04
pH值 4.2~5.8 4.2~5.8
用途處理
用途
1.可用作原料,製造乾電池和蓄電池、其他銨鹽、電鍍添加劑、金屬焊接助熔劑;
2.用作染色助劑,也用於鍍錫和鍍鋅、鞣革、醫藥、制蠟燭、黏合劑、滲鉻、精密鑄造;
3.用於醫藥、乾電池、織物印染、洗滌劑;
氯化銨能化痰止咳
①氯化銨進入體內,部分銨離子迅速由肝臟代謝形成尿素,由尿排出。氯離子與氫結合成鹽酸,從而糾正鹼中毒。
②由於對黏膜的化學性刺激,反射性地增加痰量,使痰液易於排出,因此有利於不易咳出的少量粘痰的清除。本品被吸收後,氯離子進入血液和細胞外液使尿液酸化。
禁用慎用
(1)肝腎功能不全者禁用,腎功能不全時慎用,以防高氯性酸中毒。
(2)在鐮狀細胞貧血患者,可引起缺氧或(和)酸中毒。
(3)潰瘍病、代謝性酸血症患者忌用。
(4)孕婦及哺乳期婦女禁用
(5)兒童在醫生指導下使用
4.用作農作物肥料,適用於水稻、小麥、棉花、麻類、蔬菜等作物;
5.用作分析試劑,如配製氨-氯化銨緩衝溶液。用作電化學分析中的支持電解質。用作發射光譜分析用的電弧穩定劑,原子吸收光譜分析用的干擾抑制劑,合纖粘度的檢驗;
6.藥用氯化銨用作祛痰藥和利尿藥 祛痰藥;
7.酵母養料(主要用於啤酒釀造);麵團調節劑。一般與碳酸氫鈉混合後使用,用量約為碳酸氫鈉的25%,或小麥粉量的10~20g//kg。主要用於麵包、餅乾等中。加工助劑(GB 2760-96)
危險性概述
對皮膚、黏膜有刺激性,可引起肝腎功能損害,誘發肝昏迷,造成氮質血症和代謝性酸中毒等。健康人套用50g 氯化銨可致重度中毒,有肝病、腎病、慢性心臟病的患者,5g即可引起嚴重中毒。口服中毒引起化學性胃炎,嚴重者由於血氨顯著增高,誘發肝昏迷。嚴重中毒時造成肝、腎損害,出現代謝性酸中毒,同時支氣管分泌物大量增加。職業性接觸,可引起呼吸道黏膜的刺激和灼傷。慢性影響: 經常性接觸氯化銨,可引起眼結膜及呼吸道黏膜慢性炎症。
不燃,具刺激性。
個人防護
呼吸系統防護:空氣中粉塵濃度超標時,必須佩戴自吸過濾式防塵口罩。緊急事態搶救或撤離時,應該佩戴空氣呼吸器。
眼睛防護:戴化學安全防護眼鏡。
身體防護:穿防毒物滲透工作服。
手防護:戴橡膠手套。
其他防護:工作完畢,淋浴更衣。注意個人清潔衛生。產品設備要密閉,車間通風應良好。
急救措施
皮膚接觸:脫去污染的衣著,用大量流動清水沖洗。
眼睛接觸:提起眼瞼,用流動清水或生理鹽水沖洗。就醫。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難應立即就醫處治。
食入:飲足量溫水,催吐。洗胃,導泄。就醫。
消防措施
危險特性:未有特殊的燃燒爆炸特性。受高溫分解產生有毒的腐蝕性煙氣。
有害燃燒產物:氯化氫、氮氧化物。
滅火方法:消防人員必須穿全身防火防毒服,在上風向滅火。滅火時儘可能將容器從火場移至空曠處。
泄漏應急處理
應急處理:隔離泄漏污染區,立即切斷泄漏源,將盛裝容器訊速移出事故區域,遠離熱源,火源。應急處置人員應佩戴安全防護用品,事故處理完,應將處理用品用具,參與廢料、事故現場,清洗廢水等進行無害化處理酯達到環保要求。。建議應急處理人員戴防塵面具(全面罩),穿防毒服。避免揚塵,小心掃起,置於袋中轉移至安全場所。若大量泄漏,用塑膠布、帆布覆蓋。收集回收或運至廢物處理場所處置。
生產方法
廢處理
用氫氧化鈉溶液預處理,放出的氨氣回收使用,剩下的處理液加水稀釋到規定的容許濃度,再進行無害化處理。
離子型
氯化銨由於銨根的半徑為143pm,接近鉀離子(133pm)和銣離子(149pm)的半徑,因而銨鹽性質類似於鹼金屬鹽類,而且往往與鉀鹽和銣鹽同晶,並有相似的溶解度。
氯化銨的晶胞類型是氯化銫型,即氯離子做簡單立方堆積,銨根離子填入全部的立方體空隙,為立方晶系,簡單立方晶胞。
儲運
應儲存在陰涼、通風、乾燥的庫房內,注意防潮。避免與酸類、鹼類物質共儲混運。運輸過程中要防雨淋和烈日曝曬。裝卸時要小心輕放,防止包裝破損。失火時,可用水、沙土、二氧化碳滅火器撲救。
技術條件:執行中華人民共和國國家標準。
GB/T2946-2008(2009年8月1日)開始執行,產品分為工業用氯化銨和農業用氯化銨兩大類,其中,工業氯化銨一等品質量標準如下:
⑴外觀:白色結晶
⑵氯化銨含量(以乾基計)>99.3%
⑶水份含量<0.7%
⑷灼燒殘渣<0.4%
⑸鐵含量<0.001%
⑹重金屬含量(以Pb計)< 0.0005%
⑺硫酸鹽含量(以SO42- 計) < 0.05%
⑻PH值:4.0-5.8
類別 鹽
醫藥套用
適應症
該品為刺激性祛痰藥:適用於乾咳以及痰不易咳出等;也用於泌尿系感染需酸化尿液時。該品用於糾正代謝性鹼中毒。
①重度代謝性鹼中毒,套用足量氯化鈉注射液不能滿意糾正者。②氯化銨負荷試驗可了解腎小管酸化功能,用於腎小管性酸中毒的鑑別診斷。③祛痰,適用於乾咳以及痰不易咳出等。
禁用慎用
①肝腎功能不全者禁用;
②在鐮狀細胞貧血患者,可引起缺氧或(和)酸中毒。
⑴肝功能不全時禁用。
⑵腎功能不全時慎用,以防高氯性酸中毒。
⑶潰瘍病、代謝性酸血症患者忌用。
⑷孕婦及哺乳期婦女禁用
⑸兒童在醫生指導下使用
給藥說明
隨訪檢查:①酸鹼平衡分析指標;②血氯、鉀、鈉濃度測定。
輕、中度代謝性鹼中毒,僅需給予足量氯化鈉注射液或同時給予氯化鉀即可糾正。該品僅用於重度代謝性鹼中毒。
用於腎小管性酸中毒的鑑別診斷時,已有酸中毒者不需再做氯化銨負荷試驗,以免加重酸中毒。
不良反應
服用後有噁心,偶出現嘔吐。過量或長期服用可造成酸中毒和低鉀血症。
⑴氯化銨過量可致高氯性酸中毒,低鉀及低鈉血症。
⑵肝功能不全時,因肝臟不能將銨離子轉化為尿素而發生氨中毒。
⑶口服氯化銨可有胃腸道反應。
劑量過大時有嘔吐,噁心,可引起胃腸道刺激或不適.
相互作用
該品與磺胺嘧啶、呋喃妥因等呈配伍禁忌。
與鹼、金黴素、新黴素、呋喃妥因、磺胺嘧啶、華法林呈配伍禁忌。
不良反應及其注意事項如下:
⑴套用過量可導致高氯性酸血症,故應注意使用適量為妥。
⑵凡右心衰竭和肝硬化便伴有代謝性鹼血證的病人,均應禁用該藥,以免加重原來病情。
⑶腎功能不全病人也需要禁用。
該藥不宜與對氨基水楊酸鈉、阿司匹林及安體舒通合用,一面是後者的毒性增加。也不宜與苯丙胺、丙咪嗪、阿米替林或多慮平合用,以免造成後者療效減弱。
CAS No.:12125-02-9
工業用
工業級氯化銨 99.5%
化學名稱:工業氯化銨
英文名稱:AMMONIUM CHLORIDE
分 子 式:NH4Cl
分 子 量:53.49
性 質
技術條件
執行中華人民共和國國家標準:GBT-2946-2008
⑴外觀:白色結晶
⑵氯化銨含量(以乾基計)》99.5%
⑶水份含量 《0.4%
⑷氯化鈉含量(以乾基計)《 0.2%
⑸鐵含量《0.001%
⑹重金屬含量(以Pb計)《 0.0005%
⑺水不溶物含量《0.02%
⑻硫酸鹽含量(以SO42- 計) 《 0.02%
⑼PH值:4.0~5.8
⑽灼燒殘渣:《0.4%
包裝
每件袋25Kg或50Kg內襯塑膠袋,外層編織袋。
用途
工業級氯化銨的用途主要用於電池、電鍍、染織、鑄造、醫藥、植絨,絨毛,化工中間體等方面。
常見四種
四丁基氯化銨
中文名稱:四丁基氯化銨
英文名稱:Tetrabutylammonium Chloride [Reagent for Ion-Pair Chromatography]
CAS號:1112-67-0
分子式:C16H36ClN
分子量:277.92
純度:>98.0%
等級:Ace
MDL號:MFCD00011635
四戊基氯化銨
中文名稱:四戊基氯化銨
英文名稱:Tetraamylammonium Chloride
英文別名:Tetrapentylammonium Chloride
CAS號:4965-17-7
分子式:C20H44ClN
分子量:334.02
純度:>98.0%
等級:EP
MDL號:MFCD00011857
四丙基氯化銨
中文名稱:四丙基氯化銨
英文名稱:Tetrapropylammonium Chloride

