形態
氟銻酸或稱六氟銻酸、六氟合銻酸,化學式為HSbF
6,是
氫氟酸和電子酸五氟化銻反應後的產物.以一比一的比例混合時成為已知最強的超強酸,實驗證明能分解碳氫化合物,產生碳正離子以及氫氣。
氫氟酸(HF)和五氟化銻(SbF
5)互相反應強烈放熱.HF會釋放質子H
+,然後氟離子F
-會與SbF
5形成八面體型的SbF
6-陰離子。SbF
6-是非配位陰離子,親核性和鹼性都很弱.於是質子實際上是“裸露”在溶液中,使得混合物體系呈現超強的酸性,比純硫酸要強2×10
19倍。該酸必須用特氟龍(
聚四氟乙烯)材料裝盛。
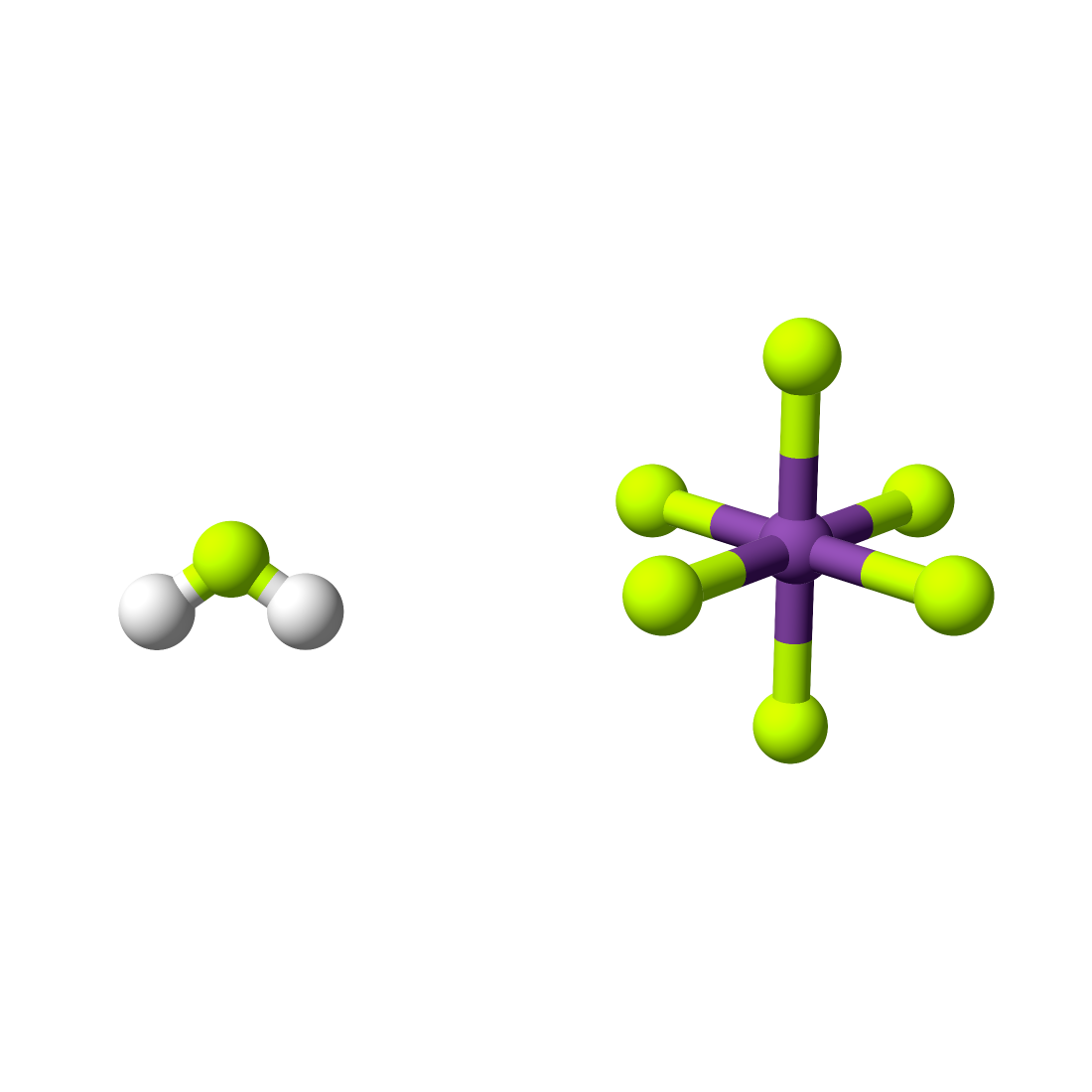
圖右為氟銻酸的3D分子球棍模型。
結構
用
X射線晶體學研究兩份HF-SbF5反應形成的結晶,發現化學式分別為[H2F][Sb2F11]和[H3F2][Sb2F11],都含有Sb2F11作陰離子。據估計,Sb2F11離子的鹼性比SbF6還要弱,因此更加穩定。
酸度對照
氟銻酸【1:1】(1990)(H0值= -28)
註:碳硼烷酸是單一分子酸中酸性最強的酸,而非酸性最強的酸。
六氟銻酸是超強酸體系,而非化合物。
套用
(CH3)3CH + H+→ (CH)3C3 + H2;
(CH3)4C + H+→ (CH3)3C + CH4
1、使某些很難質子化的物質(如高氯酸)質子化,進一步製備含有-ClO3基團的有機物:
HClO4 + H+ ==== [H2ClO4]+
[H2ClO4]+ +H+ ====[ClO3]++ [H3O]+
C6H6 + [ClO3]+ ==== [C6H6ClO3]+
[C6H6ClO3]+ - H+ ====C6H5ClO3
(CH3)3CH + H → (CH3)3C + H2;
(CH3)4C + H → (CH3)3C + CH4
3、含有
羥基的有機物(如醇、酚、羧酸等)質子化,進一步脫
羥基化。
R-OH + 2H = R+(碳正離子) + [H3O]+
4、
強氧化劑:Sb(Ⅵ)氟化物例如SbF
6具有很強的
氧化性,能夠氧化多種金屬及還原劑。
5,配位性:Au+HSbF
6Au
3++Sb
3++HF
要注意的是,氟銻酸是無水體系,當氟銻酸與大量水混合時發生強烈反應,氫離子(
質子)被中和生成
水合氫離子,不再具有超酸性。
反應方程式:H++H2O=H3O+
危險性
氟銻酸會與水發生強烈反應甚至爆炸,若溶劑為水,則與其他酸的強度無法區分。 盛氟銻酸的容器必須用
特氟龍(即聚四氟乙烯)的材料盛裝,其他塑膠會被嚴重腐蝕。
性狀:
1、沸點:無(注意,混合物無固定沸點)
2、熔點:無(注意,混合物無固定熔點)
3、氟銻酸中均不含水,SbF5為溶劑,H2SbF7及HF是溶質。故氟銻酸均為無色油狀液體。
4、
氧化性:因為其中含有五價銻,所以氧化性非常強。




