歐乃派克(碘海醇注射液),適應症為X線造影劑。可用於心血管造影、動脈造影、尿路造影、靜脈造影、CT增強檢查;頸、胸和腰段椎管造影、經椎管蛛網膜下腔注射後CT腦池造影;關節腔造影、經內窺鏡胰膽管造影(ERCP)、疝或瘺道造影、子宮輸卵管造影、涎腺造影、經皮肝膽管造影(PTC)、竇道造影、胃腸道造影和“T”型管造影等。
基本介紹
- 藥品名稱:歐乃派克?
- 藥品類型:處方藥、基本藥物、醫保工傷用藥
- 用途分類:腦脊髓造影劑
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,核准日期,修訂日期,
成份
本品主要成份為碘海醇,其化學名稱為:5-[N-(2,3-二羥丙基)乙醯胺基]-N,N’-雙(2,3-二羥丙基)-2,4,6-三碘-1,3-苯二甲醯胺。
化學結構式:
分子式:C19H26I3N3O9
分子量:821.14
輔料:氨丁三醇,EDTA鈣鈉,鹽酸調節pH,注射用水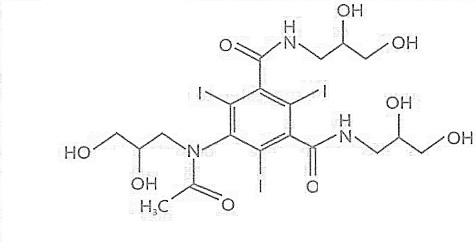
化學結構式:
分子式:C19H26I3N3O9
分子量:821.14
輔料:氨丁三醇,EDTA鈣鈉,鹽酸調節pH,注射用水

性狀
本品為無色至淡黃色澄明溶液。
適應症
X線造影劑。可用於心血管造影、動脈造影、尿路造影、靜脈造影、CT增強檢查;頸、胸和腰段椎管造影、經椎管蛛網膜下腔注射後CT腦池造影;關節腔造影、經內窺鏡胰膽管造影(ERCP)、疝或瘺道造影、子宮輸卵管造影、涎腺造影、經皮肝膽管造影(PTC)、竇道造影、胃腸道造影和“T”型管造影等。
規格
(1)10ml:3g(I) (2)20ml:6g(I) (3)50ml:15g(I) (4)75ml:22.5g(I) (5)100ml:30g(I) (6)20 ml:7g(I) (7)50ml:17.5g(I) (8)75 ml:26.25g(I) (9)100ml:35g(I) (10)200 ml:70g(I)
用法用量
給藥劑量取決於檢查的種類、病人的年齡、體重、心輸出量和全身情況及使用的技術。一般而言,該藥的常用碘濃度和容量與目前使用的其它含碘對比劑相似。和其它造影劑一樣,在用藥前後都必須保證體內有充足的水份。以下的劑量可作為臨床指導。
1、 靜脈注射指南
2、 動脈注射指南
3、脊髓造影指南
4、體腔內使用指南
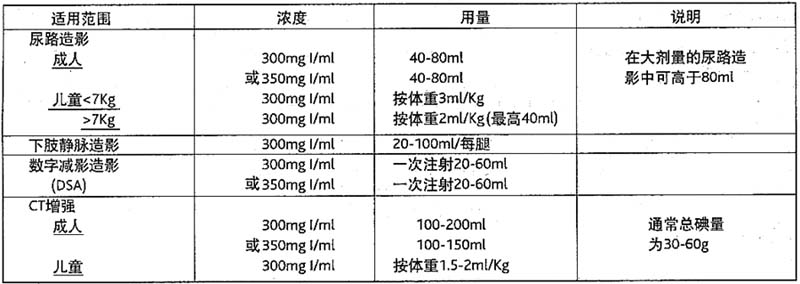
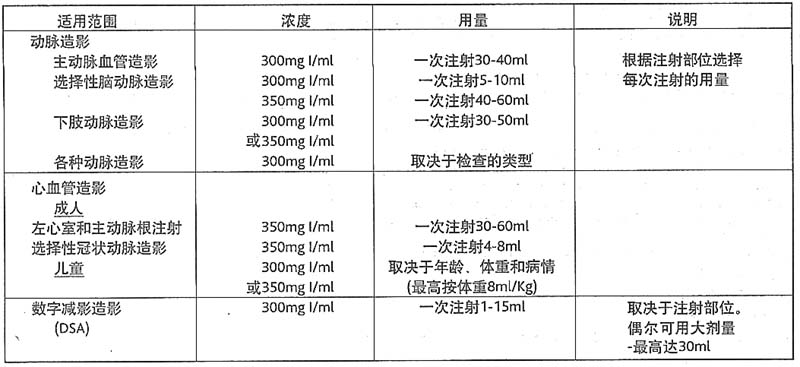


1、 靜脈注射指南
2、 動脈注射指南
3、脊髓造影指南
4、體腔內使用指南




不良反應
[u]常見不良反應(適用於所有含碘對比劑)[/u]
以下所列的是與造影有關的不良反應,包括了非離子型單體對比劑,對應各種不同檢查而產生的不良反應,詳見對應章節。
和含碘對比劑有關的不良反應本質上一般都為輕到中度且為暫時性的,非離子型對比劑的不良反應要比離子型對比劑更少。重度反應和致死反應非常罕見。
常見的不良反應為輕度的感覺異常,如熱感或暫時性的金屬味覺。腹部不適或疼痛很罕見(發病率[1:1000),胃腸道反應如噁心、嘔吐也很少見(發病率[1:100,但]1:1000)。過敏反應較少見,通常表現為[u]輕度的呼吸道和皮膚反應[/u],如呼吸困難、皮疹、紅斑、蕁麻疹、瘙癢和血管性水腫,它們可在注射後立即出現也可在幾天后出現。嚴重的反應如喉頭水腫、支氣管痙攣或肺水腫非常少見。嚴重甚至毒性的皮膚反應已有報導。過敏樣反應可能與劑量和用藥途徑無關。嚴重反應的最初症狀可能僅是輕微的過敏症狀,必須馬上停止繼續使用造影劑,必要時應立即通過血管給藥進行相應的治療。使用β受體阻滯劑的病人其過敏反應的症狀可能不典型,容易誤為迷走神經反應。迷走神經反應可引起低血壓和心律過緩,很少見。可能發生頭痛或發熱。偶可發熱伴寒戰。碘中毒或“碘中毒性腮腺炎”是一種罕見的與使用碘造影劑有關的併發症,表現為腮腺的腫脹和觸痛,可在檢查後持續達10天。
[u]血管內注射(動脈和靜脈內注射)[/u]
請首先閱讀“常見不良反應”章節。以下內容只描述了在血管內注射非離子型單體對比劑後易發生的不良反應。
在動脈內注射對比劑所引起的不良反應性質與注射的部位和劑量有關。選擇性動脈造影或其它相應的技術操作可使目標器官處於高濃度造影劑狀態,可能會引起相應器官的併發症。外周血管造影常會引起遠端的疼痛和熱感(發症率]1:10)。再注射含碘造影劑後短暫性血清肌酐上升也很常見,但通常無臨慶意義。腎功能衰竭非常罕見。不過在高危病人中有致死病例的報導。冠脈、腦或腎動脈注射後會引起動脈痙攣並導致局部缺血。神經系統反應非常罕見。它們可為癲癇發作或短暫性運動或感覺障礙。偶可在隨防的CT掃描時見到造影劑通過血腦屏障為腦皮質攝取,有時可伴短暫性意識模糊或皮層盲。嚴重的心臟併發症如心搏停止、心律紊亂、心功能減退或心肌缺血都很少見。
靜脈造影后的血栓性靜脈炎和靜脈內血栓形成很少見。曾有極個別關節痛的病例報導。
[u]椎管內使用[/u]
請首先閱讀“常見不良反應”章節。以下內容只描述了在椎管內注射非離子型單體對比劑後易發生的不良反應。
鞘內注射後的不良反應可能在檢查後幾小時甚至幾天后延遲出現。其發生率與單獨腰穿相似。頭痛、噁心、嘔吐和頭暈很常見,主要與穿刺點腦脊液滲漏引起蛛網膜下腔壓力下降有關。有些病人會有嚴重的頭痛並持續幾天。不要抽出太多的腦脊液以避免壓力過度下降。輕度的局部疼痛、外周感覺異常和根性疼痛偶可發生在注射的部位(發生率[1:10,但]1:100)。偶見下肢疼痛和痛性痙攣。腦膜刺激所致的畏光和假性腦膜炎偶有發生。症狀明顯的化學性腦膜炎非常罕見,也應考慮有感染性腦膜炎的可能。非常少見的反應還有短暫性腦功能失調,包括癲癇發作、短暫性意識喪失、運動和感覺障礙。少數病人有EEG的改變。
[u]體腔內使用[/u]
請首先閱讀“常見不良反應”章節。以下內容只描述了在體腔內注射非離子型單體對比劑後易發生的不良反應。
全身性過敏反應少見。
ERCP:澱粉酶水平略有升高比較常見。ERCP檢查後偶可在腎臟內見到造影劑,此情況提示ERCP後胰腺炎的危險性大為增加。也有發生壞死性胰腺炎的個案報導。
口服造影劑偶可發生胃腸道不適。
子宮輸卵管造影:常下腹部短暫性輕度疼痛。
關節腔造影:造影術後疼痛比較常見。症狀明顯的關節炎罕見,此種病人應考慮感染性關節炎的可能。
疝造影:輕度的術後疼痛較常見。
以下所列的是與造影有關的不良反應,包括了非離子型單體對比劑,對應各種不同檢查而產生的不良反應,詳見對應章節。
和含碘對比劑有關的不良反應本質上一般都為輕到中度且為暫時性的,非離子型對比劑的不良反應要比離子型對比劑更少。重度反應和致死反應非常罕見。
常見的不良反應為輕度的感覺異常,如熱感或暫時性的金屬味覺。腹部不適或疼痛很罕見(發病率[1:1000),胃腸道反應如噁心、嘔吐也很少見(發病率[1:100,但]1:1000)。過敏反應較少見,通常表現為[u]輕度的呼吸道和皮膚反應[/u],如呼吸困難、皮疹、紅斑、蕁麻疹、瘙癢和血管性水腫,它們可在注射後立即出現也可在幾天后出現。嚴重的反應如喉頭水腫、支氣管痙攣或肺水腫非常少見。嚴重甚至毒性的皮膚反應已有報導。過敏樣反應可能與劑量和用藥途徑無關。嚴重反應的最初症狀可能僅是輕微的過敏症狀,必須馬上停止繼續使用造影劑,必要時應立即通過血管給藥進行相應的治療。使用β受體阻滯劑的病人其過敏反應的症狀可能不典型,容易誤為迷走神經反應。迷走神經反應可引起低血壓和心律過緩,很少見。可能發生頭痛或發熱。偶可發熱伴寒戰。碘中毒或“碘中毒性腮腺炎”是一種罕見的與使用碘造影劑有關的併發症,表現為腮腺的腫脹和觸痛,可在檢查後持續達10天。
[u]血管內注射(動脈和靜脈內注射)[/u]
請首先閱讀“常見不良反應”章節。以下內容只描述了在血管內注射非離子型單體對比劑後易發生的不良反應。
在動脈內注射對比劑所引起的不良反應性質與注射的部位和劑量有關。選擇性動脈造影或其它相應的技術操作可使目標器官處於高濃度造影劑狀態,可能會引起相應器官的併發症。外周血管造影常會引起遠端的疼痛和熱感(發症率]1:10)。再注射含碘造影劑後短暫性血清肌酐上升也很常見,但通常無臨慶意義。腎功能衰竭非常罕見。不過在高危病人中有致死病例的報導。冠脈、腦或腎動脈注射後會引起動脈痙攣並導致局部缺血。神經系統反應非常罕見。它們可為癲癇發作或短暫性運動或感覺障礙。偶可在隨防的CT掃描時見到造影劑通過血腦屏障為腦皮質攝取,有時可伴短暫性意識模糊或皮層盲。嚴重的心臟併發症如心搏停止、心律紊亂、心功能減退或心肌缺血都很少見。
靜脈造影后的血栓性靜脈炎和靜脈內血栓形成很少見。曾有極個別關節痛的病例報導。
[u]椎管內使用[/u]
請首先閱讀“常見不良反應”章節。以下內容只描述了在椎管內注射非離子型單體對比劑後易發生的不良反應。
鞘內注射後的不良反應可能在檢查後幾小時甚至幾天后延遲出現。其發生率與單獨腰穿相似。頭痛、噁心、嘔吐和頭暈很常見,主要與穿刺點腦脊液滲漏引起蛛網膜下腔壓力下降有關。有些病人會有嚴重的頭痛並持續幾天。不要抽出太多的腦脊液以避免壓力過度下降。輕度的局部疼痛、外周感覺異常和根性疼痛偶可發生在注射的部位(發生率[1:10,但]1:100)。偶見下肢疼痛和痛性痙攣。腦膜刺激所致的畏光和假性腦膜炎偶有發生。症狀明顯的化學性腦膜炎非常罕見,也應考慮有感染性腦膜炎的可能。非常少見的反應還有短暫性腦功能失調,包括癲癇發作、短暫性意識喪失、運動和感覺障礙。少數病人有EEG的改變。
[u]體腔內使用[/u]
請首先閱讀“常見不良反應”章節。以下內容只描述了在體腔內注射非離子型單體對比劑後易發生的不良反應。
全身性過敏反應少見。
ERCP:澱粉酶水平略有升高比較常見。ERCP檢查後偶可在腎臟內見到造影劑,此情況提示ERCP後胰腺炎的危險性大為增加。也有發生壞死性胰腺炎的個案報導。
口服造影劑偶可發生胃腸道不適。
子宮輸卵管造影:常下腹部短暫性輕度疼痛。
關節腔造影:造影術後疼痛比較常見。症狀明顯的關節炎罕見,此種病人應考慮感染性關節炎的可能。
疝造影:輕度的術後疼痛較常見。
禁忌
有嚴重的甲狀腺毒症表現的患者禁用;對本品有嚴重過敏史者禁用。
注意事項
[u]使用非離子型單體對比劑的一般注意事項:[/u]
1、 有過敏、哮喘和對含碘製劑有過不良反應的需特別注意。對這些病例可考慮使用預防用藥,如類固醇,H1,H2組胺受體拮抗劑等。
2、 使用本品後發生嚴重反應的風險很小。但是,碘造影劑可激發過敏樣反應或其它過敏反應的表現。因此應預先進行急救措施的訓練和預備必需的搶救藥物和器械以應付可能出現的嚴重反應。
3、 鑒於預試驗對有非離子型造影劑引起的過敏反應預測的準確性極低,以及預試驗本身也可能導致嚴重過敏反應,因此不見建議採用預試驗來預測碘過敏。
4、 在整個X線檢查過程中應始終保持靜脈輸液通路暢通。
5、 體外試驗中,非離子型造影劑對凝血系統的影響較離子型造影劑為輕。在施行血管造影術時,應十分小心在血管內的技術操作,不時地用肝素化的生理鹽水灌洗導管以減少與操作技術相關的血栓形成和栓塞。
6、 在用造影劑前後必須保證體內有足夠的水分。這一點尤其適合患有多發性骨髓瘤、糖尿病、腎功能不全的病人及嬰幼兒和老年人。小於1歲的嬰兒,特別是新生兒易引起電解質紊亂和血液動力學失調。對有嚴重心臟病和肺動脈高壓的病人需特別注意。因為他們易發展為血液動力學失調和心律紊亂。
7、 急性腦病、腦瘤或有癲癇病史的病人要預防癲癇發作並需特別的注意。酗酒和吸毒者其癲癇發作和神經系統反應危險性大為增加。少數病人在椎管造影后發生短暫性聽力喪失或耳聾,這可能是腰穿後腦脊液壓力下降所致。
8、 為預防使用造影劑後的急性腎功能衰竭,對已有腎功能損害和糖尿病的病人需要特別注意,因為他們的危險性較大。異型球蛋白血症(多發性骨髓瘤病和Waldenstrom巨球蛋白血症)的病人危險性也較大。
9、[u] 預防措施包括:[/u]
-鑑別有高危險因素的病人。
-確保體內有足夠的水分。如有必要,可在檢查前由靜脈維持輸液直到造影劑從腎臟清除。
-在造影劑清除之前避免任何加重腎臟負擔的腎毒性藥物、口服膽囊造影劑、動脈鉗閉術、腎動脈成形術或其它大型手術。
-延遲重複的造影檢查直到腎功能恢復到檢查前水平。
為防止乳酸性中毒。在對使用二甲雙胍的糖尿病人血管內注射含碘對比劑前,必須測定血清肌酐水平。對於[u]血清肌酐/腎功能正常的患者[/u]:在注射造影劑時必須停用二甲雙胍並在48小時內不能恢復用藥,或直至腎功能/血清肌酐達正常值。對於[u]血清肌酐/腎功能不正常[/u]的患者:必須停用二甲雙胍並將對比劑檢查推遲至48小時後。只有在腎功能/血清肌酐水平恆定後才能恢復二甲雙胍的用藥。對有些腎功能不正常或未知的急救病例,醫生必須評估使用造影劑檢查的利弊,並需採取預防措施:停用二甲雙胍,給病人充足的水分,監測腎功能和仔細觀察乳酸性酸中毒的症狀。
存在發生暫時性肝功能紊亂的潛在風險。嚴重肝腎功能不全的病人需特別注意,因為這些病人清除造影劑的時間明顯延長。血透的病人在接受造影劑檢查後應立即進行血液透析。
含碘造影劑可加重重症肌無力的症狀。嗜鉻細胞瘤病人在介入治療時應給予預防高血壓危象的α受體阻滯劑。甲亢病人也需特別注意。多髮結節性甲狀腺腫的病人在使用碘造影劑後有發展成甲亢的可能。應清楚地認識到早產兒在使用造影劑後有短暫性甲減的可能。
造影劑外滲時偶然會引起局部的疼痛和水腫,它們會逐漸消退,不留後遺症。不過,偶可見發生炎症甚至組織壞死的病例。常規處理方法為抬高患肢和局部冷敷。萬一發生隔室綜合症需手術減壓。
10、[u]觀察時間:[/u]
使用造影劑後的病人應至少觀察30分鐘以上,因為大多數的嚴重不良反應都發生在這段時間。不過,仍有發生延遲反應的可能。
11、[u]椎管內注射:[/u]
在椎管造影後,病人應休息1小時,頭、胸抬高20°。然後可小心下床行走但不要彎腰。如仍躺在床上,應保持頭胸抬高位6小時。對癲癇發作閾較低的病人在此期間應密切觀察。門診病人最初的24小時內不能獨處。
12、對駕駛和操作機器能力的影響:
在椎管內注射後24小時內不應駕駛和操作機器。
13、如所有的非胃腸道藥品本品應在使用前目檢,以檢查是否有微粒、變色及容器是否損壞。藥品應在使用前才被抽入針筒,本品每瓶本品僅供單次使用,丟棄未用部分。
1、 有過敏、哮喘和對含碘製劑有過不良反應的需特別注意。對這些病例可考慮使用預防用藥,如類固醇,H1,H2組胺受體拮抗劑等。
2、 使用本品後發生嚴重反應的風險很小。但是,碘造影劑可激發過敏樣反應或其它過敏反應的表現。因此應預先進行急救措施的訓練和預備必需的搶救藥物和器械以應付可能出現的嚴重反應。
3、 鑒於預試驗對有非離子型造影劑引起的過敏反應預測的準確性極低,以及預試驗本身也可能導致嚴重過敏反應,因此不見建議採用預試驗來預測碘過敏。
4、 在整個X線檢查過程中應始終保持靜脈輸液通路暢通。
5、 體外試驗中,非離子型造影劑對凝血系統的影響較離子型造影劑為輕。在施行血管造影術時,應十分小心在血管內的技術操作,不時地用肝素化的生理鹽水灌洗導管以減少與操作技術相關的血栓形成和栓塞。
6、 在用造影劑前後必須保證體內有足夠的水分。這一點尤其適合患有多發性骨髓瘤、糖尿病、腎功能不全的病人及嬰幼兒和老年人。小於1歲的嬰兒,特別是新生兒易引起電解質紊亂和血液動力學失調。對有嚴重心臟病和肺動脈高壓的病人需特別注意。因為他們易發展為血液動力學失調和心律紊亂。
7、 急性腦病、腦瘤或有癲癇病史的病人要預防癲癇發作並需特別的注意。酗酒和吸毒者其癲癇發作和神經系統反應危險性大為增加。少數病人在椎管造影后發生短暫性聽力喪失或耳聾,這可能是腰穿後腦脊液壓力下降所致。
8、 為預防使用造影劑後的急性腎功能衰竭,對已有腎功能損害和糖尿病的病人需要特別注意,因為他們的危險性較大。異型球蛋白血症(多發性骨髓瘤病和Waldenstrom巨球蛋白血症)的病人危險性也較大。
9、[u] 預防措施包括:[/u]
-鑑別有高危險因素的病人。
-確保體內有足夠的水分。如有必要,可在檢查前由靜脈維持輸液直到造影劑從腎臟清除。
-在造影劑清除之前避免任何加重腎臟負擔的腎毒性藥物、口服膽囊造影劑、動脈鉗閉術、腎動脈成形術或其它大型手術。
-延遲重複的造影檢查直到腎功能恢復到檢查前水平。
為防止乳酸性中毒。在對使用二甲雙胍的糖尿病人血管內注射含碘對比劑前,必須測定血清肌酐水平。對於[u]血清肌酐/腎功能正常的患者[/u]:在注射造影劑時必須停用二甲雙胍並在48小時內不能恢復用藥,或直至腎功能/血清肌酐達正常值。對於[u]血清肌酐/腎功能不正常[/u]的患者:必須停用二甲雙胍並將對比劑檢查推遲至48小時後。只有在腎功能/血清肌酐水平恆定後才能恢復二甲雙胍的用藥。對有些腎功能不正常或未知的急救病例,醫生必須評估使用造影劑檢查的利弊,並需採取預防措施:停用二甲雙胍,給病人充足的水分,監測腎功能和仔細觀察乳酸性酸中毒的症狀。
存在發生暫時性肝功能紊亂的潛在風險。嚴重肝腎功能不全的病人需特別注意,因為這些病人清除造影劑的時間明顯延長。血透的病人在接受造影劑檢查後應立即進行血液透析。
含碘造影劑可加重重症肌無力的症狀。嗜鉻細胞瘤病人在介入治療時應給予預防高血壓危象的α受體阻滯劑。甲亢病人也需特別注意。多髮結節性甲狀腺腫的病人在使用碘造影劑後有發展成甲亢的可能。應清楚地認識到早產兒在使用造影劑後有短暫性甲減的可能。
造影劑外滲時偶然會引起局部的疼痛和水腫,它們會逐漸消退,不留後遺症。不過,偶可見發生炎症甚至組織壞死的病例。常規處理方法為抬高患肢和局部冷敷。萬一發生隔室綜合症需手術減壓。
10、[u]觀察時間:[/u]
使用造影劑後的病人應至少觀察30分鐘以上,因為大多數的嚴重不良反應都發生在這段時間。不過,仍有發生延遲反應的可能。
11、[u]椎管內注射:[/u]
在椎管造影後,病人應休息1小時,頭、胸抬高20°。然後可小心下床行走但不要彎腰。如仍躺在床上,應保持頭胸抬高位6小時。對癲癇發作閾較低的病人在此期間應密切觀察。門診病人最初的24小時內不能獨處。
12、對駕駛和操作機器能力的影響:
在椎管內注射後24小時內不應駕駛和操作機器。
13、如所有的非胃腸道藥品本品應在使用前目檢,以檢查是否有微粒、變色及容器是否損壞。藥品應在使用前才被抽入針筒,本品每瓶本品僅供單次使用,丟棄未用部分。
孕婦及哺乳期婦女用藥
人類妊娠期間使用本品的安全性並未確立。實驗性動物研究的結果並不直接或間接表明在人類生殖、胚胎或胎兒發育中的損害作用。因為在妊娠的任何時候都應避免射線的照射,所以在考慮對妊娠婦女使用造影檢查時必須慎重權衡利弊。本品不套用於妊娠婦女除非臨床醫生認為利遠大於弊時。
造影劑在人類的乳汁中排出極少,通過胃腸道吸收的量也極少。因此對吃奶的嬰兒損害的可能性很小。
造影劑在人類的乳汁中排出極少,通過胃腸道吸收的量也極少。因此對吃奶的嬰兒損害的可能性很小。
兒童用藥
見【用法用量】項下的內容。
老年用藥
老年人在使用造影劑前後必須保證體內有足夠的水分。
藥物相互作用
1、使用含碘造影劑可能會導致短暫性腎功能不全,這可使服用二甲雙胍的糖尿病人發生乳酸性酸中毒(詳見【注意事項】項下的相關內容)。
2、二周內用血細胞介素-2治療的病人其延遲反應的危險性會增加(感冒樣症狀和皮膚反應)。
3、所有的碘造影劑都會影響甲狀腺功能的測定,甲狀腺碘結合能力下降會持續幾周。
4、血清和尿中高濃度的造影會影響膽紅素、蛋白或無機物(如鐵、銅、鈣和磷)的實驗室測定結果。在使用造影劑的當天不應做這些檢查。
5、雖然沒有明確的配伍禁忌,本品仍不應與其它藥物直接混合使用。應使用單獨的注射器。
2、二周內用血細胞介素-2治療的病人其延遲反應的危險性會增加(感冒樣症狀和皮膚反應)。
3、所有的碘造影劑都會影響甲狀腺功能的測定,甲狀腺碘結合能力下降會持續幾周。
4、血清和尿中高濃度的造影會影響膽紅素、蛋白或無機物(如鐵、銅、鈣和磷)的實驗室測定結果。在使用造影劑的當天不應做這些檢查。
5、雖然沒有明確的配伍禁忌,本品仍不應與其它藥物直接混合使用。應使用單獨的注射器。
藥物過量
臨床前的實驗數據提示本品有高度的安全範圍,在日常血管內使用時還未制定出固定的劑量上限水平。在腎功能正常的病人中全身性過量使用的可能性很小,除非病人在一個固定的時間段內接受超過2000mgl/公斤體重的劑量。檢查的持續時間很重要。因為腎臟耐受高濃度造影劑的能力有限(t1/2~2小時)。偶然的過量使用最可能發生在對兒童施行複雜的血管檢查,特別是多次反覆注射高濃度的造影劑。
一旦過量,必須馬上糾正水電解質的不平衡。連續監測腎功能3天,必要時可進行血透以清除過量的對比劑。沒有特殊的對比劑拮抗劑。
一旦過量,必須馬上糾正水電解質的不平衡。連續監測腎功能3天,必要時可進行血透以清除過量的對比劑。沒有特殊的對比劑拮抗劑。
藥理毒理
動物試驗結果表明本品對犬肝臟、腹主動脈、CT掃描影像有增強效應。另據文獻報導,本品的毒性較非離子型造影劑,如Metrizamide低;靜注造影時,大鼠、兔子及犬主要從尿中排出,小部分(大鼠5%、犬1%)從糞便中排出。尚未發現任何器官吸收的現象,也未在動物中檢測到任何代謝產物。本品蛋白結合率少於2%;犬腎動脈造影時有蛋白尿發生的現象。
藥代動力學
據報導,通過靜脈注射到體內的碘海醇,於24小時內以原狀在尿液中排出的近乎百分之百,尿液中碘海醇濃度最高的情況,出現在注射後的一小時內,沒有代謝物產生。
貯藏
不超過30℃,遮光、密閉保存。
包裝
300mgl/ml×10ml 玻璃瓶 1瓶/盒 10瓶/盒
300mgl/ml×20ml 玻璃瓶 1瓶/盒 6瓶/盒
300mgl/ml×50ml玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
300mgl/ml×75ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
300mgl/ml×100ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgl/ml×20ml 玻璃瓶 1瓶/盒 6瓶/盒
350mgI/ml×50ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgI/ml×75ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgI/ml×100ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgI/ml×200ml 玻璃瓶 1瓶/盒 6瓶/盒
350mgl/ml×200ml 聚丙烯瓶 1瓶/盒 10瓶/盒
300mgl/ml×20ml 玻璃瓶 1瓶/盒 6瓶/盒
300mgl/ml×50ml玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
300mgl/ml×75ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
300mgl/ml×100ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgl/ml×20ml 玻璃瓶 1瓶/盒 6瓶/盒
350mgI/ml×50ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgI/ml×75ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgI/ml×100ml 玻璃瓶/聚丙烯瓶 1瓶/盒 10瓶/盒
350mgI/ml×200ml 玻璃瓶 1瓶/盒 6瓶/盒
350mgl/ml×200ml 聚丙烯瓶 1瓶/盒 10瓶/盒
有效期
36個月
執行標準
國際標準YBH14102008
批准文號
300mgl/ml×10ml 國藥準字H20000591
300mgl/ml×20ml 國藥準字H20000592
300mgl/ml×50ml 國藥準字H20000593
300mgl/ml×75ml 國藥準字H20000594
300mgl/ml×100ml 國藥準字H20000595
350mgl/ml×20ml 國藥準字H20000596
350mgl/ml×50ml 國藥準字H20000597
350mgl/ml×75ml 國藥準字H20000598
350mgl/ml×100ml 國藥準字H20000599
350mgl/ml×200ml 國藥準字H20000600
300mgl/ml×20ml 國藥準字H20000592
300mgl/ml×50ml 國藥準字H20000593
300mgl/ml×75ml 國藥準字H20000594
300mgl/ml×100ml 國藥準字H20000595
350mgl/ml×20ml 國藥準字H20000596
350mgl/ml×50ml 國藥準字H20000597
350mgl/ml×75ml 國藥準字H20000598
350mgl/ml×100ml 國藥準字H20000599
350mgl/ml×200ml 國藥準字H20000600
生產企業
通用電氣藥業(上海)有限公司
核准日期
2006年10月16日
修訂日期
2009年01月22日
