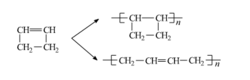定義
聚合物還存在立體異構現象。不同構型的重複結構單元沿分子鏈規則排列的聚合物稱為立構規整聚合物(stereoregular polymer),能夠生成立構規整聚合物的聚合反應稱為立體選擇聚合(stereoselective polymerization)或有規立構共聚,產生等規立構和間規立構聚合物的聚合反應分別稱為等規聚合反應和間規聚合反應。
聚合物的立構異構體
結構異構:化學組成相同,原子和基團的連線順序不同;頭-尾,頭-頭和尾-尾連線的結構異構;兩種單體在共聚物分子鏈上不同排列的序列異構。
立體異構:由於分子中的原子或基團的空間構型和構象不同而產生。分為構型異構和構象異構。構型異構又分為光學異構和幾何異構。
光學活性聚合物:是指聚合物不僅含有手性碳原子,而且能使偏振光的偏振面旋轉,具有旋光性。
烯烴聚合的立體化學
立構規整聚合物的形成與聚合反應的立體化學密切關聯,即單體和增長鏈進行加成反應時遵循一定立體化學規則。從動力學角度分析,聚合反應的立體定向程度取決於單體分子以與增長鏈末端單元相同構型進行加成反應的速率和以相反構型進行加成反應的速率之比,增長鏈活性中心是自由的還是與引發劑配位的又直接影響到兩種加成方式的相對速率。對於自由基活性中心和自由離子活性中心,這兩種加成方式都是可能的,聚合物的立構規整性取決於聚合的溫度,因為它決定著兩種加成方式的相對速率。對於引發劑配位的活性中心,某一種加成方式有可能抑止,在這種情況下配位作用制約了單體的加成方式。
1自由基聚合反應
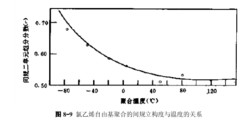
自由基聚合的增長鏈活性中心可以繞著增長鏈末端的碳-碳鍵自由旋轉,只有當單體加到鏈末端後,它的構型才能確定。形成間規立構和等規立構的速率常數分別為kr和km,兩者的比值(kr/km)決定立構規整的程度和類型。圖顯示聚氯乙烯間規二單元組的分數(r)隨溫度的變化,(r)由120℃的0.51增加到-78℃的0.67。氯乙烯在約60℃的聚合產物是完全無規的,甲基丙烯酸甲酯在100℃的聚合產物的二單元間規規整度為0.73,這是因為1,1-二取代甲基丙烯酸甲酯在聚合物鏈中鄰近單體單元的取代基之間有較大的排斥作用。
氯乙烯自由基聚合的間規立構度與溫度的關係
間規立構易於生成是聚合物鏈上取代基之間的空間和(或)靜電排斥導致的,最重要的是增長鏈末端和次末端的取代基之間的排斥作用。間規立構聚合的機理屬於聚合物鏈末端控制。
2離子型聚合
1)自由的活性中心
在溶劑化作用很強的溶劑中進行離子型鏈式聚合反應,增長鏈活性中心為被溶劑分離的離子對和自由離子,聚合物的立構控制同自由基聚合反應的情況相類似,聚合溫度的降低有利於間規立構的結構形成。
2)配位的活性中心
若聚合反應在溶劑化能力很差的溶劑中進行時,引發劑、增長鏈末端和單體之間存在著配位作用,聚合反應的立體化學與上述情況明顯不同。通常情況下,配位作用成為聚合反應立體化學的決定性因素,鏈增長反應就可能以一種(等規或間規)定位方式進行。若kr/km值趨於零,即發生等規立構聚合;在某些情況下也能發生間規聚合。
有規立構共聚的機理
1)配位引發劑的作用
配位引發劑具有兩種功能,第一是提供引發聚合反應的活性中心,另外是提供與活性中心、單體的配位能力從而控制聚合反應的立體化學。
2)立構規整聚合中的立構控制
間規立構聚合的控制:最重要的是增長鏈末端和次末端的取代基之間的排斥作用,屬於聚合物鏈末端控制。
等規立構聚合的控制:引發劑片段既同增長鏈末端又同新進入的單體分子發生配位作用,迫使每一個單體從活性中心碳原子的sp2雜化平面的同一側進攻增長鏈,因此等規立構聚合屬於引發劑定位控制。
用於等規聚合的傳統Ziegler-Natta引發劑為異相引發劑,手性來源於引發劑活性中心附近手性的晶格,均相的茂金屬引發劑的手性源於自身的分子結構,引發劑本身即為手性分子。某些手性引發劑的結構可以使單體交替地從活性中心碳原子的sp2雜化平面的兩側進攻增長鏈,由此形成間規聚合物,這種間規聚合也屬於引發劑定位控制,某些均相Ziegler-Natta引發劑和茂金屬引發劑會發生該種情況。
4)單體的極性
隨單體和引發劑的配位能力的增加,引發劑定位控制的容易程度隨著增加,而單體的配位能力首先取決於它的極性。非極性單體如乙烯、α-烯烴(丙烯和1-丁烯)和其它烯烴的配位能力很差,需要使用立體定向能力很強的引發劑才能進行等規立構聚合,如傳統的非均相Ziegler-Natta引發劑。極性單體如丙烯酸酯、甲基丙烯酸酯和乙烯基醚有很強的配位能力,實現等規立構聚合只要使用可溶性引發劑才可能得到間規聚合物。苯乙烯和1,3-二烯的聚合情況處於極性單體和非極性單體之間,使用均相和非均相Ziegler-Natta引發劑均都可使單體發生等規聚合。
1,3-二烯烴的有規立構共聚
1 )自由基聚合
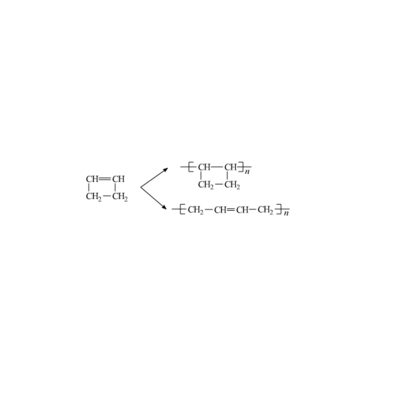
1,4-聚合比1,2-和3,4-聚合優先,反式1,4-聚合優於順式1,4-聚合。1,3-二烯烴聚合時,自由基在末端單體單元的C2和C4間離域,因為C4的空間位阻比C2的小,所以1,4-增長比1,2-增長占優勢。
反式1,4-聚合優於順式1,4-聚合的原因為反式1,4-聚合物具有更高的穩定性。
2 )陰離子聚合
產物的結構取決於增長鏈活性中心是自由的、還是與反離子配位的。丁二烯在極性溶劑中,通過自由陰離子或溶劑隔離的離子對聚合,1,2-聚合的傾向優於1,4-聚合。在非極性溶劑中,1,4-聚合傾向增加。當反離子為配位能力最大的鋰離子時,順式1,4-聚合更易於發生。
3 )陽離子聚合
1,3-二烯烴的陽離子聚合,其產物一般為低分子量的環狀結構,沒有什麼實際套用價值。
其它單體的有規立構共聚
烴類單體
1)1,2-二取代烯烴和環烯烴
1-氘代丙烯和環烯烴可聚合。由於環張力的存在,環烯烴易於發生聚合,引發劑可為Ziegler-Natta引發劑或者茂金屬引發劑。環烯烴有兩種可能的聚合方式,雙鍵聚合或開環聚合(烯烴易位)反應。環丁烯的雙鍵聚合產物為聚(1,2-亞環丁基),它有四種異構體;開環聚合產物存在順式和反式兩種異構體。
使用含鈦和釩的引發劑進行環戊烯聚合,聚合物同時含兩種類型的結構單元;用含鉬、鎢和鋰的引發劑只發生開環聚合。環己烯不能聚合,只有當環己烯基作為雙環體系的部分時(如冰片烯)才能發生聚合。環庚烯以及更大的環烯只發生開環聚合。
2)炔烴
使用四異丁氧基鈦/三乙基鋁(Ti(i-BuO)4/Al(C2H5)3)等Ziegler-Natta引發劑可使乙炔聚合生成聚乙炔。–18℃聚合,聚乙炔順式結構單元含量為90%;100℃聚合,反式結構單元含量超過90%。
3)苯乙烯
非均相的Ziegler-Natta引發劑,可進行立構選擇度超過95~98%等規立構聚合;高間規度(>95~98%)聚苯乙烯可由可溶性鈦引發劑(如CpTiCl3和CpTiCl2)和多種茂鈦/MAO引發劑獲得。