簡史,理化性質,結構,摻雜,溶解性,導電性,電致變色性,光學性質,表征,合成,化學氧化法,電化學聚合法,其他合成方法,聚合機理,影響因素,套用,塗料,電池,吸波材料,感測器,導電纖維,其他,
簡史
1826年,德國化學家Otto Unverdorben通過熱解蒸餾靛藍首次製得苯胺(aniline),產物當時被稱為“Krystallin”,意即結晶,因其可與硫酸、磷酸形成鹽的結晶。1840年,Fdtzsche從靛藍中得到無色的油狀物苯胺,將其命名為aniline,該詞源於西班牙語的añil(靛藍)並在1856年用於染料工業。而且他可能製得了少量苯胺的低聚物,1862年HLhetbey也證實苯胺可以在氧化下形成某些固體顆粒。但由於對高分子本質缺乏足夠的認知,聚苯胺的實際研究拖延了幾乎一個世紀,直到1984年,MacDiarmid提出了被廣泛接受的苯式(還原單元)-醌式(氧化單元)結構共存的模型。隨著兩種結構單元的含量不同,聚苯胺處於不同程度的氧化還原狀態,並可以相互轉化。不同氧化還原狀態的聚苯胺可通過適當的摻雜方式獲得導電聚苯胺。
不同氧化態聚苯胺之間的可逆反應圖冊參考資料。
理化性質
結構
聚苯胺的實際合成與結構研究始於20世紀初,英國的Green和德國的Willstatter兩個研究小組採用各種氧化劑和反應條件對苯胺進行氧化,得到一系列不同氧化程度的苯胺低聚物。Willstatter將苯胺的基本氧化產物和縮合產物通稱為苯胺黑。而Green分別以H
2O
2,NaClO
3為氧化劑合成了五種具有不同氧化程度的苯胺八隅體,並根據其氧化程度的不同分別命名為全還原式(leucoemeraldine)、單醌式(protoemeradine)、雙醌式(emeraldine)、三醌式(nigraniline)、四醌式即全氧化式(pernigraniline)。這些結構形式及命名有的至今仍被採用。1968年,Honzl用縮聚方法合成了苯基封端的聚苯胺齊聚物,同年Surville合成了聚苯胺半導體並提出可能的結構形式,而聚苯胺的結構正式為人所認同是在1984年,MacDiarmid提出了聚苯胺可相互轉化的4種形式,並認為無論用化學氧化法還是電化學方法合成的導電聚苯胺均對應於理想模型。中科院長春應化所的王佛松等人通過分析聚苯胺的IR和喇曼光譜,確認了醌環的存在並證明了苯、醌環的比例為3:1,MacDiarmid等人據此修正之前的模型,概括出了聚苯胺結構。

聚苯胺氧化態結構
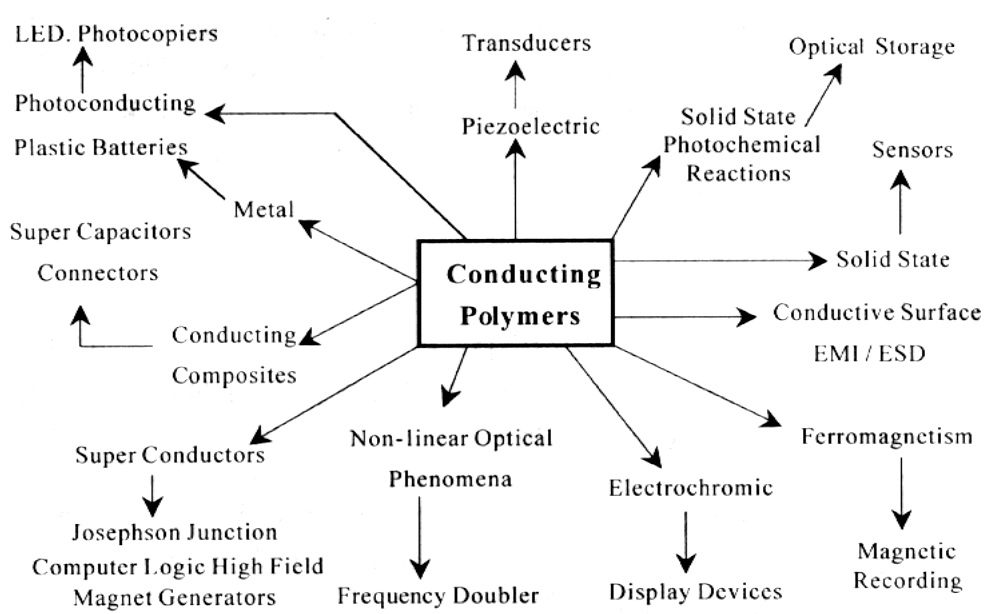
導電高分子用途
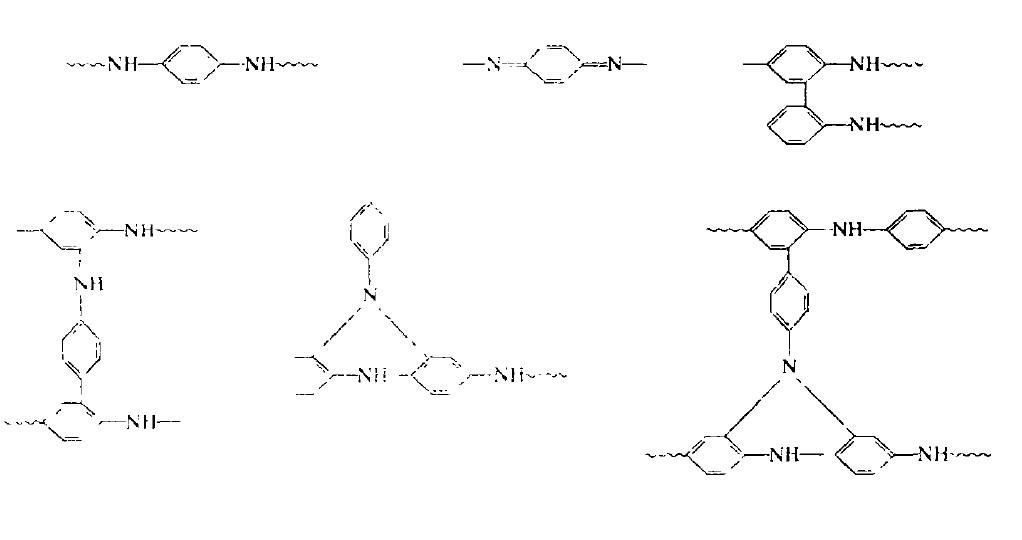
surville提出的聚苯胺結構式
聚苯胺摻雜產物的結構,主要由極化子晶格模型和四環苯醌變體模型進行解釋。聚苯胺的主要摻雜點是亞胺氮原子。質子攜帶的正電荷經分子鏈內部的電荷轉移,沿分子鏈產生周期性的分布。且苯二胺和醌二亞胺必須同時存在才能保證有效的質子酸摻雜。質子摻雜是聚苯胺由絕緣態轉變為金屬態的關鍵。本徵態的聚苯胺(PAn)是絕緣體,質子酸摻雜或電氧化都可使聚苯胺電導率提高十幾個數量級。摻雜態聚苯胺結構中x表示摻雜程度,由摻雜來決定;y表示氧化程度,由合成來決定;A表示質子酸中的陰離子,由摻雜劑決定。然而聚苯胺的摻雜過程與其他導電高分子的摻雜不同,通常導電高分子的摻雜總是伴隨著其主鏈上電子的得失,而聚苯胺

摻雜態聚苯胺結構

極化子晶格模型
在用質子酸摻雜時,電子數不發生變化。在摻雜過程中H+首先使亞胺上的氮原子質子化,這種質子化使得聚苯胺鏈上摻雜段的價帶上出現了空穴,即P型摻雜,形成一種穩定離域形式的聚翠綠亞胺原子團。亞胺氮原子所帶的正電荷通過共軛作用沿分子鏈分散到鄰近的原子上,從而增加體系的穩定性。在外電場的作用下,通過共軛π電子的共振,使得空穴在整個鏈段上移動,顯示出導電性。完全還原型(y=1)的全苯式結構(Leucoemeraldine base)和完全氧化型(y=0)的全醌式結構(Pernigraniline)都為絕緣體,無法通過質子酸摻雜變為導體,在0

中間氧化態聚苯胺結構
有人用量子化學算出了中間氧化態聚苯胺的結構。各個芳香環均偏離基準面,屬於反式構型,是一個不完全的鋸齒狀線形結構。進一步研究證實,
摻雜態聚苯胺具有與
本徵態聚苯胺類似的構型。
摻雜
物質的電學性質取決於其能帶結構,物質的能帶是由各分子或原子軌道重疊而成,分為價帶和導帶。通常禁頻寬度>10.0 eV時,電子很難激發到導帶,物質在室溫下顯絕緣性;而當禁頻寬度為1.0eV左右時,電子則可通過熱、振動或光等方式激發到導帶,成為半導體。導電高分子都有一個較長的P-電子共軛主鏈,因此又稱為共軛高分子。P-電子共軛體系的成鍵和反鍵能帶之間的能隙較小,約為1~3eV,接近於無機半導體中的導帶的價帶能隙。進行摻雜可使其電導率增加甚至十幾個數量級,接近於金屬電導率。摻雜來源於半導體化學,是指在純淨的無機半導體材料,如矽、鍺或鎵中,加入少量具有不同價態的第二種物質,以改變半導體材料中的空穴和自由電子的分布狀態。導電高分子的摻雜不同於無機半導體的摻雜。無機半導體為原子的替代和鑲嵌,而導電高分子的摻雜則常伴隨著氧化還原過程。對於無機半導體,摻雜劑可以嵌入到其晶格中,而導電高分子經摻雜後主鏈會發生變形和位移,但摻雜離子不能嵌入主鏈中去,只能存在於高分子鏈與鏈之間。無機半導體摻雜後形成電子和空穴兩種載流子;而對於導電高分子,廣為接受的載流子形式有孤子(soliton)、極子(polaron)、雙極子(bipolaron)等,這些載流子與高分子鏈上共軛P-電子緊密相關,而摻雜離子是作為對離子存在的。

DBSA摻雜PAn的TEM照片
從摻雜量上來看,導電高分子的摻雜量很大,可達一半以上,而無機半導體的摻雜量極低,僅為萬分之幾。另外,在導電聚合物中存在脫摻雜過程,摻雜/脫摻雜過程是可逆的,而無機半導體通常無法實現可逆的脫摻雜。聚苯胺的質子酸摻雜聚苯胺與質子酸反應,電導率大大提高,再與鹼反應則又變為絕緣狀態,即為質子酸摻雜和反摻雜。聚苯胺的摻雜機制同其他導電高分子的摻雜機制不同,那些高分子摻雜總是伴隨著主鏈上電子的得失,而聚苯胺的質子酸摻雜沒有改變主鏈上的電子數目,只是質子進入高分子主鏈上才使鏈帶正電,為維持電中性,陰離子也進。半氧化型半還原型的本徵態聚苯胺可進行質子酸摻雜,全氧化型聚苯胺可進行離子注入還原摻雜。全還原型聚苯胺只能進行碘摻雜和光助氧化摻雜。MacDiarmid提出當用質子酸進行摻雜時,亞胺基上的氮原子優先發生質子化,酸中的氫質子與氮原子結合形成價電子離域到大分子結構中形成共軛大P鍵,使聚苯胺的導電性能提高。

不同氧化程度聚苯胺摻雜方式
聚苯胺除了質子酸摻雜外,還可以進行光誘導摻雜、離子注入摻雜及電化學摻雜等。光誘導摻雜又稱/光助氧化摻雜,是在特定波長的光照射下,使某物質釋放質子作為聚苯胺的摻雜劑進行反應。研究表明,該摻雜是聚苯胺塗層在金屬表面能發揮防腐作用的原因之一。有人通過紫外光加速VC-MAC(Vinylidene Chloride and Methyl Acrylate)釋放質子完成了聚苯胺的光誘導摻雜。而使用離子注入摻雜將K+離子注入全氧化態聚苯胺中可以發生還原摻雜,離子注入區呈現n型半導體特性。當有40keV K束注入後,聚苯胺薄膜的電導率隨著劑量的增加而迅速增加。在電極表面發生的共軛高分子的摻雜為電化學摻雜。通過改變電極電位使塗覆在電極表面的聚合物膜與電極之間發生電荷轉移,即可完成摻雜過程。電化學摻雜可以實現許多化學摻雜法無法實現的摻雜反應,也可以通過控制高分子與電極之間的電位差來改變摻雜程度,且摻雜與脫摻雜是一個完全可逆的過程,該過程中無需除去任何化學產物。
溶解性
聚苯胺由於其鏈剛性和鏈間強相互作用,使它的可溶性極差,在大部分常用的有機溶劑中幾乎不溶,僅部分溶於N,N-二甲基甲醯胺和N-甲基吡咯烷酮,這就給表征帶來一定的困難,並且極大地限制了聚苯胺的套用。通過結構修飾(衍生物、接枝、共聚)、摻雜誘導、聚合、複合和製備膠體顆粒等方法獲得可溶性或水溶性的導電聚苯胺。如在聚苯胺分子鏈上引入磺酸基團可得到水溶性導電高分子。
不過聚苯胺溶液即使在很低的濃度(<5%)下也有較強的凝膠化傾向,在紡絲溶液所需要的高濃度(>20%)下,凝膠化傾向變得更加明顯。以NMP為溶劑溶解高分子質量的聚苯胺,並加入二甲基氮丙啶作為凝膠抑制劑,可獲得穩定溶液,這是因為二甲基氮丙啶破壞了分子鏈間的氫鍵,阻礙了凝膠作用。但這種溶劑價格昂貴,實用性前景不佳。
導電性
聚苯胺的導電性受pH值和溫度影響較大,當pH>4時,電導率與pH無關,呈絕緣體性質。
電導率與溫度在一定溫度範圍可認為隨著溫度的升高其電導率增大。在一定pH值下,隨電位升高,電導率逐漸增大,隨後達到一個平台。但電位繼續升高時,電導率卻急劇下降,最後呈現絕緣體行為。掃描電位的變化反映在聚苯胺的結構上,說明聚苯胺表現的狀態中,最高氧化態和最低還原態均為絕緣狀態,而只有中間的半氧化態呈導電性。
另外,電導率較高的樣品溫度依賴性較弱,而電導率較低的樣品溫度依賴性較強。聚苯胺的電導性不僅與主鏈結構有關,而且與取代基及取代位置有關。苯環上取代的聚苯胺由於取代基增大了苯環間的平面扭曲角,使主鏈上的P電子定域性增強,致使高分子的電導率降低。而在胺基氮原子上取代的苯胺衍生物電導率和其烷基取代基的長短有關,即取代基越長,產物的分子量越低,在有機溶劑中的溶解度越大,但電導率隨之下降。芳香基取代的聚苯胺的電導率高於烷基衍生物的電導率。有人還嘗試碳納米管摻雜聚苯胺,結果表明碳納米管的摻入可以有效地提高聚苯胺材料的電性能,但對光性能有著相反的影響。
電致變色性
電致變色是指在外加偏電壓感應下,材料的光吸收或光散射特性的變化。這種顏色的變化在外加電場移去後仍能完整地保留。聚苯胺的一個重要特性就是電致變色性,當電位在-0.2~+1.0V之間時,聚苯胺的顏色隨電位變化而變化,由亮黃色(-0.2V)變成綠色(+0.5V),再變至暗藍色(+0.8V),最後變成黑色(+1.0V),呈現完全可逆的電化學活性和電致變色效應。當電位變化範圍縮小到-0.15~0.4 V時,其電致變色的循環次數可達1,000,000次以上,回響時間在100 ms以內。
聚苯胺分子主鏈上含有大量的共軛P電子,當受強光照射時,聚苯胺價帶中的電子將受激發至導帶,出現附加的電子-空穴對,即本徵光電導,同時激髮帶中的雜質能級上的電子或空穴而改變其電導率,具有顯著的光電轉換效應。而且在不同的光源照射下回響非常複雜且非常迅速。在雷射作用下,聚苯胺表現出高非線性光學特性,可用於信息存貯、調頻、光開關和光計算機等技術上。

聚苯胺XRD
三階非線性光學效應主要來自載流子自定域而形成的激子傳輸,並且主要依賴於摻雜度、聚合條件以及主鏈的構相和取向、共軛長度、取代基種類等,不同的氧化態和摻雜度的聚苯胺具有不同的三階非線性光學係數。
聚苯胺的表征手段有電導率測量、TG-DTA、XRD、FTIR、UV-vis、XPS、TEM和SEM等。其中,TG-DTA測定複合前後的熱穩定性變化,XRD測定複合前後的晶型變化,FTIR測定複合前後的官能團變化,UV-vis可表征NCs結構及PAn摻雜狀態的變化,XPS結合能可表征NCs中各元素化學態的變化和摻雜劑對N結合能的影響,TEM和SEM直觀顯示出NCs的形貌;而根據聚苯胺的特殊功能,又有特殊的表征手段,如通過電化學阻抗譜和陽極極化曲線表征防腐蝕性能,通過循環伏安法表征電極性能,通過磁化係數、電子順磁共振技術、比飽和磁化強度、SQUID表征磁性能等。各表征手段中,以TEM和SEM的形貌表征最為直觀。
聚苯胺紫外光譜圖冊參考資料。

聚苯胺拉曼光譜
常用的聚苯胺合成方法有化學氧化合成與電化學合成。化學氧化合成法適宜大批量合成聚苯胺,易於進行工業化生產;電化學合成法適宜小批量合成特種性能聚苯胺,多用於科學研究。
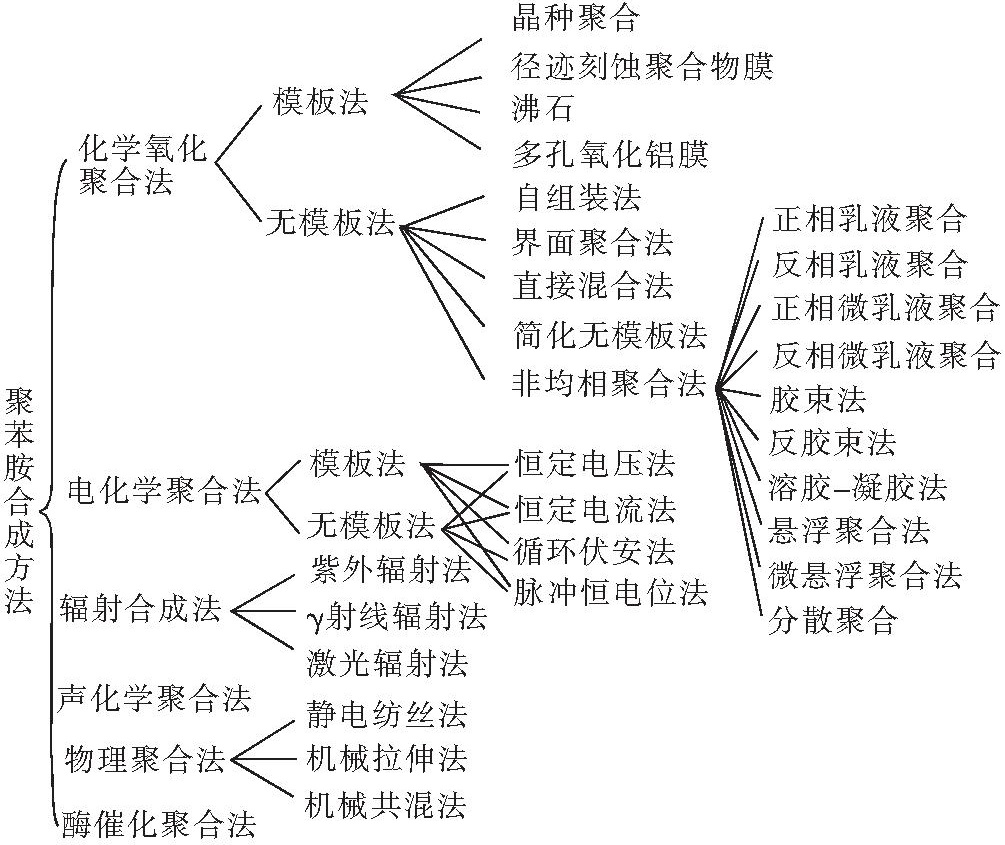
聚苯胺合成方法
化學氧化法通常是在酸性介質中,採用水溶性引發劑引發單體發生氧化聚合。合成主要受反應介質酸種類及濃度、氧化劑種類及濃度、苯胺單體濃度、反應溫度和反應時間等的影響。所用的引發劑主要有(NH4)2S2O8、K2Cr2O7、KIO3、FeCl3、H2O2、Ce(SO4)2、MnO2、BPO(過氧化苯甲醯),其中(NH4)2S2O8由於不含金屬離子,氧化能力強,後處理方便,是最常用的氧化劑。也有用(NH4)2S2O8和碳酸酯類過氧化物組成複合氧化劑。而以Fe2+為催化劑和H2O2為氧化劑可合成高溶解性的聚苯胺。
聚苯胺在酸性介質中合成的同時可能被摻雜。鹽酸摻雜雖然可使聚苯胺獲得較高的導電率,但由於HCl易揮發,容易發生去摻雜;而用H2SO4、HClO4等非揮發性的質子酸摻雜時,在真空乾燥下它們會殘留在聚苯胺的表面,影響產品的質量。從套用的角度考慮,有機質子酸摻雜的聚苯胺具有更廣闊的套用前景,十二烷基磺酸、十二烷基苯磺酸、樟腦磺酸、萘磺酸以及2,4-二硝基萘酚-7-磺酸(NONSA)等作為酸性介質的同時又可作為摻雜劑,可獲得功能質子酸摻雜的聚合物。這是提高摻雜態聚苯胺穩定性和溶解性的重要手段之一。
化學氧化法所得到的高分子溶液可通過流涎法來製備大面積自撐膜,適用於製備大構件元件和進行結構剪裁,並可通過選用合適的氧化還原劑來調節氧化態。常用的化學聚合方法主要有溶液聚合、乳液聚合、微乳液聚合、模板聚合和酶催化法等。不使用模板的方法也可以叫自組裝法(self-assembled method, SAM)。
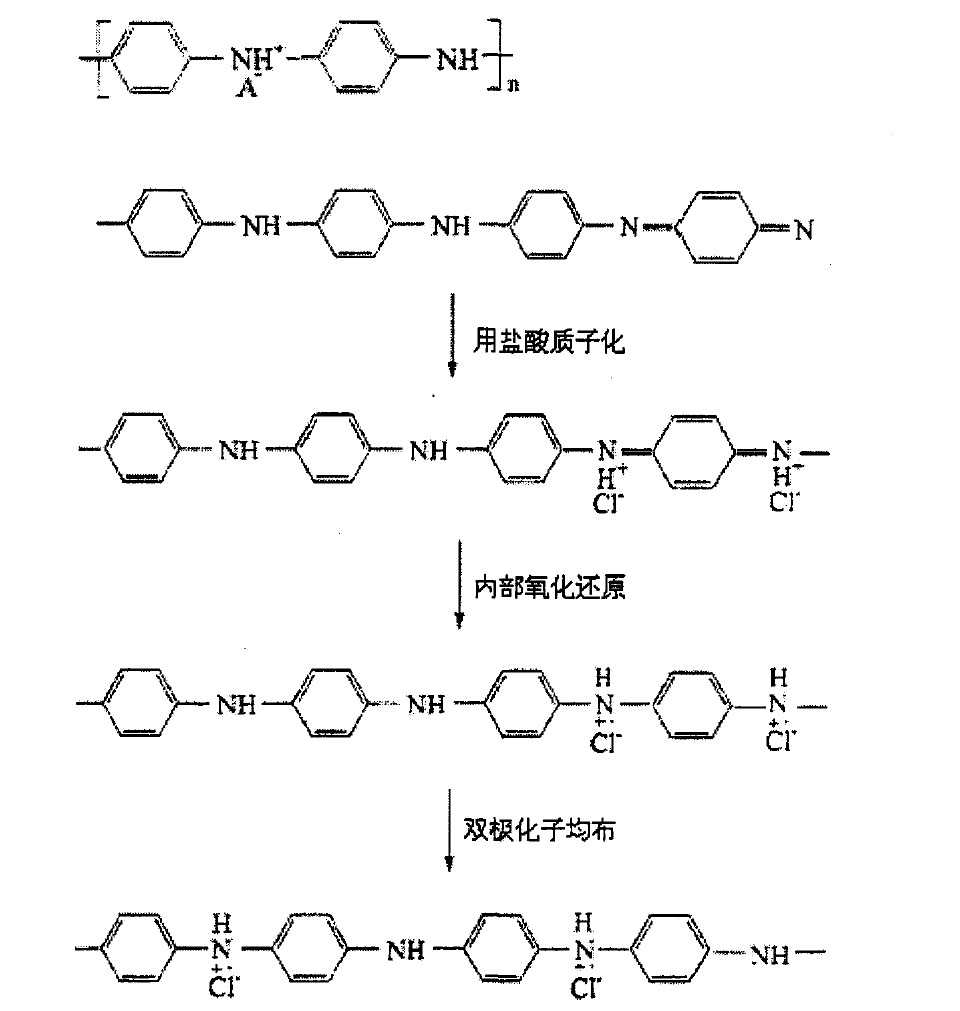
中間氧化態聚苯胺質子酸摻雜過程
溶液聚合
通常採用鹽酸、硫酸或高氯酸水溶液為介質,將引發劑溶液緩慢滴入單體溶液中引發聚合,產物易於純化;缺點是聚合過程影響因素多,分子量分布較寬,所得產品在導電率、溶解性以及熔融加工性等方面均有缺陷。一般溶液法合成路線為:取定量的苯胺單體滴入鹽酸稀溶液,再向其中緩慢滴入引發劑,如要求較高質量可通N2保護,低溫攪拌,反應結束後直接過濾、洗滌、乾燥後即得聚苯胺產品。
非均相聚合
非均相聚合通常是先將反應單體分散在水溶液中並利用機械攪拌或超音波振盪等方法,使單體形成具有一定直徑的液滴,再利用表面活性劑改性,使形成的液滴能穩定懸浮分散於溶液中。鏈反應引發劑通常溶解於連續相中,而聚合反應則被限制在液滴中進行,從而實現對產物尺寸和形貌的控制。非均相聚合法可分為乳液聚合、膠束聚合、懸浮聚合、分散聚合和溶膠-凝膠聚合等。根據乳液滴或懸浮微粒的尺寸,又可分為乳液聚合、微乳液聚合、懸浮聚合和微懸浮聚合。
乳液聚合
乳液聚合能獲得較大分子量,聚合過程中使用較低的氧化劑(引發劑)用量,優點在於聚合熱有效分散於水相,避免局部過熱,體系黏度變化小,而且其溶解性、分子量、熱穩定性及結晶形態方面的性能都明顯優於溶液聚合;但乳液聚合體系中乳化劑的濃度大,不易完全去除,給產物的純化不利,並且需要大量的有機溶劑和沉澱劑,製備成本較高。經典乳液聚合法為:採用
十二烷基苯磺酸(DBSA)作為乳化劑,同時加入水、二甲苯及苯胺,加入過硫酸銨引發反應,反應一定時間加入丙酮使PAn/DBSA 沉澱,洗滌、乾燥即可得到聚苯胺產物。多用十二烷基苯磺酸是因為它在反應體系中既是乳化劑又能提供酸性條件,還會以摻雜酸進入聚苯胺分子。

聚苯胺四種方法製備後的電鏡圖
微乳液聚合
微乳液是一種外觀透明或半透明、低黏度的熱力學穩定體系,其分散液滴小於100nm。可分成反相微乳液(W/O)、雙連續相微乳液和正相微乳液(O/W,其實正向乳液聚合就是一般意義上的乳液聚合,但因為在微乳液中反相聚合用的較多,正相反而顯得另類)。尤其是反相微乳液聚合已經越來越多地用於製備聚苯胺納米粒子,其粒徑可達10nm,而且分布較均一。反相微乳液聚合中的水油比是製備的關鍵的因素,能影響到粒子的大小和形態。一般隨水油比的增大,納米粒子直徑逐漸增大。
微乳液聚合被認為是最理想的聚苯胺合成方法之一。該法反應條件容易控制、產物粒徑均勻,而且因其粒徑都在納米級別,從而使產物具有了納米粒子的特性。所得聚苯胺產物的電導率、產率和溶解性均有提高,且其鏈結構規整性好、結晶度高。
反相微乳液聚合製備的聚苯胺粒徑小,導電性和結晶度也較好。但有時其粒子形狀會發生從球形到針形乃至薄片形的轉化。合成聚苯胺方法為:向HCl溶液中加入過硫酸銨、SDBA、丁醇(助乳化劑),這樣的混合液一經攪拌很容易配成透明的微乳液,接著往上述乳液中滴加一定量的苯胺單體,在室溫下持續攪拌反應24 h,破乳即得聚苯胺。
與反相微乳液不同,利用O/W微乳液(正相微乳液)製備納米粒子的例子並不多。這種方法可以得到分散在水相中的憎水高分子納米顆粒,其優點是快速聚合和可以形成分子量很高的聚合物。在O/W微乳液體系中乳化劑及助乳化劑的濃度很高,水溶性引發劑存在於水連續相中,苯胺單體濃度很低,主要被增溶於微乳液液滴內,極少量存在於水連續相中。在微乳液聚合過程中,溶解於水中的活性基團會迅速被膠束中的單體捕捉而引發聚合。因膠束數量很大,故聚合反應速率很快。典型的聚苯胺正相微乳液聚合過程為:將苯胺、十二烷基硫酸鈉和鹽酸攪拌混合,滴加APS溶液,整個聚合過程應控制在20℃,反應持續12 h後,破乳即可。有報導電導率達9.1S/cm。
模板聚合
具有特殊形貌與功能的聚苯胺的設計與合成一直是聚苯胺研究的熱點之一。所採用的主要是模板聚合法。這也是最有效、最簡便的製備納米結構的方法之一。在反應體系中加入沸石、多孔膜、多孔氧化鋁膜等作為模板,使聚合反應發生在模板孔洞中實現結構有序排列的方法叫做硬模板合成,它可以通過調節模板孔洞尺寸來改變產物的直徑及長度,可控性較好,但由於需要分離模板以及在分離時可能會破壞高分子結構或形成額外的共聚結構而限制了其套用。
採用模板法合成聚苯胺納米材料的一般步驟為:先將模板(多孔氧化鋁膜、沸石和多孔膜等)浸入溶有苯胺單體的酸性溶液中,再通過氧化劑(APS和KPS等)、電極電位或其他方式引發聚合鏈反應。反應進行一段時間後,模板的孔徑中會生成直徑略小的聚苯胺納米材料。模板法的優點是產物的形貌和尺寸易於控制,有效地防止了分子鏈間的相互作用、交聯以及結構缺陷的產生。用做聚苯胺合成的模板主要是膠束和反膠束。膠束聚合多採用陰離子型表面活性劑,尤其是能自摻雜的表面活性劑,但產品粒度不均,導電率也相對較低。研究表明反應物在膠束中的位置是影響反應速率、選擇性以及產率的重要因素之一,而苯胺的聚合發生在膠束/水的界面上,生成的聚苯胺顆粒以靜電斥力吸附或嵌入表面活性劑分子而得以穩定。
模板聚合的優勢之一在於有可能合成結構單一的聚苯胺,即所謂的模板導向聚合,在反應體系中加入聚陰離子電解質,在反應過程中,模板在促使苯胺單體對位取代以保證獲得頭-尾聚合的同時,為聚苯胺的摻雜提供補償離子和使聚苯胺具有水溶性。這也叫做軟模板合成或自組裝方法。用作軟模板的有表面活性劑和有機摻雜劑,其原理是可在水溶液中自組裝成具有特定形貌的有序結構,但是該方法在需要使用結構相對複雜、體積相對龐大的特殊功能性摻雜劑,可能會影響產物的結構及性能,且不利於大規模的合成。
有一個較新的趨勢是使用酶,主要用過氧化氫酶(辣根過氧化氫酶,horseradish peroxidase,HRP)來催化過氧化氫的分解,利用過氧化氫氧化使苯胺聚合。但由於聚合是在水體系中進行,而聚苯胺不溶於水,因此很快會從水中析出,導致僅能得到分子量很低的寡聚體。其他可作為酶催化的模板有聚苯乙烯磺酸鈉(SPS)和聚乙烯磺酸鈉(PVS)等。
模板合成麻煩之處在於需要用鹼液等試劑移除模板,模板的溶解會導致孔徑中的納米材料因失去支撐而團聚,而且鹼性環境會導致聚苯胺解摻雜,改變產物的原有形貌。有人嘗試選取萘磺酸(NSA)作為模板,因為NSA在作為模板的同時又作為摻雜劑進入反應產物中,並不需要在反應結束後除去。還有人使用陽極氧化鋁(AAO)作為模板,在其孔隙中合成的聚苯胺納米纖維具有良好的取向性、規整度和力學性能。這主要是由於AAO的孔隙是定位取向的,聚苯胺沿著孔壁生成所致。
界面聚合
2003年首先採用此法合成了聚苯胺納米纖維。界面聚合(interfacial polymerization)利用油/水界面將苯胺與氧化劑分離,苯胺單體溶解於有機相中(如CCl4,CS2,苯和甲苯等),氧化劑和摻雜酸(如HCl,HNO3和H2SO4等)溶解於水相中,二者在相界面接觸並發生氧化反應。隨著反應的進行,在相界面處,反應物濃度不斷降低,促使未反應的苯胺和氧化劑由於濃度差而不斷擴散至相界面,從而保證反應的連續進行,直至反應物消耗完畢。兩相界面既是苯胺與氧化劑的接觸面又是反應面,從而控制了聚合反應發生的劇烈程度,避免了苯胺的過度氧化和二次生長,有利於規整形貌的聚苯胺的合成。界面聚合的優點包括:產物的合成和純化較為簡便,無需移除模板;產物形貌規整,一致性很高;聚合反應的規模可控,重現性好。
在界面聚合過程中,通過加入一定量的表面活性劑,可以控制合成的聚苯胺纖維的直徑,而加入乳化劑可有效減少有機溶劑的用量,提高/油/水兩相界面面積,縮短聚合反應時間。
有人把界面聚合和傳統化學聚合相結合,提出了直接混合法(rapid mixing method, RMM)。反應在室溫下進行,且不控制反應溫度。以摻雜酸溶液作為溶劑,將苯胺和氧化劑分別配成溶液後在室溫下迅速混合,靜置反應一定時間,反應液經純化處理後,即可得到產物。
種子聚合
種子聚合法是以一定形貌的晶種作為結構引導劑,使得單體在聚合的過程中,PAn形貌的形成朝著晶種的形貌生長。在晶種法中,以纖維狀聚苯胺/無機NCs為例,少量的無機納米纖維如單層碳納米管束、V2O5的納米纖維等作為種子,採用種子聚合法合成了PAn納米複合纖維。核殼粒子的形貌由晶種粒子的形貌和HCl與苯胺單體的比決定;在強酸性介質中用親水晶種顆粒種子聚合苯胺製備了覆盆子結構的顆粒,而在中性介質中用疏水晶種顆粒種子聚合了表面平滑的顆粒。
電化學聚合法
在電場作用下使電解液中的單體在惰性電極表面發生氧化聚合,其優點是能直接獲得與電極基體結合力較強的高分子薄膜,並可通過電位控制聚合物的性質,也可直接進行原位電學或光學測定。在含苯胺的電解質溶液中,選擇適當的電化學條件,使苯胺在陽極上發生氧化聚合反應,生成黏附或沉積于于電極表面的聚苯胺薄膜或粉末。操作過程為:氨與氫氟酸反應製得電解質溶液,以鉑絲為對電極,鉑微盤電極為工作電極,Cu/CuF2為參比電極,在含電解質和苯胺的電解池中,以循環伏安法進行電化學聚合,反應一段時間後,聚苯胺便吸附在電極上,形成薄膜。與化學聚合法相比,電化學方法操作簡便,聚合和摻雜同時進行;可通過改變聚合電勢和電量控制聚苯胺膜的氧化態和厚度;所得產物無需分離步驟。
電化學法包括循環伏安法、恆電流法、恆電勢法、脈衝電流法等。其中,循環伏安法製得的聚苯胺膜質地均勻、導電性良好、氧化還原可逆性優良、膜厚易控制以及膜與基體結合牢固、可獲得自支撐膜,套用最為廣泛。聚合體系多為三電極系統,主要由電解液、工作電極、對電極、參比電極和電化學工作站組成。常用的工作電極為鉑片、陽極鋁氧化物和銦錫氧化物玻璃(ITO)等,對電極多採用鉑電極,而參比電極為飽和甘汞電極或標準Ag/AgCl電極等。電極材料、電極電位、電解質溶液的pH值及其種類對苯胺的聚合都有一定的影響。其中,電解質陰離子對苯胺陽極聚合速度有較大影響,聚合速度順序為H2SO4>H3PO4>HClO4,但所得聚苯胺結構基本相似。
苯胺在電化學聚合時顏色根據外界有所變化,在酸性溶液中是藍色的,而在鹼性溶液中陽極氧化時生成深黃色的物質。
電化學聚合中反應選擇性差,因為單體的氧化電位一般比所得高分子的可逆氧化還原電位高,因此在聚合過程中可能出現聚合物鏈的過氧化;單體聚合活性中心的選擇性較差,幾乎所有電化學聚合都存在不同程度的交聯;反應完成後從電極表面轉移聚苯胺的過程有可能導致產物形貌發生變化。此外,電化學聚合受電極面積制約,不利於大規模生產,所得產物的可加工性差、批量小。
其他合成方法
輻射合成法是通過光能或其他射線引發苯胺單體聚合。該法合成的聚苯胺形貌受輻射源的波長、照射面積和輻射形狀等因素的影響。採用紫外輻射時易得到球型形貌,而採用可見光輻射時產物則傾向於纖維形貌。
聲化學聚合法與化學氧化法類似,區別在於聲化學聚合法在滴加APS到ANI溶液中引發鏈反應時,利用超音波振盪使混合溶液充分分散並發生聚合反應。
聚合機理
由於苯胺的化學聚合速度很快,很難跟蹤和分離中間產物,而電化學聚合相對較易控制和跟蹤觀察,所以聚苯胺早期機理的研究主要建立在電化學的基礎上。一般認為苯胺的聚合是一種介於典型逐步增長與典型自由基鏈增長之間的聚合反應。由於苯胺的氧化電位遠高於二聚體,苯胺單體氧化形成二聚體是聚合反應的控制步驟;二聚體形成後,立即氧化成陽離子自由基,進一步氧化脫氫芳構化而生成三聚體;這樣重複親電取代-芳構化過程,即可使鏈增長持續進行。不過有人提出苯胺氧化到二聚體的形成並不是聚合反應中的最慢步驟,只是表現出需要最高的電化學氧化電位。速率的決定步驟是與體系平衡電位由0.40V上升到0.78V的聚合階段相關。

Gospodinova提出的苯胺化學聚合鏈增長機理
有人認為苯胺氧化聚合是按類似於縮聚反應的歷程進行,即各種陽離子自由基間縮合形成聚合物。首先苯胺氮原子失去一個電子形成自由基陽離子,與pH值大小無關;這是速率決定步驟,可通過氧化劑來加速,隨後的反應便是自動加速的。陽離子自由基存在三種共振形式,其中形式取代基誘導效應最強而位阻最弱,因此反應性最強;接著自由基陽離子在酸性介質中發生“頭-尾”偶合反應,從而形成二聚體,二聚體氧化形成新的自由基陽離子,再與單體陽離子自由基或二聚體陽離子自由基反應形成三聚體或四聚體;繼續進行縮合反應形成聚合物。
酸性溶液中製得的聚苯胺一般為墨綠色,具有較高的導電性、電化學活性和穩定性。研究表明苯胺在酸性溶液中的聚合是通過頭-尾偶合,即通過N原子和芳環上的C-4位的碳原子間的偶合,從而形成分子長鏈。而一旦反應中間體被氧化,則整個聚合反應停止。

wei提出的苯胺化學聚合反應機理
苯胺在鹼性溶液中陽極氧化時生成深黃色的物質。苯胺在鹼性溶液中氧化時生成兩種可溶性中間物,其氧化機理可能為形成的自由基在鹼性溶液中不穩定,很容易失去一個質子形成新自由基,後者在 1.1 V左右進一步氧化帶正電荷的可溶性中間物並在電極上發生聚合,還有少部分在傳遞過程中分解。
影響因素
反應溫度對聚苯胺的電導率影響不是很大,在低溫下(冰水浴)聚合有利於提高聚苯胺的分子量並獲得分子量分布較窄的產物。在過硫酸銨體系中,在一定溫度範圍內,隨著反應體系溫度升高,產物產率增加。不過苯胺聚合是放熱反應,且聚合過程有一個自加速過程。如果單體濃度過高會發生暴聚。
在一定範圍內,隨著氧化劑用量的增加,高分子產率和電導率也增加。當氧化劑用量過多時,體系活性中心相對較多,不利於生成高分子量的聚苯胺,且聚苯胺的過氧化程度增加,電導率下降。
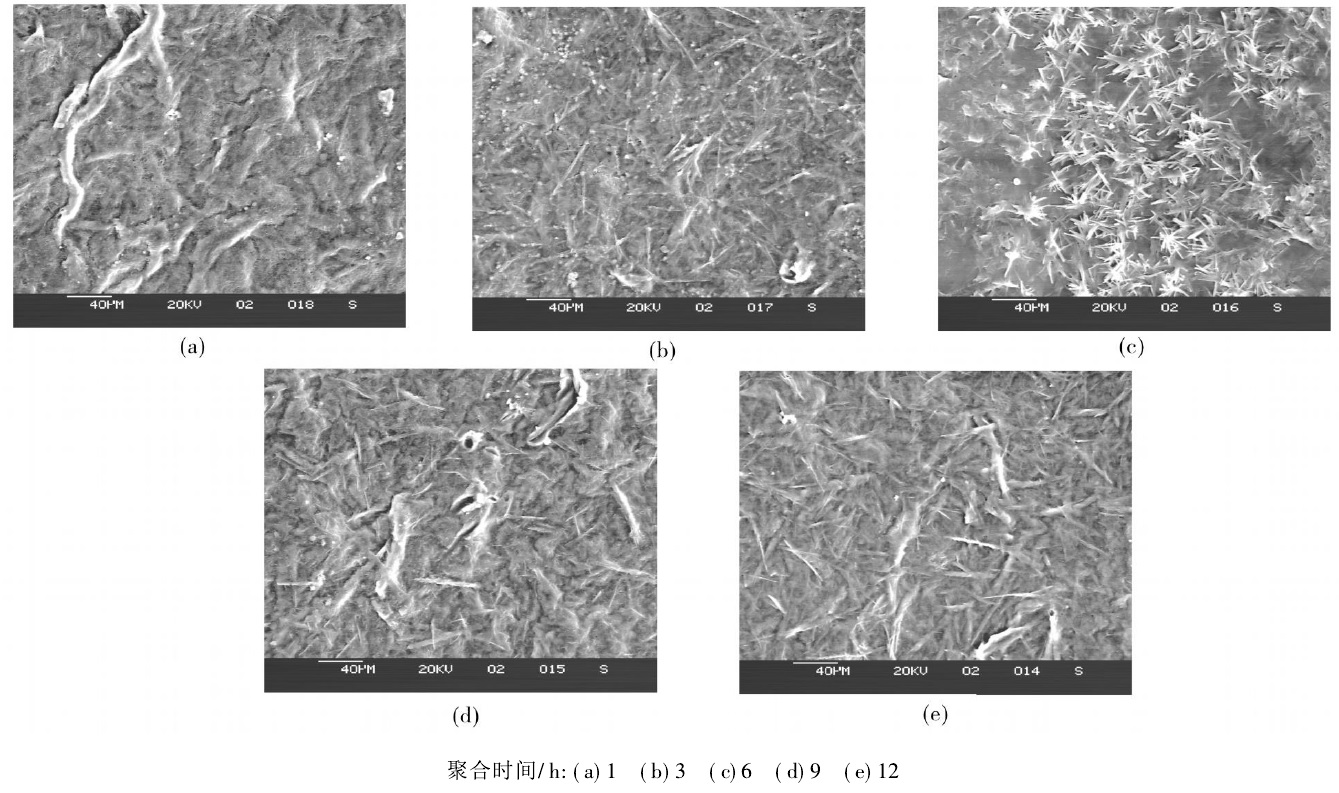
不同聚合時間PAn的SEM照片
苯胺在HCl,HBr,H2SO4,HClO4,HNO3,CH3COOH,HBF4及對甲苯磺酸等介質中聚合都能得到聚苯胺,而在H2SO4,HCl,HClO4體系中可得到高電導率的聚苯胺,在HNO3,CH3COOH體系中所得到的聚苯胺為絕緣體。非揮發性的質子酸如H2SO4,HClO4最終會殘留在聚苯胺的表面,影響產品質量,最常用的介質酸是HCl。質子酸在苯胺聚合過程中的主要作用是提供質子,並保證聚合體系有足夠酸度的作用,使反應按1,4-偶聯方式發生。只有在適當的酸度條件下,苯胺的聚合才按1,4-偶聯方式發生。酸度過低,聚合按頭-尾和頭-頭兩種方式相連,得到大量偶氮副產物。當酸度過高時,又會發生芳環上的取代反應使電導率下降。當單體濃度為0.5mol·L時,最佳酸濃度範圍為1.0~2.0mol·L。
套用
塗料
聚苯胺塗層也指塗料,是採用機械塗膜的方法在金屬,如冷軋鋼、低碳鋼、鋁、銅等表面形成均勻完整的聚苯胺防腐膜,其防腐的機理是使金屬鈍化,在金屬表面形成起保護作用的氧化層,且塗覆適合的塗層可以導致腐蝕電勢遷移,從而降低金屬的腐蝕速率。而且因其具有原料易得、合成簡單、無污染、質量輕等諸多優點,而被認為是新一代環境可接受的高效防腐塗料;但PAn不易加工成型,不溶於常規有機溶劑,且純聚苯胺對金屬的粘結性很差,且價格昂貴,利用率低,在實用化中存在一定的障礙。人們通常把聚苯胺作為防腐塗料的添加劑,使之形成聚苯胺系防腐塗料。聚苯胺塗料按物質的不同分為單一聚苯胺塗料、聚苯胺為底漆的塗料、聚苯胺與傳統塗料的共混塗料三類。
1985年,Deberry發現在不鏽鋼上電沉積的聚苯胺膜能顯著降低不鏽鋼在硫酸溶液中的腐蝕速率,其實就是單一聚苯胺塗料,即苯胺在酸溶液通過電化學聚合反應直接在金屬電極表面沉積得到聚苯胺塗層。但這種方法難以用於較大的金屬部件。
聚苯胺為底漆的塗料是指在聚苯胺塗層上塗敷傳統聚合物為面漆,與聚苯胺形成複合塗層。它的優點是不需要考慮塗料中聚苯胺的分散性,每一種塗料各自發揮作用。防腐性能則是這些作用的加和,面漆層一般起物理禁止作用。美國Los Alamos和NASA的聯合研究小組首次發現聚苯胺可作為中碳鋼的防腐塗料。
聚苯胺與傳統塗料共混塗料是指將聚苯胺粉末與常規塗料成膜物質(如環氧樹脂、醇酸樹脂等)混合後進行塗敷,可獲得聚苯胺共混防腐塗層,此方法是用於研究聚苯胺防腐性能和機理的最多的方法。它不同於聚苯胺為底漆的塗料,塗料的防腐性能是各組分有機相互作用的結果。
聚苯胺除了防腐塗料,還可以用來製備電磁干擾(EMI)禁止塗料和抗靜電塗料。高分子的導電性使得塗層對裸露的金屬區域都能起到鈍化作用,而EMI禁止的原理是:採用低阻值的導體材料,並利用電磁波在禁止導體表面的反射和在導體內部的吸收以及傳輸過程的損耗而產生阻礙其傳播的作用,當導電PAn作為導體材料時,可以在一定程度上解決金屬導電填料存在的價格昂貴、密度高、容易被氧化或腐蝕等弊端。有人以導電PAn包裹碳基材料為主要導電成分,以熱塑性樹脂為主要成膜物質製備了EMI禁止塗料。
聚苯胺防腐機理尚不明確,科研人員提出了很多理論,包括禁止機理、電場機理、雙極性塗層機理、吸附機理、陽極保護機理、摻雜劑離子緩蝕機理以及陰極保護機理等。可以肯定的是在氧化態的轉變中,聚苯胺的氧化還原電位遠高於金屬,這是聚苯胺具有金屬防腐能力的原因之一。
聚苯胺在環境pH值≥7時具有完全氧化態(LEB)和半氧化態(EB)結構,這兩種結構的聚苯胺在金屬的防護過程中,只起到一種機械隔離作用,它類似於金屬表面的非金屬塗裝保護這種形式。
當金屬表面的聚苯胺有缺損時,對該部位不起到保護作用;而當聚苯胺在環境pH值<7時,聚苯胺結構發生變化,形成聚苯胺鹽(ES)形態,此時聚苯胺具有良好的導電性和電化學活性。這種形態的聚苯胺在金屬的防護中不但具有機械隔離作用而且具有一定的催化鈍化作用。
當金屬表面的聚苯胺有缺損時,它對該部位起一種催化鈍化作用,使缺損聚苯胺塗層的金屬裸露部分在酸性條件下,發生陽極氧化反應,快速恢復表面鈍化層。
有人將聚苯胺/聚甲基丙烯酸甲酯的複合塗層材料用於低濃度氨氣的探測,根據複合材料的不同電導率可探測氨氣的極限濃度在(10~4000)×10範圍內。而當氮氣充入後,複合塗層的電導率和透光率可以迅速恢復到初始狀態,從而實現循環使用。
電池
聚苯胺具有儲存電荷的能力高、對氧和水穩定性好、電化學性能良好、密度小和有可逆的氧化/還原特性等特點,在複合物電極中既可作為導電基質又可作為活性物質,已被用於高分子鋰電池及太陽能電池等的電極材料。
用聚苯胺做成的塑膠電池不僅重量輕,且庫倫效率超過95%,它的理論能量密度可達500Wh/kg以上,是鉛酸電池(184Wh/kg)的數倍。高分子鋰電池,即以PAn及PAn複合物作電極材料的鋰離子電池,主要是利用PAn複合物在電極反應過程中摻雜/脫摻雜的可逆性來實現氧化還原反應,完成電池的充放電過程,該電池具有很高的能量密度,並突破了傳統鋰離子電池正極材料的選擇面太小的難題。
有人通過反膠束法製備了PAn/V2O5納米纖維,並將其作為鋰離子二次電池的陰極材料,對其電化學性能進行了研究。結果表明複合納米纖維比V2O5納米纖維具有更佳的循環性能,而用碳材料替代金屬鋰作為電池負極可取代金屬鋰在電極上的沉積和溶解反應,避免了在負極表面鋰的枝晶化問題,保持了鋰電池的高電壓、高比能量等優點,還大大提高了電池的循環壽命和安全性能。
高分子太陽能電池的基本機理主要是基於半導體p-n結的光生伏打效應,即在光的照射下,半導體內部產生的電子-空穴對,在靜電場的作用下發生分離產生電動勢。高分子太陽能電池因為高分子半導體材料易於製備與純化、容易加工、價格低廉,並可根據需要進行化學修飾、具有高的開路電壓、能製作大面積柔性器件等優點。
吸波材料
吸波材料的吸波原理是吸收或衰減入射電磁波,並將電磁能轉變成熱能或其它形式的能量而耗散掉。聚苯胺是一類電損耗型吸波材料,其吸波性能與其介電常數、電導率等密切相關。其中PAn具有二電子共軛體系,其導電性可以在絕緣體、半導體和金屬之間變化,且具有可分子設計和合成、結構多樣化、密度小、吸收頻頻寬、電磁參數可調、易複合加工等特點,避免了磁性金屬吸波材料抗老化、耐酸鹼能力、頻譜特性等性能差的缺點。但PAn鏈間剛性強,脆性大,將它複合後可加以改善。
有人製備了DBSA摻雜PAn/MMTNCs,在2~18GHz範圍內具有微波吸收性能,在13~14GHz範圍內反射損耗小於-10dB,在13GHz處的最大反射損耗為-10.3dB。美國等已經將其用作遠距離加熱材料,用於太空梭中的塑膠焊接技術。還把聚苯胺複合製成具有光學透明性雷達吸波材料,噴塗在飛機座艙蓋、精確制導武器的光學透明視窗上,以減弱目標的雷達回波。
但PAn很難同時滿足阻抗匹配和強吸收的特點,而將PAn與具有磁損耗吸波性能的磁性粒子複合後卻得以實現,比如當納米NiFe2O4晶體加入到PAN和石蠟的混合體系時,PAn/NiFe2O4和石蠟的復相粉體混合體系在測試頻率範圍內同時具有一定的介電損耗和磁損耗,並且其混合體系的微波吸收性能高於單獨加入PAN時的微波吸收性能。
感測器
PAn因具有良好的導電性能,可作為“分子導線”使電子在生物活性物質與電極間直接傳遞,顯著提高生物感測器的回響特性,從而製成無介體的第三代生物感測器,而且通過在合成過程中摻雜不同的陰離子,可以用於檢測不同的分析對象。有人通過滴塗法組裝了具有選擇性多巴胺生物感測器,該生物感測器在中性下可檢測出濃度為維生素C濃度1/5000的多巴胺。
還有人把聚苯胺的變色特性用於C輻射的探測,並通過對接受不同劑量輻射的聚苯胺薄膜的紫外-可見吸收光譜測定,確定了輻射劑量與吸收光譜之間的函式關係。
導電纖維
用聚苯胺製備導電纖維,不僅導電性優良持久,而且通過改變摻雜酸的濃度,很容易調節纖維的電導率,這是其它纖維所不具備的優良性質。在普通纖維中混用極少量的導電纖維,就能賦予纖維製品充分的抗靜電性能,而且抗靜電性能不會受到環境濕度的影響。有人對纖維進行氧化摻雜,製得的導電纖維的比電阻為1.05×10Ωcm。

導電纖維製備流程
製備方法主要有熔體紡絲法和原位聚合法。熔體紡絲法主要是採用聚苯胺本體紡絲或將聚苯胺與基體聚合物混合紡絲,其優點是製得的導電聚苯胺纖維有較高的電導率,但聚苯胺在普通溶劑中溶解性很差,可供選擇的溶劑極少,因此在實際生產中有很大的限制。
原位聚合法又稱現場吸附聚合法,用該法製備聚苯胺導電纖維時,聚苯胺的合成反應是在纖維的表面進行。基本流程是將基質纖維浸漬於苯胺溶液中,然後將帶有一定量苯胺單體的纖維放入氧化劑及摻雜酸的反應浴中使苯胺氧化聚合,生成的導電聚苯胺附著在纖維表面。工藝流程分別為:(1) 漂洗→烘乾→表面預處理或不處理→苯胺單體浸泡→聚合吸附→清洗→烘乾;(2) 漂洗→烘乾→表面預處理或不處理→氧化劑溶液浸泡→聚合吸附→清洗→烘乾。電學穩定性受環境溫濕度的影響。一般來說,需在織物的表面塗一層保護膜。其電導率隨時間的延長具有衰減性,並且聚苯胺沉積在織物上粗細分布不勻,引起織物電導率不勻。
該法的麻煩之處是必須保證纖維對導電聚苯胺的有效吸附,對於結構疏鬆或吸水性較好的纖維比較容易,而對於滌綸等結構緊密吸水性差的纖維就很棘手。研究表明,無機酸摻雜聚苯胺導電織物的效果優於大多數有機酸,聚苯胺複合導電滌綸織物的導電性能受洗滌液酸鹼度的影響,其中鹼性洗滌液使導電性能降低 2 個數量級,酸性洗滌液使導電性能下降1個數量級,而且聚苯胺在滌綸織物表面具有良好的附著性,且空氣穩定性好,但是鹽酸由於分子質量小易發生脫摻雜行為,空氣穩定性較差;因此鹽酸摻雜聚苯胺的脫摻雜行為是聚苯胺複合導電織物電導率隨時間衰減的主要原因。
有意思的是,原位聚合法中有研究表明,不一定是強氧化劑的氧化效果好,因為當採用過硫酸銨等強氧化劑時,氧化非常迅速,低聚物來不及向纖維滲透就進一步聚合併從溶液中沉澱出來。而弱氧化劑有效地控制了苯胺氧化聚合速度,使低聚物有充分的時間向纖維表面及內部遷移。控制氧化速度是保證纖維對聚苯胺有效吸附的關鍵。同時氧化劑濃度過高也不利於提高纖維的導電性能。
其他
PAn與磁性粒子複合,可實現電、磁性能的複合,又可通過調節各組元的組成和結構實現對複合材料電、磁性能的調節,還可彌補無機磁性材料成型加工困難的缺點,還可以作為定向集熱治療腫瘤的醫用材料使用。
PAn具有活性中心,可作為化學修飾膜材料,用貴金屬微粒,比如Pd,修飾PAn,可做催化劑使用。這種高催化活性可能來源於PAn與Pd微粒的協同效應。
由於摻雜離子在聚苯胺分子鏈之間往往形成柱狀陣列,隨著摻雜濃度的提高,後繼嵌入的摻雜離子可能進入此前形成的陣列或形成新的陣列,並導致大分子鏈相互分離。因此聚苯胺在不同氧化態下體積有顯著不同,對外加電壓有體積回響,可以用於製造人工肌肉。


















