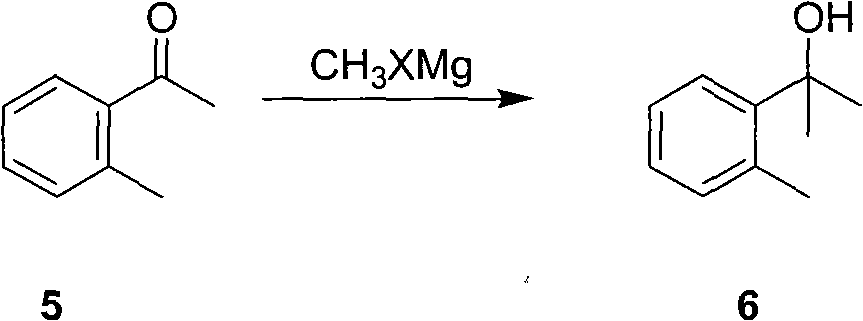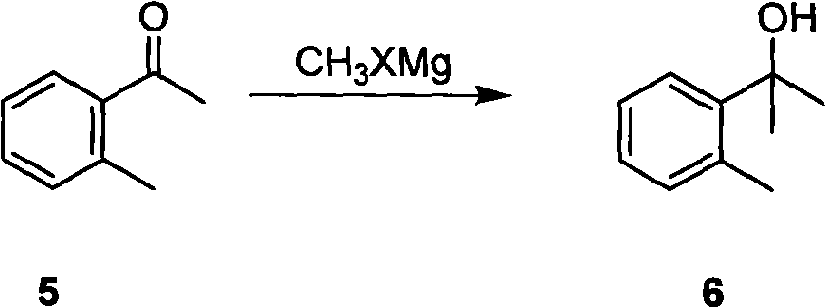專利背景
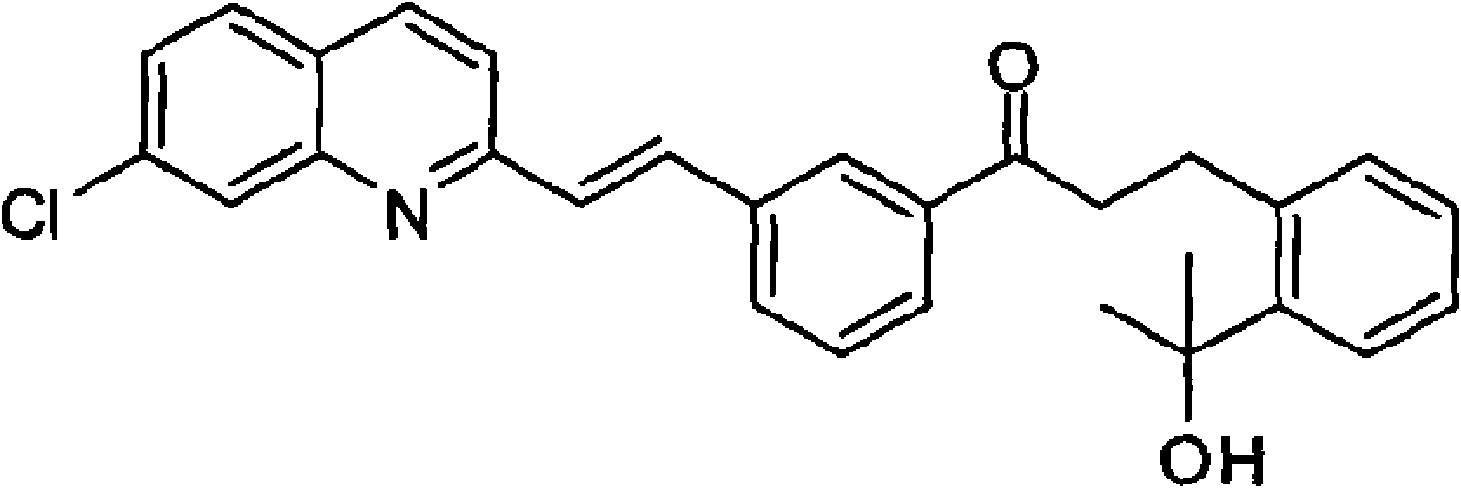
孟魯司特鈉(Montelukast Sodium)的化學名稱是:1-(((1-(R)-(3-(2-(7-氯-2-喹啉基)-乙烯基)苯基)-3-(2-(1-羥基-1-甲基乙基)苯基)丙基)硫基))甲基)環丙基乙酸鈉,結構式如下:
該化合物可以用作治療哮喘,抗過敏劑等,該化合物首先由加拿大的麥克氟羅斯特公司合成。並且由該公司在CN1061407A中公開了該化合物的結構及製備方法,在此專利中公開的合成孟魯司特鈉的方法是將2-(2-3(R)-(3-2-(7-氯-2-喹啉基)-乙烯基)苯基)-3-(羥基)丙基)苯基)丙醇與1-(巰甲基)-環丙基乙酸乙酯反應製備。
而CN1420113A中公開了另一種方法,是以2-(2-3(S)-(3-2-(7-氯-2-喹啉基)-乙烯基)苯基)-3-(巰基)丙基)苯基)丙醇與2-(1-溴甲基)-環丙基乙酸乙酯反應製備。
在CN101081834A中帶有離去基團的2-(2-3(R)-(3-2-(7-氯-2-喹啉基)-乙烯基)苯基)-3-(羥基)丙基)苯基)丙醇與1-(巰甲基)環丙基乙酸二陰離子二鋰鹽反應得到。
2009年前技術中關於孟魯司特鈉的合成,多以基本化合物2-(2-3(Rors)-(3-2(7-氯-2-喹啉基)-乙烯基)苯基)-3-(羥基)丙基)苯基)丙醇為原料,此基本化合物又是在中間體2-(2-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙基)苯甲酸甲酯或2-(2-(3-(2-(7-氯2-喹啉基)乙烯基)苯基)-3-羥基丙基)苯甲酸甲酯的基礎上合成。關於此類中間體的合成,2009年前技術中報導以下幾種途徑:
如在J.Org.Chem.(Vol.61,No.10,1996,3398-3405)中,以7-氯-2-乙烯基喹啉和2-(3-(3-溴甲基苯基)-3-氧代丙基)苯甲酸甲酯為起始原料,通過鈀催化偶聯得到2-(2-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙基)苯甲酸甲酯。
在EP480717提供的製備方法F中,是以3-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙酸乙酯與碘甲基苯甲酸甲酯反應,然後脫羧得到2-(2-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙基)苯甲酸甲酯。
在EP480717方法k中是以7-氯喹哪叮為原料和間苯二甲醛反應生成3-(2(E)-2-(7-氯喹唑啉基)乙烯基)苯甲醛,與乙烯基溴化鎂試劑進行格氏反應,然後與2-溴苯甲酸乙酯反應,得到2-(2-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙基)苯甲酸甲酯。
上述中間體的合成方法中多用到貴重的鈀金屬試劑,加大了生產成本;要么多次進行格氏反應,條件複雜苛刻,需要嚴格控制,副產物較多;同時存在生成的產物不適於長時間的放置的問題,不適於大規模生產。
發明內容
專利目的
雖然合成孟魯司特鈉中間體的方法較多,但另一類重要中間體2-(2-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙基)苯基)丙醇卻是少見,此中間體在手型還原劑的作用下,可以選擇性的得到所需要的手型母核,故此中間體具有廣泛的前景。
《孟魯司特鈉中間體的合成方法》的目的在於提供一種適合大規模生產製備的孟魯司特鈉中間體的可替代方法,具體來說,經過6步反應,可以獲得良好的收率-中間體(4)的收率可達40%和高的純度以及可靠的控制方法,主要原料間氰基苯甲醛和鄰甲基苯乙酮廉價易得。
技術方案
為達到上述目的,《孟魯司特鈉中間體的合成方法》方法採用了如下反應路線:
《孟魯司特鈉中間體的合成方法》以間氰基苯甲醛為原料和7-氯喹哪啶縮合得到中間體3-(2-(7-氯-2-喹啉基)乙烯基)苯甲氰,該化合物在空氣中穩定,可長久放置而不發生化學變化,便於儲存和運輸。然後以工業級鄰甲基苯乙酮為原料與格式試劑反應,生成2-鄰甲基苯基-2-丙醇,經二氫吡喃進行羥基保護,保護後的化合物在鹼性條件下發生羥甲基化反應,然後進行鹵化反應,生產的鹵代物在惰性溶劑中和中間體(4)縮合,然後水解得到目標產物。整個過程操作簡單,可控性強,沒有苛刻的反應條件,原料低廉,適合工業生產。
《孟魯司特鈉中間體的合成方法》採用如下技術方案:
一種合成如下結構(化合物1)的孟魯司特鈉中間體的方法,該方法包括以下步驟:
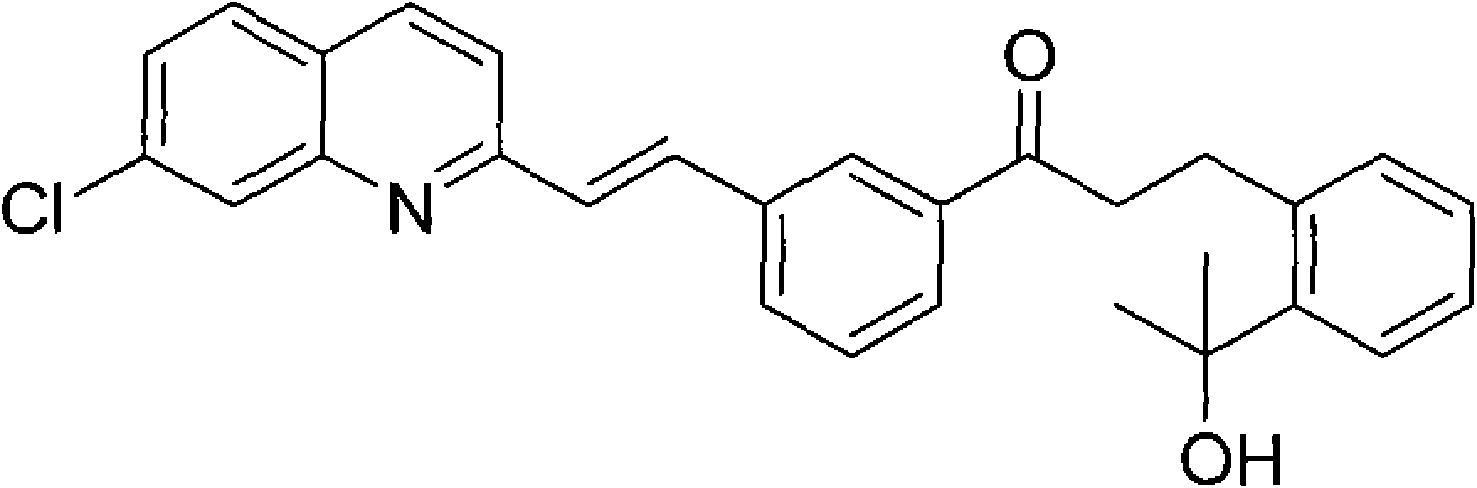
化合物1
a.將7-氯喹哪啶和3-氰基苯甲醛在乙酸酐和乙酸鈉的作用縮合下得到化合物(4)
3-(2-(7-氯-2-喹啉基)乙烯基)苯甲氰,反應如下:

該反應採用的溶劑優選二甲亞碸(DMSO)、二甲基甲醯胺(DMF)、二甲基乙醯胺(DMA)和六甲基磷醯胺的一種或一種以上的混合物,更優選DMF。反應溫度隨試劑或者溶劑的變化而變化,反應溫度為80℃~200℃,優選溫度為120~140℃。
b.鄰甲基苯乙酮在惰性溶劑中,鹵化甲基鎂的作用下生成化合物(6)2-鄰甲基苯基-2-丙醇,反應如下:
該反應所用的溶劑為苯及其同系物、四氫呋喃、2-甲基四氫呋喃、乙醚、異丙醚、乙二醇二甲醚中的一種或多種。採用的鹵化甲基鎂有氯化甲基鎂和溴化甲基鎂,TLC檢測反應終點,展開劑為:正己烷:乙酸乙酯=4:1(體積比),鑒於溴化甲基鎂比鄰甲基苯乙酮的價格要貴,反應採用苯乙酮過量,鹵化甲基鎂:鄰甲基苯乙酮=1摩爾:(1.0~1.5摩爾),反應溫度為:20℃~30℃。滴加溴化甲基鎂的溶液時,反應瓶內溫度始終保持在0℃以下。
c.化合物6在催化劑和二氫吡喃作用下生成羥基保護的化合物(7)2-(2-鄰甲基苯基丙基)四氫吡喃醚,反應如下:

該反應採用的催化劑有氫溴化三苯基磷、氫溴化三叔丁基磷、鹽酸(包括氯化氫氣體)、氫溴酸(包括溴化氫氣體)、三氯氧磷、對甲苯磺酸及其吡啶鹽、三氟化硼-乙醚中的一種或多種,優選氫溴化三苯基磷,所用的物料比為:2-鄰甲基苯基-2-丙醇:二氫吡喃:催化劑=1摩爾:2~6摩爾:0.1~1摩爾。加料過程為先加入1/2用量的二氫吡喃和氫溴化三苯基磷,反應液攪拌回流24小時後,再加入1/2用量的二氫吡喃和氫溴化三苯基磷,反應液繼續攪拌回流至結束。
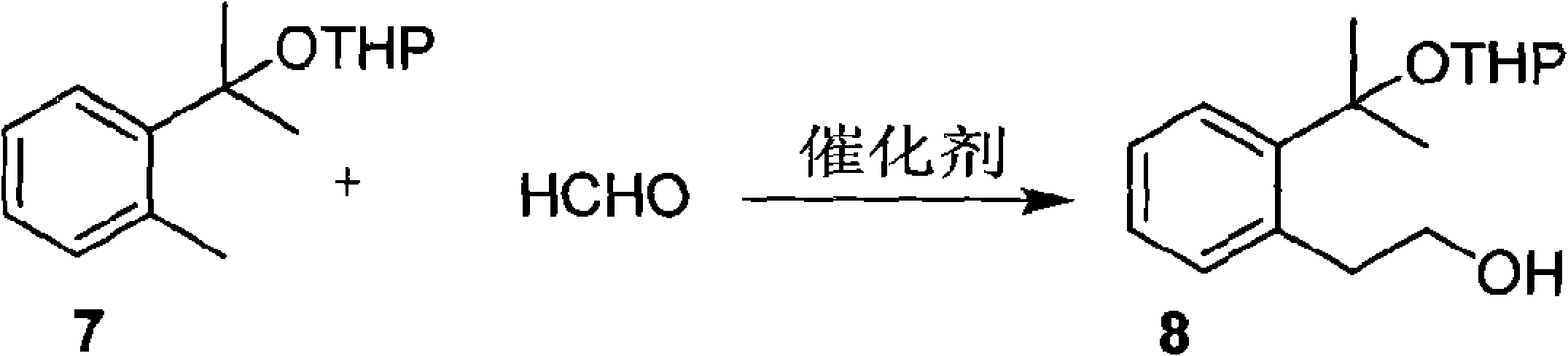
d.化合物7在催化劑存在的條件下與甲醛反應,生成化合物(8)2-(2-鄰(2-羥基乙基)苯基丙基)四氫吡喃醚,反應如下:
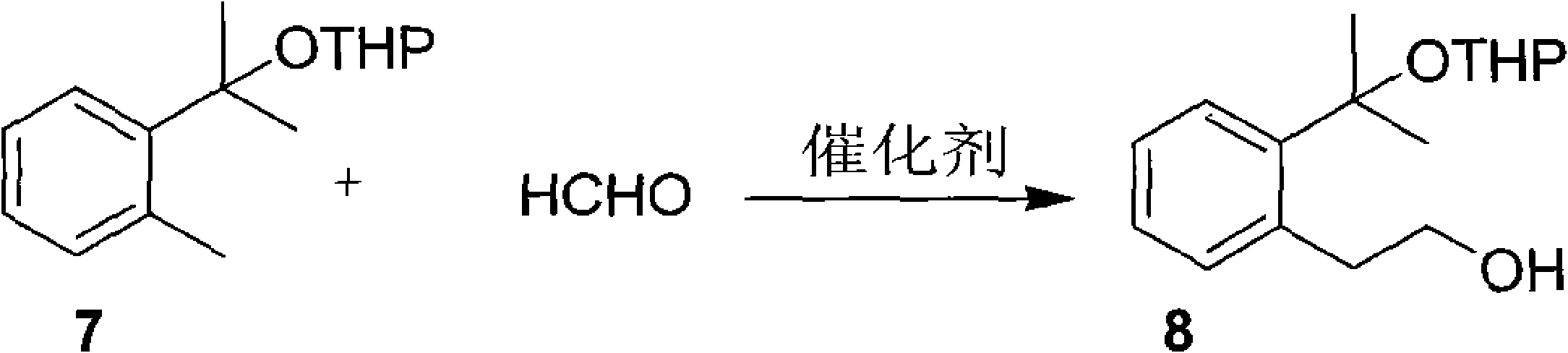
實驗所用的催化劑為氫氧化鈉等鹼金屬氫氧化物、鹼金屬碳酸鹽、有機季銨鹼中的一種,實驗所用的催化劑優選有機季銨鹼,所用的溶劑為極性溶劑,例如二甲亞碸(DMSO)、二甲基甲醯胺(DMF)、二甲基乙醯胺(DMA)、水中的一種或一種以上的混合物,優選DMSO,所用的甲醛為多聚甲醛或三聚甲醛或氣態甲醛。所用的物料比為:2-(2-鄰甲基苯基丙基)四氫吡喃醚:催化劑:甲醛=1摩爾:(0.001~0.1摩爾):(1~4摩爾),反應溫度為55℃~65℃。加料過程為先加入一部分催化劑和甲醛,每反應0.5~2小時後,分次均勻補加剩餘的催化劑和甲醛。
反應溫度隨試劑或者溶劑的變化而變化,溫度較高時,有二醇化合物產生,反應時間較長時,相應的雙羥甲基化產物增多,《孟魯司特鈉中間體的合成方法》通過分批次補加催化劑和甲醛來減少雙羥基化合物的產生,效果較好。
e.化合物8在鹵化劑的作用下,生成了鹵代化合物(9)2-(2-鄰(2-鹵乙基)苯基丙基)四氫吡喃醚,反應如下:
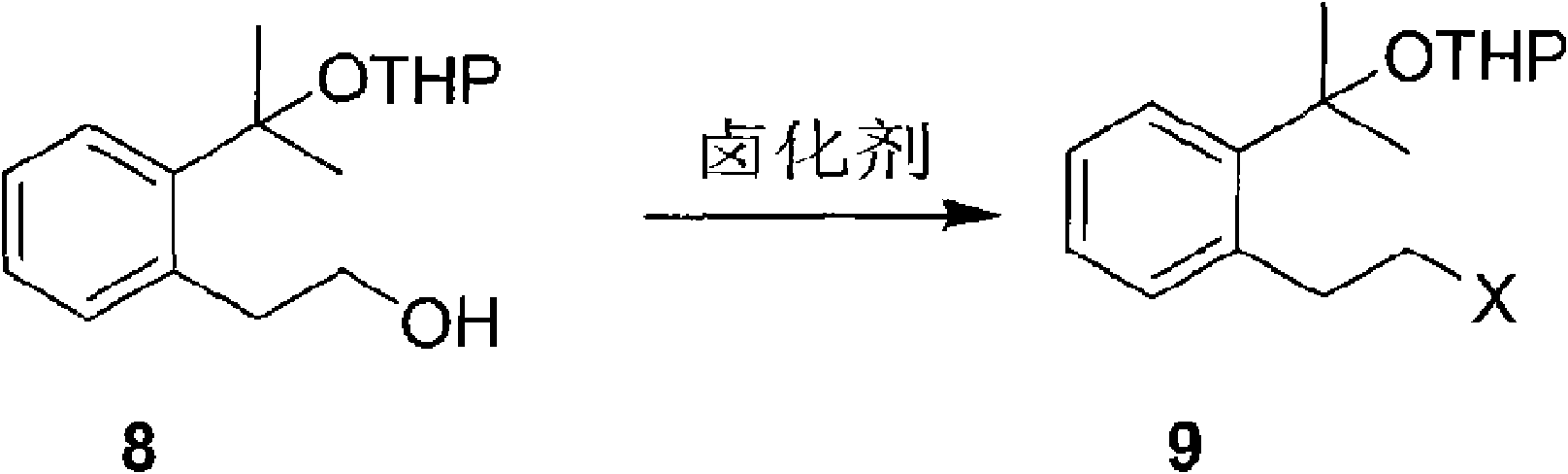
在此步驟中,發現鹵化試劑的用量要控制,以防止副反應發生,溫度最好控制在10℃以下,溫度高了容易發黑,影響收率,溫度太低容易結塊影響反應。所用的溶劑為苯、乙醚、二氯甲烷、三氯甲烷、四氯化碳、二氧六烷、六甲基磷醯胺中的一種或一種以上的混合物,優選三溴化磷,反應溫度為:-5℃~10℃。
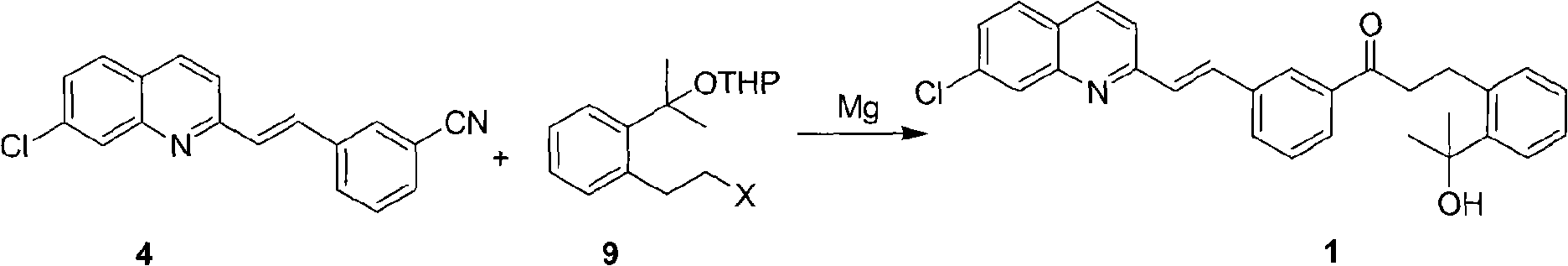
f.鹵代化合物9在金屬鎂和惰性溶劑的條件下和化合物4反應,生成了目標化合物(1)2-(2-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙基)苯基)丙醇,反應如下:
該反應在氮氣保護下,將新打磨至光亮的鎂條加入到溶有2-(2-鄰(2-溴乙基)苯基丙基)四氫吡喃醚的溶液中,反應結束後,濾除過量的鎂條備用。後稱取化合物3-(2-(7-氯-2-喹啉基)乙烯基)苯甲氰溶解,然後慢慢的向冷卻液中滴加上述製備好的四氫呋喃的格氏試劑溶液,滴加溫度為0~5℃,酸性條件下去除保護劑並水解成化合物1,物料比為:2-(2-鄰(2-溴乙基)苯基丙基)四氫吡喃醚:金屬鎂:3-(2-(7-氯-2-喹啉基)乙烯基)苯甲氰=1摩爾:(1.2~2.5摩爾):(0.8~1摩爾)。
改善效果
《孟魯司特鈉中間體的合成方法》的技術效果:通過技術最佳化,提供了一種原料來源易得,適合大規模生產製備的孟魯司特鈉中間體的可替代方法以及可靠地控制的方法。
技術領域
《孟魯司特鈉中間體的合成方法》屬於醫藥化學合成領域,具體涉及一種孟魯司特鈉中間體的合成方法。
權利要求
1.一種合成如下結構(化合物1)的孟魯司特鈉中間體的方法,該方法包括以下步驟:
化合物1
(a)將7-氯喹哪啶和3-氰基苯甲醛在乙酸酐和乙酸鈉的作用下縮合得到化合物(4)3-(2-(7-氯-2-喹啉基)乙烯基)苯甲氰,反應如下:
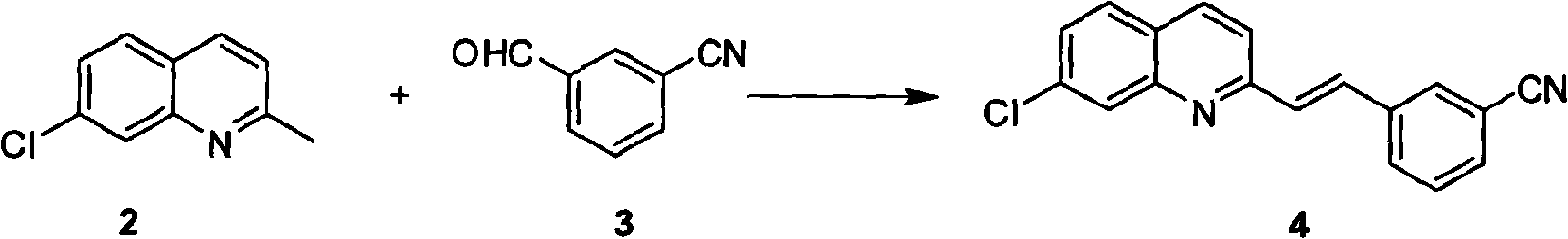
(b)鄰甲基苯乙酮在惰性溶劑中,鹵化甲基鎂的作用下,生成化合物(6)2-鄰甲基苯基-2-丙醇,反應如下:
(c)化合物6在催化劑和二氫吡喃作用下生成了羥基保護的化合物(7)2-(2-鄰甲基苯基丙基)四氫吡喃醚,反應如下:

(d)化合物7在催化劑存在的條件下與甲醛反應生成化合物(8)2-(2-鄰(2-羥基乙基)苯基丙基)四氫吡喃醚,反應如下:
(e)化合物8在鹵化劑的作用下,生成了鹵代化合物(9)2-(2-鄰(2-鹵乙基)苯基丙基)四氫吡喃醚,反應如下:

(f)鹵代化合物9,在金屬鎂和惰性溶劑的條件下和化合物4反應,生成了目標化合物(1)2-(2-(3-(2-(7-氯-2-喹啉基)乙烯基)苯基)-3-氧代丙基)苯基)丙醇,反應如下:
2.根據權利要求1所述的方法,其特徵在於步驟(a)中溶劑為二甲亞碸、二甲基甲醯胺、二甲基乙醯胺、六甲基磷醯胺、二甲苯和硝基苯中的一種或一種以上的混合物。
3.根據權利要求1所述的方法,其特徵在於步驟(a)中溶劑為二甲亞碸、二甲基甲醯胺、二甲基乙醯胺和六甲基磷醯胺中的一種或一種以上的混合物。
4.根據權利要求1所述的方法,其特徵在於步驟(a)中溶劑為二甲基甲醯胺。
5.根據權利要求1所述的方法,其特徵在於步驟(a)中反應溫度為120℃~140℃。
6.根據權利要求1所述的方法,其特徵在於步驟(b)中所用的鹵化甲基鎂是氯化甲基鎂或溴化甲基鎂。
7.根據權利要求1所述的方法,其特徵在於步驟(b)中所用的鹵化甲基鎂是溴化甲基鎂。
8.根據權利要求1所述的方法,其特徵在於步驟(b)中所用的物料比為:鹵化甲基鎂:鄰甲基苯乙酮=1摩爾:1.0~1.5摩爾。
9.根據權利要求1所述的方法,其特徵在於步驟(b)中所用的溶劑為苯、四氫呋喃、2-甲基四氫呋喃、乙醚、異丙醚、乙二醇二甲醚中的一種或多種。
10.根據權利要求1所述的方法,其特徵在於步驟(b)中所用的溶劑為四氫呋喃。
11.根據權利要求1所述的方法,其特徵在於步驟(b)中反應溫度為:20℃~30℃。
12.根據權利要求1所述的方法,其特徵在於步驟(b)中TLC檢測反應終點,展開劑體積比為:正己烷:乙酸乙酯=4:1。
13.根據權利要求1所述的方法,其特徵在於步驟(c)中催化劑為氫溴化三苯基磷、氫溴化三叔丁基磷、鹽酸、氫溴酸、三氯氧磷、對甲苯磺酸和三氟化硼-乙醚中的一種或多種。
14.根據權利要求1所述的方法,其特徵在於步驟(c)中催化劑為氫溴化三苯基磷。
15.根據權利要求1所述的方法,其特徵在於步驟(c)中所用的溶劑為二氯甲烷、氯仿、四氯化碳、四氫呋喃、乙醚、二氧六烷、二甲基甲醯胺和乙酸乙酯中的一種或多種。
16.根據權利要求1所述的方法,其特徵在於步驟(c)中所用的溶劑為二氯甲烷。
17.根據權利要求1所述的方法,其特徵在於步驟(c)中所用的物料比為:2-鄰甲基苯基-2-丙醇:二氫吡喃:催化劑=1摩爾:2~6摩爾:0.1~1摩爾。
18.根據權利要求1所述的方法,其特徵在於步驟(d)中所用的溶劑為二甲亞碸、二甲基甲醯胺、二甲基乙醯胺和水中的一種或一種以上的混合物。
19.根據權利要求1所述的方法,其特徵在於步驟(d)中所用的溶劑為二甲亞碸。
20.根據權利要求1所述的方法,其特徵在於步驟(d)中所用的催化劑為鹼金屬氫氧化物、鹼金屬碳酸鹽或有機季銨鹼中的一種。
21.根據權利要求1所述的方法,其特徵在於步驟(d)中所用的催化劑為有機季銨鹼。
22.根據權利要求1所述的方法,其特徵在於步驟(d)中所用的甲醛為多聚甲醛或三聚甲醛或氣態甲醛。
23.根據權利要求1所述的方法,其特徵在於步驟(d)中所用的物料比為:2-(2-鄰甲基苯基丙基)四氫吡喃醚:催化劑:甲醛=1摩爾:0.001~0.1摩爾:1~4摩爾。
24.根據權利要求1所述的方法,其特徵在於步驟(d)中反應溫度為:20℃~100℃。
25.根據權利要求1所述的方法,其特徵在於步驟(d)中反應溫度為:55℃~65℃。
26.根據權利要求1所述的方法,其特徵在於步驟(d)中反應時間為1.5~10小時。
27.根據權利要求1所述的方法,其特徵在於步驟(e)中所用的溶劑為苯、乙醚、二氯甲烷、三氯甲烷、四氯化碳、二氧六烷和六甲基磷醯胺中的一種或一種以上的混合物。
28.根據權利要求1所述的方法,其特徵在於步驟(e)中所用的鹵化劑為二氯亞碸、鹽酸-氯化鋅、五氯化磷、三氯氧磷、溴化氫和三溴化磷中的一種或一種以上的混合物。
29.根據權利要求1所述的方法,其特徵在於步驟(e)中所用的鹵化劑為三溴化磷。
30.根據權利要求1所述的方法,其特徵在於步驟(e)中反應溫度為:-5℃~10℃。
31.根據權利要求1所述的方法,其特徵在於步驟(f)中滴加格氏試劑溫度為0~5℃。
32.根據權利要求1所述的方法,其特徵在於步驟(f)中物料比為:2-(2-鄰(2-溴乙基)苯基丙基)四氫吡喃醚:金屬鎂:3-(2-(7-氯-2-喹啉基)乙烯基)苯甲氰=1摩爾:1.2~2.5摩爾:0.8~1摩爾。
實施方式
氮氣保護下,將137.6克(1.05摩爾)間氰基苯甲醛,177克(1.0摩爾)7-氯喹哪啶和82克乙酸鈉,加入1000毫升乙酸酐中,攪拌下加熱至125~135℃,反應24個小時後,蒸出大部分的乙酸酐,向剩餘物中加入300毫升水,乙酸乙酯萃取(500毫升×3),飽和食鹽水洗滌,無水硫酸鈉乾燥,真空濃縮,剩餘物快速柱層析得產品266.8克,收率:92%。
HNMR(DMSO)8.38(d,J=9Hz,1H),8.10(d,J=9Hz,1H),7.50-8.08(m,9H);
IR(KBr,cm),2230,1597,1504,976,824;
HRMScalcdfor(M+)C18H11ClN2290.0611,found290.0617.
氮氣保護下,將137.6克(1.05摩爾)間氰基苯甲醛,177克(1.0摩爾)7-氯喹哪啶和82克乙酸鈉,加入200毫升乙酸酐和800毫升二甲基甲醯胺(DMF)中,攪拌下加熱至回流。反應24個小時後,蒸出大部分的溶劑,向剩餘物中加入300毫升水,乙酸乙酯萃取(500毫升×3),飽和食鹽水洗滌,無水硫酸鈉乾燥,真空濃縮後,剩餘物快速柱層析得產品241克,收率:83%。
氮氣保護下,將134克(1.0摩爾)鄰甲基苯乙酮溶於1000毫升四氫呋喃中,冷卻至-5℃,慢慢滴加2M溴化甲基鎂的四氫呋喃溶液550毫升到-5℃的反應液中,保持溫度在0℃以下,滴加完畢後,將反應液在室溫下攪拌3小時,TLC跟蹤檢測,待反應完全後,將200毫升飽和NH4Cl溶液慢慢滴加到反應液中,攪拌直到沒有氣泡冒出為止,二氯甲烷萃取(500毫升×3),合併萃取液,無水硫酸鈉乾燥,活性碳吸附,過濾旋乾溶劑即得淡黃色粘稠液體2-鄰甲基苯基-2-丙醇132克,收率88%。
HNMR(CDCl3)7.18-7.42(4H,m),4.38(1H,brs),2.36(3H,s),1.33(6H,s)
氮氣保護下,將134克(1.0摩爾)鄰甲基苯乙酮溶於1000毫升四氫呋喃中,冷卻至-5℃,慢慢滴加2M氯化甲基鎂的四氫呋喃溶液550毫升到-5℃的反應液中,保持溫度在0℃以下,滴加完畢後,將反應液在室溫下攪拌4小時,TLC跟蹤檢測,待反應完全後,將200毫升飽和NH4Cl溶液慢慢滴加到反應液中,攪拌直到沒有氣泡冒出為止,二氯甲烷萃取(500毫升×3),合併萃取液,無水硫酸鈉乾燥,活性碳吸附,過濾旋乾溶劑即得淡黃色粘稠液體2鄰甲基苯基-2丙醇124克,收率82.6%。
將75克(0.5摩爾)化合物6加入500毫升乾燥二氯甲烷中,攪拌下加入84.0克(1.0摩爾)二氫吡喃和3.43克(0.01摩爾)氫溴化三苯基磷,反應液攪拌回流24小時後,再加入84.0克(1.0摩爾)二氫吡喃和3.43克(0.01摩爾)三苯磷溴化物。反應液繼續攪拌回流24小時,反應完畢,將反應液濃縮,余物用矽膠柱層析(洗脫液為甲苯),收集產品相得油狀物108克,收率92%。
將58.5克(0.25摩爾)化合物7和多聚甲醛3克(0.1摩爾)加入到50毫升DMSO中,然後向反應液中滴加1毫升三甲基苄基氫氧化銨(30%的甲醇溶液),顏色變成深褐色,保持溫度在60-65℃,每1小時向反應液中補加3克(0.1摩爾)多聚甲醛和0.5毫升三甲基苄基氫氧化銨(30%的甲醇溶液),共加入多聚甲醛12克,反應結束後調節溶液pH=6~8,蒸出大部分DMSO,向剩餘物中加入100毫升飽和的氯化鈉水溶液,乙酸乙酯萃取,柱層析分離純化得到淡黃色粘稠物51.5克,收率78%。
將58.5克(0.25摩爾)化合物7和多聚甲醛3克(0.1摩爾)加入到50毫升DMSO中,然後向反應液中滴加1毫升四甲基氫氧化銨(40%水溶液),顏色變成深褐色,保持溫度在60~65℃,每1小時向反應液中補加3克(0.1摩爾)多聚甲醛和0.5毫升四甲基氫氧化銨(40%水溶液),共加入多聚甲醛12克,反應結束後調節溶液pH=6~8,蒸出大部分DMSO,向剩餘物中加入100毫升飽和的氯化鈉水溶液,乙酸乙酯萃取,柱層析分離純化得到淡黃色粘稠物47.7克,收率72.3%。
將58.5克(0.25摩爾)化合物7和多聚甲醛3克(0.1摩爾)和0.70克(0.006摩爾)苯酚鈉加入到50毫升DMSO中,顏色變成深褐色,保持溫度在60-65℃,每2小時向反應液中補加3克(0.1摩爾)多聚甲醛,共加入多聚甲醛12克,反應結束後調節溶液pH=6~8,蒸出大部分DMSO,向剩餘物中加入100毫升飽和的氯化鈉水溶液,乙酸乙酯萃取,柱層析分離純化得到粘稠物41.6克,收率63%。
將26.4克(0.1摩爾)化合物8溶於300毫升乙醚中,冷卻至0℃,然後慢慢的向反應液中滴加3.8毫升(0.04摩爾)三溴化磷,保持溫度在5℃以下,滴加完畢後,室溫攪拌5小時,反應結束後,向反應液中滴加飽和NaHCO3水溶液,調節至中性,然後乙醚萃取(300毫升×3),合併萃取液,無水硫酸鎂乾燥,減壓濃縮得到產品32克(HPLC99.2%),收率98%。
將26.4克(0.1摩爾)化合物8溶於300毫升甲苯中,冷卻至0℃,然後慢慢的向反應液中滴加16克48%的氫溴酸溶液,保持溫度在5℃以下,滴加完畢後,室溫攪拌過夜,反應結束後,向反應液中滴加飽和NaHCO3水溶液,調節至中性,然後乙醚萃取(300毫升×3),合併萃取液,無水硫酸鎂乾燥,減壓濃縮得到產品30.9克,收率95%。
將26.4克(0.1摩爾)化合物8溶於300毫升二氯甲烷中,冷卻至0℃,然後慢慢的向反應液中滴加8毫升二氯亞碸,保持溫度在5℃以下,滴加完畢後,室溫攪拌5小時,反應結束後,向反應液中滴加飽和NaHCO
3水溶液,調節至中性,然後
二氯甲烷萃取(300毫升×3),合併萃取液,無水硫酸鎂乾燥,減壓濃縮得到產品27克,收率95%。
將26.4克(0.1摩爾)化合物8溶於300毫升二氯甲烷中,冷卻至0℃,然後慢慢的向反應液中滴加9克三溴化磷,保持溫度在5℃以下,滴加完畢後,室溫攪拌5小時,反應結束後,向反應液中滴加飽和NaHCO3水溶液,調節至中性,然後二氯甲烷萃取(300毫升×3),合併萃取液,無水硫酸鎂乾燥,減壓濃縮得到產品32克,收率99%。
氮氣保護下,將2.16克(0.09摩爾)新打磨至光亮的鎂條加入到溶有16.3克(0.06摩爾)2-(2-鄰(2-溴乙基)苯基丙基)四氫吡喃醚的60毫升四氫呋喃中,反應結束後,濾除過量的鎂條備用。稱取14.5克(0.05摩爾)化合物3-(2-(7-氯-2-喹啉基)乙烯基)苯甲氰溶於100毫升四氫呋喃中,然後冷卻至0℃,然後慢慢的向冷卻液中滴加上述製備好的四氫呋喃的格氏試劑溶液,保持溫度在5℃以下,滴加完畢後,回流攪拌3小時,反應結束後,向反應液中滴加30毫升(6摩爾/升)的鹽酸溶液,加熱攪拌回流6小時,乙酸乙酯萃取(100毫升×3),合併萃取液,無水硫酸鎂乾燥,減壓濃縮得到產品18.9克,收率70%。
HRMScalcdfor(M+)C34H34ClNO3539.2227,found539.2216。
榮譽表彰
2018年12月20日,《孟魯司特鈉中間體的合成方法》獲得第二十屆中國專利獎優秀獎。