威太(鹽酸伊托必利分散片),適應症為本品適用於功能性消化不良引起的各種症狀,如:上腹部不適、餐後飽脹、早飽、食欲不振、噁心、嘔吐等。
基本介紹
- 藥品名稱:威太
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:胃腸促動藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,核准日期,修訂日期,
成份
化學名稱:N-[4-[2-(二甲胺基)乙氧基]苯甲基]-3,4-二甲氧苯甲醯胺鹽酸鹽
化學結構式:
分子式:C20H26N2O4·HCl
分子量:394.90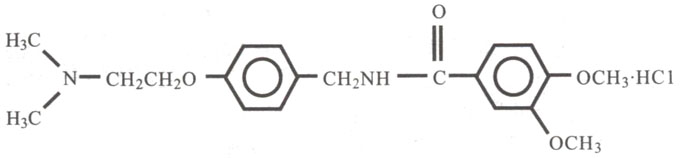
化學結構式:
分子式:C20H26N2O4·HCl
分子量:394.90

性狀
本品為白色或類白色分散片。
適應症
本品適用於功能性消化不良引起的各種症狀,如:上腹部不適、餐後飽脹、早飽、食欲不振、噁心、嘔吐等。
規格
50 mg
用法用量
口服。成人每日3次,每次1片(50 mg),飯前15-30分鐘服用;或遵醫囑。
不良反應
1、過敏症狀:皮疹、發熱、瘙癢感等。
2、消化系統:腹瀉、腹痛、便秘、唾液增加等。
3、精神神經系統:頭痛、刺痛、睡眠障礙、眩暈等。
4、血液系統:白細胞減少。確認出現異常時應停止給藥。
5、偶爾會出現BUN、肌酐上升,有AST、ALT、催乳素上升(在正常範圍內)的報導。
6、其他:胸背部疼痛、疲勞、手指發麻、手抖等。
2、消化系統:腹瀉、腹痛、便秘、唾液增加等。
3、精神神經系統:頭痛、刺痛、睡眠障礙、眩暈等。
4、血液系統:白細胞減少。確認出現異常時應停止給藥。
5、偶爾會出現BUN、肌酐上升,有AST、ALT、催乳素上升(在正常範圍內)的報導。
6、其他:胸背部疼痛、疲勞、手指發麻、手抖等。
禁忌
1、對本品成分過敏者禁用。
2、存在胃腸道出血、機械梗阻或穿孔時禁用。
2、存在胃腸道出血、機械梗阻或穿孔時禁用。
注意事項
1.本品可增強乙醯膽鹼的作用,故使用時應當注意。
2.使用本品效果不佳時,應避免長期無目的的使用。
3.嚴重肝腎功能不全者慎用。
4.用藥中如出現心電圖QTc間期延長者應停藥。
2.使用本品效果不佳時,應避免長期無目的的使用。
3.嚴重肝腎功能不全者慎用。
4.用藥中如出現心電圖QTc間期延長者應停藥。
孕婦及哺乳期婦女用藥
1.由於尚未確認妊娠婦女給藥的安全性,對於孕婦或有妊娠可能的婦女,只有確認其治療上的有益性高於危險性時才可以給藥。
2.由於已有報告在動物實驗(大白鼠)中本品可向乳汁中轉移,因而服用本藥物時應當避免哺乳。
2.由於已有報告在動物實驗(大白鼠)中本品可向乳汁中轉移,因而服用本藥物時應當避免哺乳。
兒童用藥
兒童服用本品的安全性資料尚未確立,應避免服用。
老年用藥
由於老年人的生理功能下降,常易發生不良反應,因此老年人在服用本品後需仔細觀察,一旦出現不良反應,需採取減量或停藥等措施。
藥物相互作用
由於替喹溴胺、丁溴東莨菪鹼、噻哌溴銨等抗膽鹼藥物可能使本品促進胃腸道運動的作用減弱,故本品應避免與上述藥物合用。
藥物過量
目前尚無過量服用本品的報導。假如服藥過量,應採取對症治療。
藥理毒理
藥理作用
鹽酸伊托必利通過對多巴胺D2受體的拮抗作用而增加乙醯膽鹼的釋放,同時通過對乙醯膽鹼酶的抑制作用來抑制已釋放的乙醯膽鹼分解,從而增強胃、十二指腸動力。本品具有良好的胃動力作用,可增強胃、十二指腸收縮力,加速胃排空,並有抑制嘔吐的作用。
毒理研究
重複給藥毒性
大鼠經口給藥劑量為10、30、100 mg/kg/d,持續26周,結果100 mg/kg/d組雌鼠的體重增加較快,攝食量和攝水量增多,與對照組相比,雌鼠的白蛋白值顯著性下降,總蛋白量和A/G比值明顯下降,雌鼠乳腺增生的發生率升高,所有大鼠的血清膽固醇、甘油三酯、磷脂值明顯降低,30 mg/kg/d劑量組雌鼠的體重增加較快,攝食量略有增多,總蛋白量A/G比值、磷脂值降低,乳腺增生的發生率升高;無毒性反應劑量為10 mg/kg/d。犬經口給藥劑量分別為10、30、100 mg/kg/d,持續13周,結果100 mg/kg/d組動物從給藥第一周開始,給藥1小時後觀察到自發活動減少、震顫、行為異常等症狀,這些症狀均在給藥24小時後或恢復期消失,100 mg/kg/d劑量組一些動物的體重和體重增加幅度輕度降低;30 mg/kg/d以上組前列腺重量低於對照組,這與病理組織學檢查所見前列腺組織輕度萎縮結果一致;以上改變均可恢復,無毒性反應劑量為10 mg/kg/d。
生殖毒性
一般生殖毒性試驗中,雌雄動物經口給藥,劑量為3、30、300 mg/kg,結果300 mg/kg劑量組給藥初期約1/2雄鼠出現流涎體徵,雌鼠給藥和妊娠期間體重增加,在交配前攝食量增多;30 mg/kg以上劑量組雌鼠性周期延長,大鼠交配率、受孕率、胎仔存活率和胎仔發育未見異常。圍產期生殖毒性試驗中,300 mg/kg劑量組幼鼠體重增加緩慢,10、100 mg/kg劑量組母鼠分娩、F1代仔鼠發育、生殖能力均未見異常。
遺傳毒性
小鼠微核試驗、微生物回復突變試驗和入血細胞染色體畸變結果均為陰性。
鹽酸伊托必利通過對多巴胺D2受體的拮抗作用而增加乙醯膽鹼的釋放,同時通過對乙醯膽鹼酶的抑制作用來抑制已釋放的乙醯膽鹼分解,從而增強胃、十二指腸動力。本品具有良好的胃動力作用,可增強胃、十二指腸收縮力,加速胃排空,並有抑制嘔吐的作用。
毒理研究
重複給藥毒性
大鼠經口給藥劑量為10、30、100 mg/kg/d,持續26周,結果100 mg/kg/d組雌鼠的體重增加較快,攝食量和攝水量增多,與對照組相比,雌鼠的白蛋白值顯著性下降,總蛋白量和A/G比值明顯下降,雌鼠乳腺增生的發生率升高,所有大鼠的血清膽固醇、甘油三酯、磷脂值明顯降低,30 mg/kg/d劑量組雌鼠的體重增加較快,攝食量略有增多,總蛋白量A/G比值、磷脂值降低,乳腺增生的發生率升高;無毒性反應劑量為10 mg/kg/d。犬經口給藥劑量分別為10、30、100 mg/kg/d,持續13周,結果100 mg/kg/d組動物從給藥第一周開始,給藥1小時後觀察到自發活動減少、震顫、行為異常等症狀,這些症狀均在給藥24小時後或恢復期消失,100 mg/kg/d劑量組一些動物的體重和體重增加幅度輕度降低;30 mg/kg/d以上組前列腺重量低於對照組,這與病理組織學檢查所見前列腺組織輕度萎縮結果一致;以上改變均可恢復,無毒性反應劑量為10 mg/kg/d。
生殖毒性
一般生殖毒性試驗中,雌雄動物經口給藥,劑量為3、30、300 mg/kg,結果300 mg/kg劑量組給藥初期約1/2雄鼠出現流涎體徵,雌鼠給藥和妊娠期間體重增加,在交配前攝食量增多;30 mg/kg以上劑量組雌鼠性周期延長,大鼠交配率、受孕率、胎仔存活率和胎仔發育未見異常。圍產期生殖毒性試驗中,300 mg/kg劑量組幼鼠體重增加緩慢,10、100 mg/kg劑量組母鼠分娩、F1代仔鼠發育、生殖能力均未見異常。
遺傳毒性
小鼠微核試驗、微生物回復突變試驗和入血細胞染色體畸變結果均為陰性。
藥代動力學
本品口服後吸收迅速,給藥後約30分鐘可達峰值血藥濃度,半衰期約為6小時。多次口服給藥時,血清中藥物濃度與單次給藥時相同。本品原形藥物4-5%、其他代謝物約75%從尿中排泄。多次給藥時,排泄率與單次給藥無明顯差異。據文獻報導,動物口服吸收後主要分布在肝臟、腎臟及消化系統,較少在中樞神經系統分布;十二指腸內給藥時,在胃肌肉層中的藥物濃度是血液中藥物濃度的兩倍。
貯藏
密閉保存。
包裝
鋁塑包裝,6片×1板,6片×3板,12片×1板,12片×2板。
有效期
24個月
執行標準
國家藥品標準WS1-(X-014)-2009Z
批准文號
國藥準字H20031270
生產企業
迪沙藥業集團有限公司
核准日期
2007年3月13日
修訂日期
2011年11月17日
