相關研究
氮氧自由基的單電子轉移反應 以哌啶氮氧自由基為模型化合物,進行了電子結構的計算以及取代基和溶劑效應對電子自旋共振超精細分裂的影響的測定,套用循環伏安法對氮氧自由基單電子氧化還原作了系統研究,採用動態電子自旋共振及紫外光譜研究了氮氧自由基與維生素C、半胱氨酸、谷胱甘肽等生物活性分子的反應動力學,首次揭示了這些反應的單電子轉移機理及活性中間體(如抗壞血酸負離子自由基),為探討生物氧化還原反應提供了有價值的信息。同時還研究了氮氧自由基在酸性介質中對芳胺、含氮、硫芳雜環等的單電子氧化生成自由基正離子的反應,闡明了反應機理,為產生自由基正離子提供了一種新的簡便方法。
80年代以來,格氏試劑的生成及某些烷基格氏試劑的單電子轉移反應機理的研究引起了許多研究工作者的興趣,但還未見烯基格氏試劑的有關報導。本項研究通過電子自旋共振、化學誘導動態核極化等現代實驗技術,研究了一系列烯基格氏試劑的生成及其與苯基取代鹵甲烷的反應,首次揭示了這些反應是通過單電子轉移機理進行的。
常見反應
單電子轉移反應可以在化學試劑和光的作用及電化學條件下產生。許多無機試劑,如S
2O
8-、
AlCl3、O
2、X
2等都表現出很強的單電子氧化性,它們與有機分子的許多反應是通過單電子氧化形成的自由基型中問體進行的。醯基過氧化物和醇金屬試劑,碳陰離子(基),硫化物等也都易引發單電子轉移反應。許多過渡金屬離子具有不止一個比較穩定的氧化態。所以,過渡金屬離子在涉及單電子轉移的過程中經常被用作催化劑和試劑。
羧酸根離子的單電子氧化反應產生醯氧自由基,後者再發生一般的脫羧反應,如Kolbe製備烷烴的電解反應:
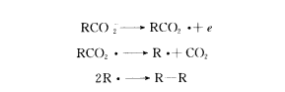 製備烷烴電解反應
製備烷烴電解反應戊酸在LiCl存在下用四乙酸鉛氧化生成氯丁烷:
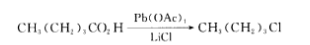 反應方程
反應方程反應第一步是與Pb
4+配位的
羧酸根離子氧化生成烷基自由基、CO
2和Pb
3+,烷基自由基從Pb
4+絡合物奪走鹵素生成Pb
3+,Pb
3+分解生成Pb
2+,同時再生成一個烷基自由基使鏈式過程繼續下去。但機理可能並不止這一條。
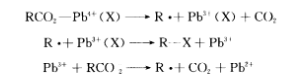 反應機理
反應機理鹼金屬、鹼土金屬及某些稀土金屬也都是很強的供電子體。含有共軛π鍵的分子則具有較高的電子親和力而易於成為負離子基;當它們與電子受體作用時又由於它具有較低的電離勢而成為正離子基。
 反應方程
反應方程影響因素
立體因素和電子因素是影響有機反應途徑的主要因素。
從這兩種反應途徑看,在結構相似的分子中立體阻礙大的兩個原子(團)之間的反應將更易於發生單電子轉移歷程,這是因為在極性反應的過渡態中反應物分子間已經部分成鍵,而經單電子轉移反應的過渡態並無這種作用。雖然極性反應的過渡態能量較低,但只有當兩個反應物相互接近到一定距離時才能作用,如果反應物的立體位阻很大,由成鍵引起的過渡態能量的降低將由於立體阻礙而被部分抵消,囚此不利於極性反應。而單電子轉移途徑對立體因素的敏感度要小得多。
在電子因素方面,
電子供體D與受體A發生單電子轉移反應後,若能形成較穩定的價電子構型中間體D
+或A
-,則有利於單電子轉移反應。如
鹼金屬和許多陰離子自由基都是很強的單電子還原劑,易於失去一個電子。此外,電子供體和受體的氧化還原電位的差值越大,發生單電子轉移反應的傾向也越大。如穩定性較高,還原性較強的碳負離子與苄氯的反應就易於按單電子轉移途徑進行,而還原性較低的碳負離子的反應易於按極性途徑進行。
D—A鍵的強度和自由基型中問體D
+,A
-的離域程度對
反應機理也有一定影響。D一A鍵越弱,它們之間發生單電子轉移的可能性也越大,硫化物的C—S鍵能較弱,故常可作為單電子還原劑參與反應;D
+和A
-的離域程度越大,越有利於它們的穩定存在,因此也有利於單電子轉移反應。
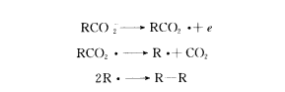 製備烷烴電解反應
製備烷烴電解反應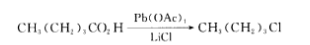 反應方程
反應方程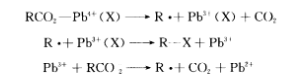 反應機理
反應機理 反應方程
反應方程