介入磁共振是一個醫療技術。
基本介紹
- 中文名:介入磁共振
- 外文名:InterventionalMagnetic Resonance
簡介
介入磁共振系統磁體設計
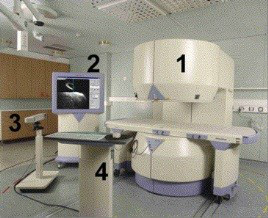
介入磁共振手術場所及器械設備
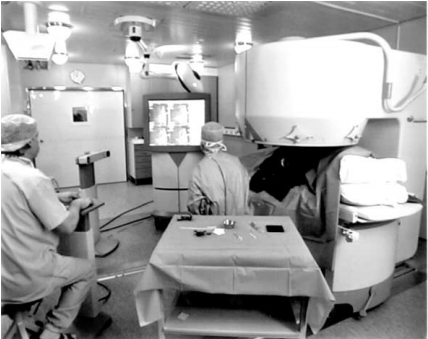
介入磁共振成像序列
磁共振介入導航的主要方式
磁共振介入的臨床套用
- MR引導下經皮穿刺活檢及囊腫、血腫和膿腫的抽吸引流;
- 腫瘤間質消融治療:腫瘤雷射熱消融術、氬氦刀冷凍消融治療;
- 腫瘤內局部放射性粒子及化學藥物植入術;
- 疼痛治療:神經根阻滯與腹腔神經叢的阻滯與損毀術;
- 椎間盤突出微創性旋切結合臭氧治療術;
- 中晚期帕金森病的微創治療;
- 乳腺早期病變及前列腺腫瘤的病理診斷與冷凍消融治療。
擴展閱讀
- 趙磊,王洋. MRI 導引與監控微創介入治療技術[J]. 醫學影像學
- 林征宇,武樂斌,李成利,等.光學導航介入性MR的臨床套用[J].中華放射學雜誌,2005,39(7):740—742.
- F.A. Jolesz, S.M. Blumenfeld. Interventional use of magnetic resonance imaging.
- Magn Reson Q, 10 (1994), pp. 85–96
- J. Kettenbach, D.F. Kacher, S.K. Koskinen, etal. Interventional and intraoperative magnetic resonance imaging. Annu Rev Biomed Eng, 2 (2000), pp. 661–690
- J.S. Lewin, C.A. Petersilge, S.F. Hatem, etal. Interactive MR imaging-guided biopsy and aspiration with a modified clinical C-arm system. AJR Am J Roentgenol, 170 (1998), pp. 1593–1601
- R. Lufkin, L. Teresi, L. Chiu, W. Hanafee. A technique for MR-guided needle placement.AJR Am J Roentgenol, 151 (1988), pp. 193–196
- R. Lufkin, L. Teresi, W. Hanafee. New needle for MR-guided aspiration cytology of the head and neck. AJR Am J Roentgenol, 149 (1987), pp. 380–382
- P.R. Mueller, D.D. Stark, J.F. Simeone, etal. MR-guided aspiration biopsy: needle design and clinical trials. Radiology, 161 (1986), pp. 605–609
- G. Duckwiler, R.B. Lufkin, W.N. Hanafee. MR-directed needle biopsies. Radiol Clin North Am, 27 (1989), pp. 255–263
- E. vanSonnenberg, P. Hajek, V. Gylys-Morin, etal. A wire-sheath system for MR-guided biopsy and drainage: laboratory studies and experience in 10 patients. AJR Am J Roentgenol, 151 (1988), pp. 815–817
- H.E. Cline, J.F. Schenck, K. Hynynen, R.D. Watkins, S.P. Souza, F.A. Jolesz. MR-guided focused ultrasound surgery. J Comput Assist Tomogr, 16 (1992), pp. 956–965
- B. Quesson, J.A. de Zwart, C.T. Moonen. Magnetic resonance temperature imaging for guidance of thermotherapy. J Magn Reson Imaging, 12 (2000), pp. 525–533
- E. Salomonowitz. MR imaging-guided biopsy and therapeutic intervention in a closed-configuration magnet: single-center series of 361 punctures. AJR Am J Roentgenol, 177 (2001), pp. 159–163
- Y. Popowski, E. Hiltbrand, D. Joliat, M. Rouzaud. Open magnetic resonance imaging using titanium–zirconium needles: improved accuracy for interstitial brachytherapy implants? Int J Radiat Oncol Biol Phys, 47 (2000), pp. 759–765
- J.F. Schenck, F.A. Jolesz, P.B. Roemer, etal. Superconducting open-configuration MR imaging system for image-guided therapy. Radiology, 195 (1995), pp. 805–814
- D.H. Gronemeyer, R.M. Seibel, L. Kaufman. Low-field design eases MRI-guided biopsies. Diagn Imaging (San Franc), 13 (1991), pp. 139–143
- R. Ojala, E. Vahala, J. Karppinen, et al. Nerve root infiltration of the first sacral root with MRI guidance. J Magn Reson Imaging, 12 (2000), pp. 556–561
- Buecker, G. Adam, J.M. Neuerburg, A. Glowinski, J.J. van Vaals, R.W. Guenther. MR-guided biopsy using a T2-weighted single-shot zoom imaging sequence (Local Look technique). J Magn Reson Imaging, 8 (1998), pp. 955–959
- J.L. Duerk, J.S. Lewin, D.H. Wu. Application of keyhole imaging to interventional MRI: a simulation study to predict sequence requirements.J Magn Reson Imaging, 6 (1996), pp. 918–924
- G. Adam, A. Bucker, C. Nolte-Ernsting, J. Tacke, R.W. Gunther. Interventional MR imaging: percutaneous abdominal and skeletal biopsies and drainages of the abdomen.Eur Radiol, 9 (1999), pp. 1471–1478
