專利背景
生物相容性是指生物醫用材料與生物體之間的相互作用而產生的各種物理化學反應,是生物醫用材料最重要的特性之一,生物相容性的優劣直接決定該材料是否能套用於生物體。對於與血液接觸的材料來說,材料表面血液相容性較差,蛋白質(如纖維蛋白原(Fg)、人血白蛋白(HSA)等)在材料表面的不可控的、非特異性的吸附會引起一系列不良反應,如凝血、溶血、血栓等現象。於是製備具有優異血液相容性的材料表面顯得非常有意義。
截至2016年6月用提高材料表面抗蛋白吸附能力的最為普遍的是PEG,然而PEG在一定環境中的降解性限制了其在很多領域的套用。聚乙烯基吡咯烷酮(PVP)是一種具有優異水溶性、良好生物相容性和化學穩定性的高分子聚合物,是由單體N-乙烯基吡咯烷酮在一定條件下聚合而成,已廣泛套用於生物、醫藥、食品、材料等領域。聚乙烯基吡咯烷酮(PVP)已開始被廣泛套用於製備優異血液相容性的材料表面。於是利用其提高材料表面的抗蛋白吸附性能,改善材料表面血液相容性成為了研究的熱點。研究人員採用的這些修飾方法可以將聚乙烯基吡咯烷酮(PVP)接枝於材料表面,但都不能控制接枝密度和接枝鏈長,因而無法研究這兩個因素對聚乙烯基吡咯烷酮改善基材抗蛋白非特異性吸附性能的影響,然而上述兩個因素被認為是影響著材料抗蛋白非特異性吸附性能的重要因素。
發明內容
專利目的
《一種利用可控接枝技術提高材料表面血液相容性的方法》的目的在於克服截至2016年6月相關技術存在的問題,提供一種利用可控接枝技術提高材料表面血液相容性的方法,該方法可控制接枝密度和接枝鏈長。
《一種利用可控接枝技術提高材料表面血液相容性的方法》先合成巰基化聚乙烯基吡咯烷酮,利用該巰基與金的化學反應,將聚合物接Au表面,提高材料表面抗蛋白吸附性能,製備具有優異血液相容性材料表面。
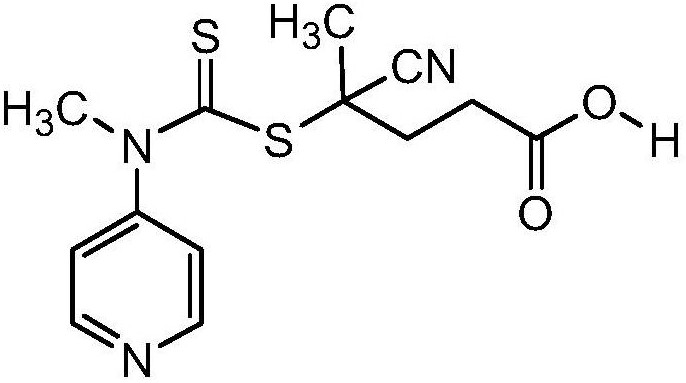
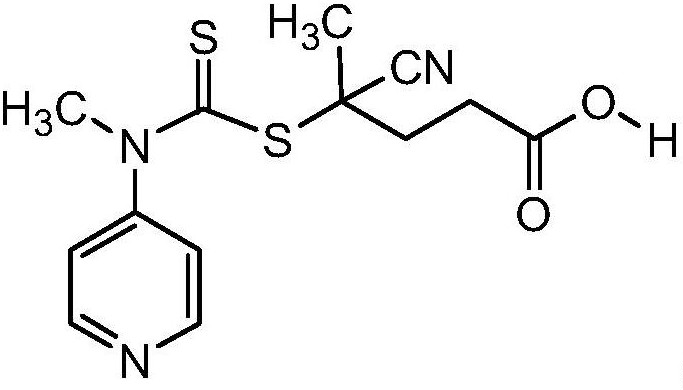
可逆加成斷裂鏈轉移聚合採用的RAFT試劑SC(Z)S-R,R基團末端含有羧基,其結構式為:
既含氨基又含巰基的化合物NH2(CH2)nSH的結構式為:
其中該化合物的n取值如何界定;n=1~6。
食人魚洗液(piranha溶液);巰基化聚乙烯基吡咯烷酮(HS-PVP)
技術方案
《一種利用可控接枝技術提高材料表面血液相容性的方法》的目的通過以下技術方案實現:
一種利用可控接枝技術提高材料表面血液相容性的方法,包括如下步驟:
1)將單體NVP、RAFT試劑和溶劑乙腈置於容器中,加入引發劑AIBN,混合均勻;
2)進行液氮除氧,在60-80℃的恆溫油浴中反應,經過5-48小時聚合後,放入液氮驟冷終止反應;產物加入無水乙醚進行沉澱;沉澱產物放在常溫真空乾燥箱至恆重,得到PVP-COOH;
3)將PVP-COOH、DCC和NHS混合;在氮氣氛圍下向混合物中加入乾燥的二氯甲烷,在冰水浴條件下反應0.5-3小時;
4)加入巰基乙胺,常溫下避光反應6-18小時;將溶劑蒸發乾淨,得到粗製樣品;
5)將步驟4)得到的粗製樣品溶於水,在避光下使用去氧水透析,然後冷凍乾燥得到HS-PVP;
6)將金片表面利用piranha溶液進行處理;
7)以乙醇為溶劑,溶解所述HS-PVP,得HS-PVP溶液;
8)將HS-PVP溶液置於PE管中,放入步驟6)得到的金片,使金片與巰基間進行化學吸附反應;
9)將步驟8)的金片取出,利用去離子水和乙醇充分清洗,得到具有優異血液相容性材料表面。
為進一步實現《一種利用可控接枝技術提高材料表面血液相容性的方法》目的,優選地,所述RAFT試劑與單體NVP的摩爾比為1:20-1:500。
優選地,所述引發劑AIBN與RAFT試劑的摩爾比為1:2-1:20。
優選地,所述PVP-COOH、DCC與NHS的摩爾比為1:1:1.2-1:4:4.8。
優選地,以每克PVP-COOH計,所述二氯甲烷的用量為2-20毫升。
優選地,所述PVP-COOH與巰基乙胺摩爾比為1:1-1:3。
優選地,所述透析時間為12-48小時,每隔2-4小時換一次水;所述液氮除氧的次數為3-5次。
優選地,所述piranha溶液中雙氧水與濃硫酸的體積比為3:7,處理時間為5-15分鐘。
優選地,所述HS-PVP(巰基化聚乙烯基吡咯烷酮)的濃度為1毫克-50毫克/毫升。
優選地,所述金片與巰基間進行化學吸附反應的時間為0.5-3小時,溫度為25-37℃,反應中氧含量低於2百萬分比濃度,且避光。
改善效果
《一種利用可控接枝技術提高材料表面血液相容性的方法》具有如下優點:
(1)該發明製備具有優異血液相容性材料表面,抗蛋白吸附性能和生物相容性能優異;
(2)該發明製備的具有優異血液相容性材料表面具有良好的化學穩定性,不易降解;
(3)該發明製備的具有優異血液相容性材料表面可以抑制95%的人血白蛋白和約85%的纖維蛋白原在其表面的粘附。
(4)該發明可以控制接枝分子的接枝鏈長,可以得到不同接枝分子量修飾的材料表面。
附圖說明
圖1-1為空白金面XPS測試C譜圖
圖1-2為空白金面XPS測試N譜圖;
圖1-3為空白金面XPS測試O譜圖;
圖2-1為實施例1中PVP修飾後金面XPS測試C譜圖;
圖2-2為實施例1中PVP修飾後金面XPS測試N譜圖;
圖2-3為實施例1中PVP修飾後金面XPS測試O譜圖;
圖3-1為實施例1人血白蛋白HSA吸附量測試結果圖;
圖3-2為實施例2人血白蛋白HSA吸附量測試結果圖;
圖3-3為實施例3人血白蛋白HSA吸附量測試結果圖;
圖4-1為實施例1纖維蛋白原Fg吸附量測試結果圖;
圖4-2為實施例2纖維蛋白原Fg吸附量測試結果圖;
圖4-3為實施例3纖維蛋白原Fg吸附量測試結果圖。
技術領域
《一種利用可控接枝技術提高材料表面血液相容性的方法》涉及一種具有抗蛋白吸附材料,特別是涉及一種利用可控接枝技術提高材料表面血液相容性的方法,是一種具有抗蛋白吸附材料表面的製備方法。
權利要求
1.一種利用可控接枝技術提高材料表面血液相容性的方法,其特徵在於包括如下步驟:
1)將單體NVP、RAFT試劑和溶劑乙腈置於容器中,加入引發劑AIBN,混合均勻;所述的RAFT試劑為SC(Z)S-R,R基團末端含有羧基,結構式為:
2)進行液氮除氧,在60-80℃的恆溫油浴中反應,經過5-48小時聚合後,放入液氮驟冷終止反應;產物加入無水乙醚進行沉澱;沉澱產物放在常溫真空乾燥箱至恆重,得到PVP-COOH;
3)將PVP-COOH、DCC和NHS混合;在氮氣氛圍下向混合物中加入乾燥的二氯甲烷,在冰水浴條件下反應0.5-3小時;
4)加入巰基乙胺,常溫下避光反應6-18小時;將溶劑蒸發乾淨,得到粗製樣品;
5)將步驟4)得到的粗製樣品溶於水,在避光下使用去氧水透析,然後冷凍乾燥得到HS-PVP;
6)將金片表面利用piranha溶液進行處理;
7)以乙醇為溶劑,溶解所述HS-PVP,得HS-PVP溶液;
8)將HS-PVP溶液置於PE管中,放入步驟6)得到的金片,使金片與巰基間進行化學吸附反應;
9)將步驟8)的金片取出,利用去離子水和乙醇充分清洗,得到具有優異血液相容性材料表面。
2.根據權利要求1所述的方法,其特徵在於,所述RAFT試劑與單體NVP的摩爾比為1:20-1:500。
3.根據權利要求1所述的方法,其特徵在於,所述引發劑AIBN與RAFT試劑的摩爾比為1:2-1:20。
4.根據權利要求1所述的方法,其特徵在於,所述PVP-COOH、DCC與NHS的摩爾比為1:1:1.2-1:4:4.8。
5.根據權利要求1所述的方法,其特徵在於,以每克PVP-COOH計,所述二氯甲烷的用量為2-20毫升。
6.根據權利要求1所述的方法,其特徵在於,所述PVP-COOH與巰基乙胺摩爾比為1:1-1:3。
7.根據權利要求1所述的方法,其特徵在於,所述透析時間為12-48小時,每隔2-4小時換一次水;所述液氮除氧的次數為3-5次。
8.根據權利要求1所述的方法,其特徵在於,所述piranha溶液中雙氧水與濃硫酸的體積比為3:7,處理時間為5-15分鐘。
9.根據權利要求1所述的方法,其特徵在於,所述HS-PVP的濃度為1毫克-50毫克/毫升。
10.根據權利要求1所述的方法,其特徵在於,所述金片與巰基間進行化學吸附反應的時間為0.5-3小時,溫度為25-37℃,反應中氧含量低於2百萬分比濃度,且避光。
實施方式
一種利用可控接枝技術提高材料表面血液相容性的方法,包括如下步驟:
(1)稱量單體NVP(4毫升,0.0371摩爾),RAFT試劑(0.2402克,6×10摩爾),4毫升溶劑乙腈置於安培瓶中,最後加入0.028克引發劑AIBN,混合均勻,對安培瓶進行液氮除氧三次,在70℃的恆溫油浴中反應,反應15小時,將安培瓶放入液氮驟冷終止反應;
(2)將步驟(1)安培瓶中的產物加入無水乙醚進行沉澱;放在常溫真空乾燥箱至恆重,得到的PVP-COOH樣品;
(3)稱取樣品1克PVP-COOH、0.1212克DCC和0.0744克NHS置於兩口燒瓶中,在氮氣氛圍下加入5毫升乾燥的二氯甲烷,在冰水浴條件下反應1小時,然後加入0.0445克巰基乙胺,常溫下避光反應12小時,將溶劑蒸發乾淨,得到粗製樣品;
(4)將步驟(3)得到的粗製樣品溶於水,在避光下使用去氧水透析,然後冷凍乾燥得到樣品HS-PVP1;
(5)將1×1厘米金片表面放入食人魚洗液(piranha溶液)進行處理;
(6)取10毫升乙醇,溶解20毫克的HS-PVP1;
(7)取5毫升配製好的HS-PVP1溶液置於PE管中,將步驟(5)得到的直徑1厘米金片放入,放置150分鐘後取出,利用去離子水和乙醇充分清洗,得到具有抗蛋白吸附的、優異血液相容性的材料表面。
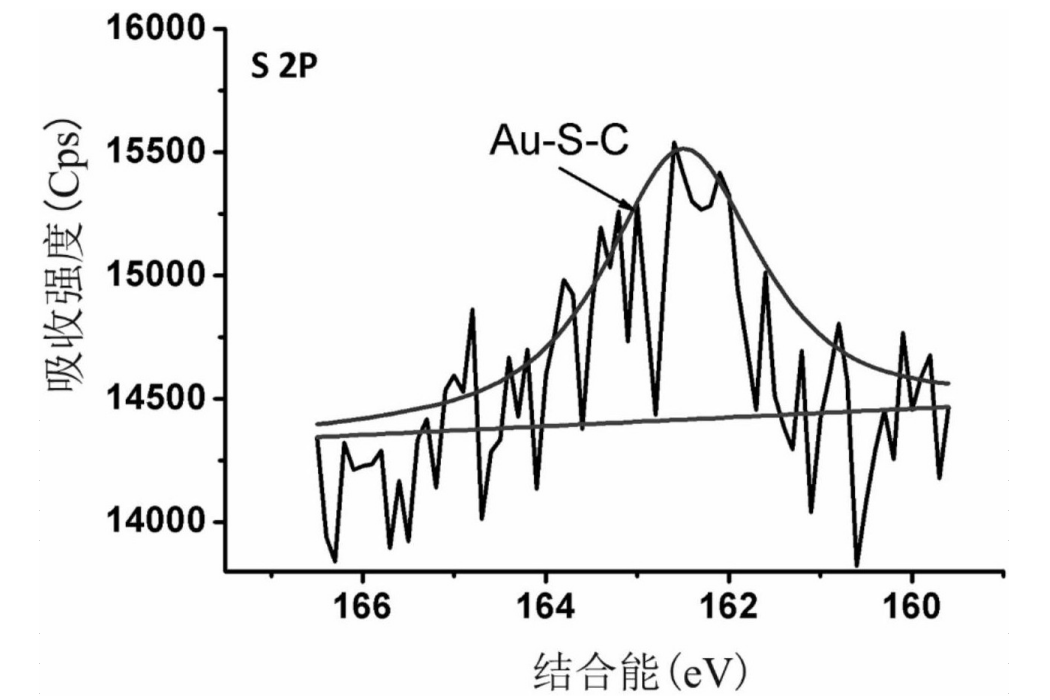
《一種利用可控接枝技術提高材料表面血液相容性的方法》採用型號為Axis UltraDCD的X射線光電子能譜(XPS)對聚乙烯基吡咯烷酮自組裝前後的金片表面進行元素組成和含量的分析。X射線光電子能譜測試結果以C 1s(284.6電子伏特)為基準對譜圖進行校準,利用avantage軟體對C、N、S元素進行擬合譜圖。
如圖1-1、圖1-2、圖1-3,圖2-1、圖2-2和圖2-3為實施例1的XPS測試圖,HS-PVP自組裝於Au表面後,其表面元素含量發生明顯變化,元素所處的化學環境也會發生明顯變化,其中,圖1-1、圖1-2、圖1-3為空白樣的測試結果,空白樣的表面N和S元素,C元素只有一種結合狀態;圖2-1、圖2-2和圖2-3為改性後的材料表面測試結果圖,發現HS-PVP改性後的材料表面出現了N和S元素,且C元素出現三種結合狀態。對比圖1-1、圖1-2、圖1-3,圖2-1、圖2-2和圖2-3結果表明HS-PVP1可成功接枝於材料表面。
可通過石英晶體微天平(QCM-D)研究聚乙烯基吡咯烷酮自組裝金片後的材料表面對蛋白(人血漿白蛋白和人纖維蛋白原)吸附行為得到的結果;其中蛋白濃度為1毫克/毫升PBS溶液,吸附量是通過QCM-D測試得到的F變化以及軟體擬合得到。人體血液含有多種蛋白,其中人血清白蛋白的含量最多,當材料與人體血液接觸時,人血清白蛋白和纖維蛋白原在材料表面的吸附對血栓的形成有著重要影響,因而人體血液白蛋白(HSA)和纖維蛋白原(Fg)是研究材料血液相容性的常用蛋白。
空白樣為Au,HS-PVP接枝修飾後的材料為Au-PVP,圖3-1和圖4-1分別為通過石英晶體微天平(QCM-D)測試得到的材料(Au和Au-PVP)表面對人體血液白蛋白(HSA)和纖維蛋白原(Fg)的吸附量柱狀圖。從測試結果可以看出,PVP成功修飾於材料表面,且相比空白樣,改性後的材料表面可以減少95.32%的人血白蛋白和84.76%的纖維蛋白原在其表面的粘附。細胞相容性實驗結果表明,99.51%的細胞可以存活。
從圖3-1和圖4-1中可以看出,相比空白樣Au,改性後的材料表面可以明顯地減少人血白蛋白和纖維蛋白原在其表面的粘附。
用石英晶體微天平(QCM-D)測試HS-PVP在材料表面的接枝過程。,石英晶體微天平(QCM)的核心是石英晶體感測器。當感測器兩端施加電壓時,石英晶體會在共振頻率處引發一個小的剪下振動。如果在晶體表面即樣品表面上吸附一層物質,晶體的振動就會減弱,並且這種振動的減弱或者頻率的降低隨著薄膜的厚度和密度變化。即當晶片表面有物質吸附時,晶片的頻率會降低,即表面晶體表面質量變化導致頻率變化得到Δf,Δf曲線表示樣品表面質量變化。
在以乙醇作為基線的情況下,當通入含HS-PVP的乙醇溶液後Δf曲線出現明顯變化,大概在30分鐘處出現轉折,Δf變化均變緩慢,自組裝時間為150分鐘時,Δf基本達到平衡,而在150分鐘後通入乙醇,出現比較大幅度的上升,對應的Δf分別為-19.67赫茲,-21.69赫茲,-24.59赫茲,這表明HS-PVP溶液接觸Au表面時,在Au表面同時存在HS-PVP的自組裝及其物理吸附兩個過程,通入乙醇後Δf的變化可能是由於表面一些只是物理吸附在Au表面的HS-PVP被乙醇沖刷帶走而導致;10分鐘後Δf曲線重新達到平衡狀態,HS-PVP已比較牢固地接枝於材料表面。由於接枝前後通入的液體是一致的,通入可以溶解HS-PVP的溶劑後,Δf曲線重新達到平衡狀態,即HS-PVP接枝於材料的質量達到一個穩定狀態,通過良溶劑沖洗,也無法使其從樣品表面脫落,說明以當前條件下,HS-PVP接枝於材料表面,且無法沖洗使其脫落,可說明HS-PVP已比較牢固地接枝於材料表面。
利用QTools軟體擬合得到HS-PVP1在乙醇溶液中接枝於材料表面的質量約為2.03微克/平方厘米。說明了HS-PVP在材料表面的接枝過程,隨著時間的變化,HS-PVP接枝於材料表面的質量也會隨著變化。目的是展現HS-PVP在材料表面的接枝過程中質量變化過程。2.03微克/平方厘米是通過石英晶體微天平(QCM0-D)自帶軟體QTools擬合得到的,該值說明HS-PVP接枝於材料表面的接枝密度。
一種利用可控接枝技術提高材料表面血液相容性的方法,其步驟如下:
(1)稱量單體NVP(4毫升,0.0371摩爾),RAFT試劑(0.1201克,3×10摩爾),4毫升溶劑乙腈置於安培瓶中,最後加入0.014克引發劑AIBN,混合均勻,對燒瓶進行液氮除氧三次,在80℃的恆溫油浴中反應,反應24小時,將安培瓶放入液氮驟冷終止反應;
(2)將步驟(1)燒瓶中的產物加入無水乙醚進行沉澱;放在常溫真空乾燥箱至恆重,得到的PVP-COOH樣品;
(3)稱取樣品1克PVP-COOH、0.0606克DCC和0.0372克NHS置於兩口燒瓶中,在氮氣氛圍下加入10毫升乾燥的二氯甲烷,在冰水浴條件下反應1小時,然後0.0225克巰基乙胺,常溫下避光反應12小時,將溶劑蒸發乾淨,得到粗製樣品;
(4)將步驟(3)得到的粗製樣品溶於水,在避光下使用去氧水透析,然後冷凍乾燥得到最終樣品HS-PVP2;
(5)將1×1厘米金片表面放入食人魚洗液進行處理15分鐘;
(6)取10毫升乙醇,溶解30毫克的HS-PVP2;
(7)取5毫升配製好的HS-PVP溶液置於PE管中,將步驟(5)得到的直徑1厘米金片放入,放置150分鐘後取出,利用去離子水和乙醇充分清洗,得到具有抗蛋白吸附的、具有優異血液相容性的材料表面。
圖3-2和圖4-2為材料表面對人體血液白蛋白(HSA)和纖維蛋白原(Fg)的吸附量柱狀圖,圖3-2和圖4-2的測試方式與實施例1相同。只是實施例2使用了另一種分子量的HS-PVP(HS-PVP2)。從圖3-2和圖4-2測試結果可以看出,PVP成功修飾於材料表面,且相比空白樣,改性後的材料表面可以減少88.31%的人血白蛋白和78.97%的纖維蛋白原在其表面的粘附。
一種利用可控接枝技術提高材料表面血液相容性的方法,其步驟如下:
(1)稱量單體NVP(4毫升,0.0371摩爾),RAFT試劑(0.0601克,1.5×10摩爾),4毫升溶劑乙腈置於安培瓶中,最後加入0.010克引發劑AIBN,混合均勻,對燒瓶進行液氮除氧三次,在80℃的恆溫油浴中反應,反應36小時,將安培瓶放入液氮驟冷終止反應;
(2)將步驟(1)燒瓶中的產物加入無水乙醚進行沉澱;放在常溫真空乾燥箱至恆重,得到的PVP-COOH樣品;
(3)稱取樣品1克PVP-COOH、0.0303克DCC和0.0186克NHS置於兩口燒瓶中,在氮氣氛圍下加入10毫升乾燥的二氯甲烷,在冰水浴條件下反應1小時,然後0.0113克巰基乙胺,常溫下避光反應24小時,將溶劑蒸發乾淨,得到粗製樣品;
(4)將步驟(3)得到的粗製樣品溶於水,在避光下使用去氧水透析,然後冷凍乾燥得到最終樣品HS-PVP3;
(5)將1×1厘米金片表面放入食人魚洗液進行處理15分鐘;
(6)取10毫升乙醇,溶解50毫克的HS-PVP3;
(7)取5毫升配製好的HS-PVP3溶液置於PE管中,將步驟(1)得到的直徑1厘米金片放入,放置150分鐘後取出,利用去離子水和乙醇充分清洗,得到具有抗蛋白吸附的、優異血液相容性的材料表面。
圖3-3和圖4-3為材料表面對人體血液白蛋白(HSA)和纖維蛋白原(Fg)的吸附量柱狀圖,圖3-3和圖4-3的測試方式與實施例1相同。與實施例1相似,該實施例3使用了另一種分子量的HS-PVP(HS-PVP3)。從測試結果可以看出,PVP成功修飾於材料表面,且相比空白樣,改性後的材料表面可以減少81.21%的人血白蛋白和75.23%的纖維蛋白原在其表面的粘附,且細胞相容性實驗結果表明,98%的細胞可以存活。
《一種利用可控接枝技術提高材料表面血液相容性的方法》控制接枝密度是通過控制HS-PVP與材料表面的接觸時間實現,而控制接枝鏈長則是通過控制HS-PVP的分子量實現,不同的分子量接枝於材料表面得到不同分子量聚乙烯基吡咯烷酮修飾的材料表面。
表1是實施例1-3所用的HS-PVP的分子量以及分子量分布,說明《一種利用可控接枝技術提高材料表面血液相容性的方法》可以通過製備不同的分子量的樣品進行接枝實驗來控制接枝分子(即接枝鏈)的長度。
圖3-1、圖3-2、圖3-3、圖4-1、圖4-2和圖4-3為不同接枝分子量修飾的材料表面對人血白蛋白和纖維蛋白原的吸附性能柱狀圖,從這些圖可以明顯看出經過HS-PVP修飾的材料表面對蛋白的吸附量相比於空白樣Au明顯減少,達到75%以上,對人血白蛋白和纖維蛋白原的非特異性吸附明顯減少,表明製備的樣品具有優異的血液相容性。
從實施例1-3可以說明《一種利用可控接枝技術提高材料表面血液相容性的方法》可以控制接枝分子的接枝鏈長,可以得到不同接枝分子量修飾的材料表面,並且製備的材料表面可以有效抑制人血白蛋白和纖維蛋白原在其表面的粘附,使其具有優異的血液相容性。
專利榮譽
2021年6月24日,《一種利用可控接枝技術提高材料表面血液相容性的方法》獲得第二十二屆中國專利銀獎。