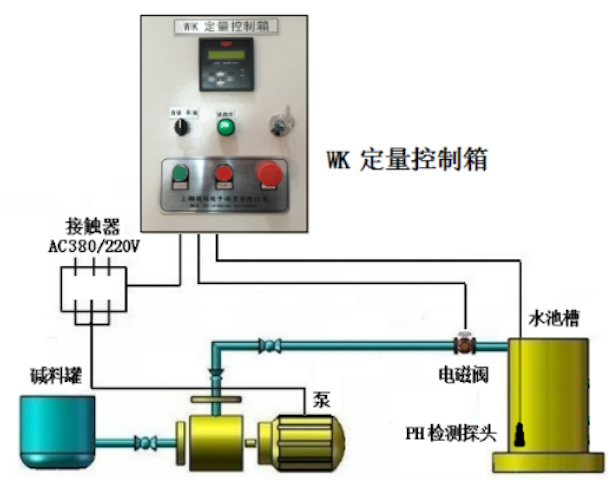
pH自動控制系統多採用可程式控制器作為調節器,可以同時輸入多種信號,如pH值, 輸入流量值,儲槽液位,控制閥狀態等信息。控制系統將輸入的各信息量進行一定運算,根據pH測定值準確地計算出需要的中和劑的計量值,準確控制加藥量。pH自動控制系統套用於眾多的工業生產過程和廢水處理過程。
基本介紹
- 中文名:pH自動控制系統
- 外文名:PH automatic control system
- 系統構成:玻璃電極、調節閥、加藥裝置等
- 控制特徵:平衡遲緩和震盪、非線性
- 套用:工業生產過程和廢水處理過程
- 套用學科:控制科學、冶金學、儀器科學
簡介,pH自動控制系統組成相關,pH測量設備,PH計的日常維護,調節對象,執行機構,常見pH自動控制系統,閾值控制,反饋控制,pH控制過程的特徵,中和滴定曲線,非線性,平衡遲緩和震盪,
簡介
pH自動控制系統套用於眾多的工業生產過程和廢水處理過程。在pH控制過程中,中和試劑供給量變化範圍可能達到幾個數量級,而且控制過程中的測量信號(pH值)與控制的加藥量之間,具有強烈的非線性關係。
pH自動控制系統多採用可程式控制器作為調節器,可以同時輸入多種信號,如pH值,輸入流量值,儲槽液位,控制閥狀態等信息。控制系統將輸入的各信息量進行一定運算,組成智慧型性控制系統。當被處理的液體的中和滴定曲線已知時,控制系統可以根據pH測定值準確地計算出需要的中和劑的計量值,準確控制加藥量。同時,當整個處理系統確定後,其平衡遲緩可以實地測定,據此,可以抑制甚至排除因平衡遲緩所引起的系統震盪,在保持控制的高靈敏度的同時,保證系統的穩定性。
pH自動控制系統組成相關
pH測量設備
PH值是用溶液中氫離子濃度的負對數來表示的。是衡量水體酸鹼度的一個值,是溶液中氫離子活度的一種標度,也就是通常意義上溶液酸鹼程度的衡量標準。PH測量設備由感測器和變送器組成的。PH感測器俗稱PH探頭,由玻璃電極和參考電極兩部分組成,用玻璃電極與參比電極組成原電池。在玻璃膜與被測溶液中氫離子進行離子交換過程中,通過測量電極之間的電位差來檢測溶液中的氫離子濃度,從而測得被測液體的PH值,由於PH值與溫度有關,所以一般還要增加一個溫度電極進行溫度補償。
玻璃電極是工業上用得最廣泛的指示電極, 它能在相當寬的範圍內有良好的線性關係,並能在較強的酸、鹼溶液中穩定工作。我國目前生產的工業pH 傳送器, 由於結構上的原因,不適台工業廢水處理謊程中使用, 其主要問題是:(1)參比電極的鹽橋常常由於氣泡膽阱或KCI結晶析出而造成測量電池迴路短路。(2)結構複雜而笨重,日常維護、安裝困難。
PH計的日常維護
PH儀感測器的工作電極與參比電極之間的電子通路是通過被測介質進行的,工作電極玻璃膜的沾污會直接影響到測量。若要保持PH的測量敏感性和準確性,玻璃探頭的清洗工作是十分重要的。在正常使用中應每天清理一次探頭保護管周圍的雜物,以便使探頭接觸到的液體為實測介質。每周對探頭進行一次人工清洗,每三個月進行定期校驗。測量池要定期排污清理,防止污泥淤積。
調節對象
pH 值控制系統是一個以其可變增益著稱的成分控制系統。
如圖描述了一條典型的曲線,這是pH 值相對於所加的酸液與流入液體流量之比值的關係曲線。橫坐標是一個比值,它表明過程的增益,即單位酸液流量所引起的pH 值變化, 隨著要處理的流入液體的流量而變化。當被調參數出現偏差時,調節器對於偏差e作出的回響,應該是其輸出量的變化Δm恰好把偏差減小到零。要完成這項任務所需要前調節器增益與過程增益成反比,過程增益可以定義為偏差與消除這個偏差所需的m 的變化量之比值

Kp可用曲線上連線偏差為e和偏差為0這兩個點的直線的斜率來表示,如圖所示。只有在控制點上,pH 曲線的斜率才與該點構過程增益相等。在其它點上,曲線的斜率要比該點的過程增益Kp小稃多,可見pH 值控制系統是一個典型的可變增益系統。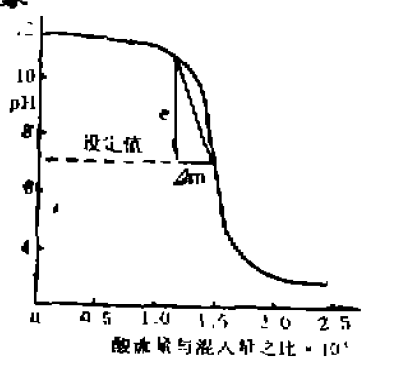

執行機構
調節閥是調節系統中非常重要的一個環節, 因為它處於最終執行調節任務的地位,調節閥選擇的好壞,對系統是否能夠很好起調節作用關係甚大。選調節閥首先要使其流通能力滿足生產要求, 其次要估計調節閥在管線上的阻力降分配比,要使閥在全開情況下占有整個管線阻力降的較大比 ,這是調節閣能否起調節作用的關鍵。如果流經調節闊的阻力降所占的比倒較小,將使調節閥的工作特性發生畸變。而調節閥的流量特性的非線性特性, 可作為過程非線性的一種補償手段。
常見pH自動控制系統
閾值控制
市售的最常見的pH自動控制系統,提供了兩個由使用者設定的閾值。例如pH=6和pH=9。當測得的pH值小於6時,鹼加藥機開;pH大於6時,鹼加藥機關;當測得的pH值大於9時酸加藥機開,小於9時酸加藥機關。這類簡單的自動控制系統一般不能對pH值實行有效的控制,相反會造成系統pH值強烈的震盪。
反饋控制
常規的反饋控制系統採用偏差值(ΔpH)經過各種不同類型的控制規律的運算後,作為控制的輸出。當輸出與偏差之間成非線性關係時,控制系統需要加以非線性補償。但是,一般非線性補償只有在一定的範圍內才有效。當輸出與偏差間的非線性過於強烈時,一般的控制系統是無法勝任的。圖是文獻報導的一個pH值控制過程的真實記錄曲線。該過程設定的pH值是7.5。使用石灰作為鹼添加劑,硫酸作為酸添加劑,由一個常規調節器組成的調節系統。控制系統輸出的記錄曲線顯示出系統的pH值強烈震盪。
pH控制過程的特徵
中和滴定曲線
被處理水水質的pH定量特徵常用其中和滴定曲線來表征。如圖是一實測的中和滴定曲線。水樣取自一染化廠的廢水。圖中的橫坐標為添加的中和劑(此處為0.1molNaOH)的體積毫升數,縱坐標為pH值。廢水初始的pH值為0.69,中和到接近pH=7時,添加的NaOH總量為280.5毫升。 pH 中和滴定曲線
pH 中和滴定曲線
 pH 中和滴定曲線
pH 中和滴定曲線非線性
由圖可見,中和滴定曲線呈S型。曲線在低pH值範圍變化緩慢,添加中和劑總量的95%時,即267毫升的NaOH,僅僅使pH值由0.69上升到2.5左右。而在pH=7附近,曲線變化非常陡峭,添加中和劑總量的1%,即2.8毫升的NaOH,即可使pH值由pH=5.7上升到pH=9.8。
用緩衝指數(BufferIndex:σ=ΔpH/Δφ)定量地表征水樣的pH特徵。由圖可見,在pH=7附近時,σ=1.46(mL/1)。而在低pH值範圍時,σ=0.007(mL/1)。緩衝指數的急劇變化,即pH值變化的強烈的非線性,是pH控制問題中最顯著的一項特徵,也是造成pH控制困難的一個重要原因。
在上述染化廠廢水的例子中,如果需要將廢水的口H控制在6到9之間,則添加劑的誤差不能超過中和劑總量的0.5%。當廢水初始的pH值更低時,控制的精度要求更高。綜上所述,pH值控制問題具有基本特徵是:強烈的非線性;離子濃度(H離子或oH離子)的變化範圍大,從而所需添加的中和劑量的變化範圍可以達到幾個數量級;為了將pH值控制在允許範圍以內,要求非常高的控制精度。正是這些特徵,使得pH的控制問題成為工程控制中最困難的問題之一。
平衡遲緩和震盪
平衡遲緩指的是系統加入擾動後,達到平衡需要的時間。當過程需要連續控制時,平衡遲緩給控制帶來了很大困難,常常導致系統震盪。是一個實驗系統pH值隨時間變化的記錄曲線。在t=t0時刻,由酸液注入裝置向系統加入酸液,系統的pH值開始下降。在t=tm時,酸液擴散至pH計的探頭,測得pH的極小值。但直到t=tb時刻,新加入的酸液才和整個系統均勻混合,達到新的穩定值。顯然,如果系統在達到穩定之前,例如根據在t=tm口時刻測得的pH值作出反應,則會過量添加中和劑,造成系統控制品質的下降。系統達到平衡需要的時間取決於系統的組成、液體的流速、攪拌的效率、加藥機和pH探頭的安裝的位置以及中和反應速度等多種因素。