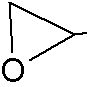
物性數據
1.性狀:無色液體,有類似乙醚的氣味。
2.熔點(℃):-112
3.沸點(℃):34
4.相對密度(水=1):0.83
5.相對蒸氣密度(空氣=1):2.0
6.飽和蒸氣壓(kPa):71.7(25℃)
7.燃燒熱(kJ/mol):-1755.8
8.臨界溫度(℃):209.1
9.臨界壓力(MPa):4.93
10.辛醇/水分配係數:0.03
11.閃點(℃):-37(CC);-28.8(OC)
12.引燃溫度(℃):449
13.爆炸上限(%):36.0
14.爆炸下限(%):2.3
15.溶解性:溶於水,混溶於甲醇、乙醚、丙酮、苯、四氯化碳等多數有機溶劑。
分子結構數據
1、摩爾折射率:15.53
2、摩爾體積(cm3/mol):64.2
3、等張比容(90.2K):144.0
4、表面張力(dyne/cm):25.2
5、極化率(10-24cm3):6.15
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:1
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積12.5
7.重原子數量:4
8.表面電荷:0
9.複雜度:26.5
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:1
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.具有醚類氣味的低沸易燃液體。工業品為兩種旋光異構體的外消旋混合物。環氧丙烷是易燃、易爆化學品,其蒸汽會分解。應避免酸性鹽(如氯化錫、氯化鋅)、鹼類、叔胺等過量會污染環氧丙烷。對金屬無腐蝕性,由於對某些橡膠和塑膠有作用,應注意選擇墊圈和閥門。由於沸點低,揮發性大,易燃,化學性質活潑,應注意防止與電火花、靜電、熱源、酸、鹼等接近。與水部分混溶[20℃時水中溶解度40.5%(重量);水在環氧丙烷中的溶解度12.8%(重量)],與乙醇、乙醚混溶,並與二氯甲烷、戊烷、戊烯、環戊烷、環戊烯等形成二元共沸物。
2.化學性質極其活潑,特別是能與含有活潑氫的化合物反應,生成各種衍生物。例如,與水反應生成1,2-丙二醇;與氨反應生成異丙醇胺;與醇反應生成羥基醚;與脂肪酸反應生成羥基酯;與鹵化氫反應生成鹵代醇;與丙二醇反應生成聚丙二醇;氧化生成乙酸;與甘油反應生成聚醚三元醇;與羧酸反應生成酯等。在500℃通過浮石時部分發生重排,生成丙酮和丙醛。在無水狀態下與氯作用,生成氯代丙酮和1-氯-2-丙醇。氧化時生成乙酸,用鈉汞齊還原生成異丙醇。
3.穩定性:穩定。
4.禁配物:酸類、鹼類、強氧化劑。鐵、錫、鋁的無水氯化物,鐵、鋁的過氧化物、氨水、氯磺酸、鹽酸、氟化氫、硝酸、硫酸、發煙硫酸等。
5.避免接觸的條件:受熱。
6.聚合危害:不聚合。
合成方法
1.氯醇法:由丙烯和氯氣、水在常壓和60℃下經次氯酸化生成氯丙醇,再經皂化、凝縮、蒸餾而得。工藝流程:
(1)丙烯次氯酸化 將丙烯和氯氣分別通入水中進行氣液相反應,反應溫度為35-50℃,丙烯與氯氣摩爾比為(1.1-1.2):1。水與氯氣首先反應生成次氯酸,然後丙烯再與次氯酸進行加成反應生成氯丙醇。為減少副反應,避免二氯丙烷的生成,氯丙醇的濃度不宜過高,一般不高於6%-7%;氯氣不可過量,除氯氣過量將導致副產物二氯乙烷增多外,還有可能引起爆炸的危險性;向反應器通氯氣和丙烯時,應儘量避免兩種氣體的直接接觸。一般將氯氣入口設在丙烯入口下方,而水的入口設在最下方。
(2)氯丙醇脫氯化氫反應 將含水的氯丙醇加入皂化釜中,然後再加10%的石灰乳,攪拌下進行皂化反應,過程中必須注意物料的加入方式,如果將氯丙醇加入到石灰乳中,生成的環氧丙烷處於鹼性介質中,會發生水解生成丙二醇厚。因此,對於氯丙醇脫氯化氫反應,必須將鹼液加到氯丙醇中,以獲得儘可能高的環氧丙烷收率。環氧丙烷生成反應立即蒸出,以避免水解。(3)環氧丙烷的提純蒸出的環氧丙烷經冷凝後,送入精餾塔進行精餾即得成品。
2.直接氧化法:在銀催化作用下,由丙烯與氧或空氣進行氧化製得。
3.間接氧化法:由乙苯(或異丁烷、異丙苯等)經氧化製成氫過氧化乙苯(或叔丁基過氧化氫、氫過氧化異丙苯等),在環烷酸鉬等催化劑存在下,與丙烯進行環氧化反應而得。
4.電化氯醇法:此法利用氯化鈉(或氯化鉀、溴化鈉、碘化鈉)的水溶液,經電解生成氯氣和氫氧化鈉的原理,在陽極區通入丙烯,生成氯丙醇,在陰極區氯丙醇與氫氧化鈉作用生成環氧丙烷。
5.過氧化物法:主要過程為有機過氧化氫的製造,用過氧化物將丙烯氧化。該反應無論是生產有機過氧化氫或在催化劑存在下將過氧化物的氧轉移到丙烯分子上都是液相反應,該方法除主產品環氧丙烷外,還有聯產品。目前已經實現工業化的有乙苯哈康法和異丁烷哈康法。
(1)乙苯哈康法:以乙苯為原料經氧化制乙苯氫過氧化物,在環烷酸銅等催化劑作用下,進行丙烯環氧化反應,得到環氧丙烷,同時得到α-苯乙醇,經脫水可得到苯乙烯。
乙苯氧化的反應溫度為130~150℃,壓力為0.07~0.14 MPa,生成乙苯氫過氧化物的選擇性達90%,環氧化溫度為50~120℃,壓力為常壓0.1~0.864 MPa。例如將乙苯氫過氧化物14%、丙烯35%、乙苯50%、α-苯乙醇1%(質量分數)的混合物加入0.4%環烷酸錳-環烷酸鈉(nMo/nNa=2,摩爾比)作催化劑,在100℃反應1.5 h,得到乙苯氫過氧化物的轉化率為99%,生成環氧丙烷的選擇性78%,反應產物經蒸餾處理可得環氧丙烷成品,而α-苯乙醇在脫水反應器用TiO3-Al2O3作催化劑,在250~280℃脫水,100%轉化為苯乙烯,其選擇性為92%。該方法特點:成本低,經濟合理,三廢少,同時有聯產苯乙烯。
(2)異丁烷哈康法:是以異丁烷為原料,經氧化劑叔丁基氫過氧化物再與丙烯反應得環氧丙烷和叔丁醇,工藝過程與乙苯哈康法類似。製取叔丁基氫過氧化物是在100~110℃,不用催化劑,通常用叔丁基氫過氧化物作繼引發劑,丙烯環氧化的反應條件是反應溫度121℃,壓力4.1 MPa。在鉬催化劑存在下進行,反應時間0.5 h,環氧丙烷的產率為88%(以過氧化物計),選擇性81%。此法可以聯產叔丁醇,產率約60%。
貯存方法
1.儲存注意事項:儲存於陰涼、通風的庫房。庫溫不宜超過29℃。遠離火種、熱源。保持容器密封。應與氧化劑、酸類、鹼類分開存放,切忌混儲。採用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備和合適的收容材料。
2.環氧丙烷為低沸、易燃液體,其蒸氣在空氣中能自燃或爆炸,應按有毒危險品規定貯運。貯槽和反應器等宜覆蓋以惰性氣體。容器的溫度、壓力應保持在25℃、0.3Mpa以下。施行有關安全防火防爆措施。貯運容器宜用不鏽鋼制。
用途
環氧丙烷是重要的有機化工原料,為丙烯系的第三大產品,最大用途是制聚醚多元醇,進而製造聚氨酯,在美國和西歐的用途分配中,這方面的用途分別占60%和70%以上。用於製造非離子表面活性劑和丙烯醇、丙二醇、醇醚、碳酸丙烯酯、異丙醇胺、丙醛、合成甘油、有機酸、合成樹脂、泡沫塑膠、增塑劑、乳化劑、濕潤劑、洗滌劑、殺菌劑、熏蒸劑等。環氧丙烷衍生的精細化學品幾乎套用於所有工業部門和日常生活中。另外,環氧丙烷還少量用於塗料、剎車液、防凍劑、噴氣發動機燃油添加劑、地板拋光劑、印刷油墨、電子化學品、清潔劑、選礦劑、皮革加工、PS版用感光液、短效增塑劑、染料、非離子型表面活性劑、油田破乳劑、阻燃劑、農藥乳化劑及潤濕劑等行業。也用於有機合成。用作硝酸纖維素、醋酸纖維素、各種樹脂的溶劑,氯乙烯樹脂和含氯溶劑的穩定劑,硝基噴漆褪色的防止劑等。還用於表面活性劑(潤濕劑、洗滌劑、乳化劑等)以及醫藥、農藥、香料、人造皮革的製造。
毒理學數據
1.急性毒性:
LD50:380mg/kg(大鼠經口);1245mg/kg(兔經皮)。
LC50:4000ppm(大鼠吸入,4h);4127mg/m3(小鼠吸入,4h)。
2.刺激性:
家兔經皮:50mg(6min),重度刺激;415mg,中度刺激(開放性刺激試驗)。
家兔經眼:20mg(2h),中度刺激。
3.亞急性與慢性毒性:0.3g/kg灌胃,每周5次,18次,大鼠體重減輕,出現胃刺激和肝臟損害。
4.致突變性:微生物致突變:鼠傷寒沙門菌350μg/皿。DNA損傷:大腸桿菌1μmol/L。顯性致死實驗:大鼠吸入300ppm(5d)(間歇)。細胞遺傳學分析:人淋巴細胞1850μg/L。姐妹染色單體交換:人淋巴細胞25000ppm。
5.致畸性:大鼠孕後7~16d吸入最低中毒劑量(TCLo)500ppm(7h),致肌肉骨骼系統、顱面部(包括鼻、舌)發育畸形。
6.致癌性: IARC致癌性評論:G2B,可疑人類致癌物。
7.其他:大鼠吸入最低中毒濃度(TCLo):500ppm(7h)(孕後7~16d用藥),致胚胎毒性,致肌肉骨骼發育異常。
生態學數據
1.生態毒性:
LC50:170mg/L(24h)(金魚);
TLm:141mg/L(96h)(食蚊魚,靜態);
215mg/L(96h)(藍鰓太陽魚,靜態)。
2.生物降解性:MITI-I測試,初始濃度100ppm,污泥濃度30ppm,2周后降解96%。
3.非生物降解性:
空氣中,當羥基自由基濃度為5.00×105個/cm3時,降解半衰期為30d(理論)。
在25℃,當pH值為7~9.5時,水解半衰期分別為11.6d,6.6d(理論)。