《製備2-腈基聯苯衍生物的方法》是浙江華海藥業股份有限公司於2003年10月15日申請的發明專利,該專利的申請號為2003101080306,公布號為CN1528740,公布日為2004年9月15日,發明人是肖永鵬、何琦、陳寶珍。
《製備2-腈基聯苯衍生物的方法》是一種採用在金屬錳或錳的氧化物及含磷的鹵化物為催化劑由格氏試劑與2-鹵代苯腈縮合來製備2-腈基聯苯衍生物,該發明提供了一種催化效果好、收率高、成本低的環保的製備2-腈基聯苯衍生物的方法。
2014年11月6日,《製備2-腈基聯苯衍生物的方法》獲得第十六屆中國專利優秀獎。
基本介紹
- 中文名:製備2-腈基聯苯衍生物的方法
- 公布號:CN1528740
- 公布日:2004年9月15日
- 申請號:2003101080306
- 申請日:2003年10月15日
- 申請人:浙江華海藥業股份有限公司
- 地址:浙江省臨海市汛橋開發區
- 發明人:肖永鵬、何琦、陳寶珍
- 分類號:C07C255/50、C07C253/30
- 代理機構:杭州天正專利事務所有限公司
- 類別:發明專利
- 代理人:黃美娟、王兵
專利背景,發明內容,專利目的,技術方案,改善效果,權利要求,實施方式,榮譽表彰,
專利背景
高血壓、心臟病、中風、大腦卒中、腎炎之類循環系統疾病正嚴重威脅人類的健康,經過大量研究發現,血管緊張素II(簡稱A(II)拮抗體是治療此類疾病較好的、可行的藥物。進入20世紀90年代以來(截至2003年10月),世界各國加緊了開發研製拮抗體藥物的步伐,已有“洛沙坦”、“頡沙坦”、“伊普沙坦”、“伊貝沙坦”等多種藥物套用於臨床治療。
2-腈基聯苯衍生物則是這些拮抗體藥物的重要中間體,伴隨著藥品開發已經研製成功。合成方法分為保護基多步合成法、催化一步合成法和芳構化閉環合成法。而採用閉環合成法,則僅具有實驗室價值;保護基多步合成法中保護基的形成與除去產生了大量不必要的污染,生產綜合費用高,也可能是此基礎中間體向開發中國家轉移的原因;而催化劑法則具有收率高、選擇性好、副產品少、污染物少、製備投入少、原料價廉易得等優點,如能在中國國內儘快實現工業生產,將對國際上採用多步法的生產產生極大的衝擊,前期投入的回報也將是巨大的。
2003年10月以前技術中,製備2-腈基聯苯衍生物的催化劑法主要包括Ni催化劑和錳催化劑兩種。Ni催化劑法是指製備2-腈基聯苯衍生物過程中採用Ni系列催化劑,但必需要有ZnCl2和季銨鹽存在下才能進行。該方法反應收率較高,至少可達80%以上,但製備過程中使用了較為昂貴的季銨鹽作催化劑,使之不具有工業化價值。錳催化劑法採用原料均採用對鹵甲苯和鄰鹵苯腈,使用催化劑均含有錳。
日本專利JP06-9536所公開的製備方法中使用MnX2(X=I、Br、Cl)作催化劑,該方法由於MnX2含有4個結晶水,極易吸潮,使催化活性降低,以至於影響了收率;
美國專利US639208提供了一種聯苯腈的製備方法,以錳鹽為主催化劑以及過渡金屬為助催化劑,此法所用的助催化劑較難取得。
歐洲專利EP854135A2、JP8109143、JP8231454所公開的製備方法使用MnO2和TMSiCl作催化劑,其中MnO2工業上大多使用電解極,該含量一般只有91%左右,催化效果受影響,而且TMSiCl為有機物質,其催化效果不穩定,對環境也易造成污染,且成本較高。針對2003年10月前對鹵甲苯和鄰鹵苯腈製備2-腈基聯苯衍生物所採用的催化劑對環境易造成污染,且成本較高的不足,有必要設計一種催化效果好、對環境污染小,成本低製備2-腈基聯苯衍生物的方法。
發明內容
專利目的
為了克服已有技術中催化效果不穩定、對環境也易造成污染的、成本高的不足,《製備2-腈基聯苯衍生物的方法》提供了一種催化效果好、收率高、成本低的環保的製備2-腈基聯苯衍生物的方法。
技術方案
《製備2-腈基聯苯衍生物的方法》所述化合物結構如式(I)所示:

它由格氏試劑(II)與2-鹵代苯腈(III)縮合而成,

即反應式為: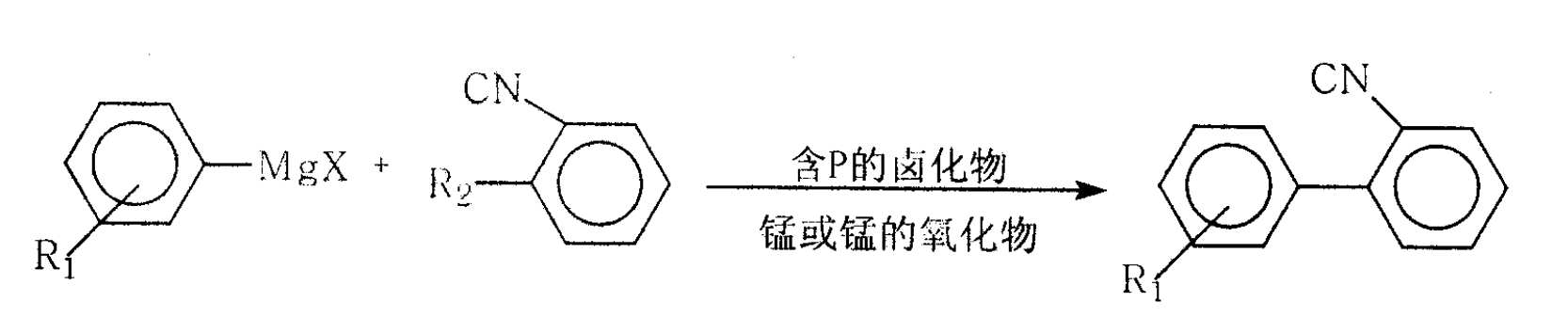

其中結構式(I)、結構式(II)中R1為含有1~6個碳原子的烷基、或含有1~6個碳原子烷氧基、或氫;結構式(III)中R2為Cl、Br;其特徵在於所述的製備方法是將催化劑錳或錳的氧化物及含磷的鹵化物和2-鹵代苯腈(III)加入以醚為底物的有機溶劑中,和格氏試劑(II)反應,生成2-腈基聯苯衍生物(I)。
所述的結構式(I)、結構式(II)中R1所代表的含有1-6個碳原子的烷基包括支鏈和直鏈烷基,例如:直鏈烷基:甲基、乙基、正丙基、正丁基、戊基、己基等,支鏈烷基:異丙基、仲丁基、異丁基、叔丁基、等。當R1為甲基時,化合物(I)即為4’-甲基-2-腈基聯苯,該化合物是沙坦類藥物的關鍵中間體。
R1所代表含有1-6個碳原子的烷氧基包括甲氧基、乙氧基、丙氧基、異丙氧基、正丁氧基、異丁氧基、仲丁氧基、叔丁氧基、戊氧基、己氧基等等。
格氏試劑(II)包括:苯基氯化鎂、鄰甲苯基氯化鎂、間甲苯基氯化鎂、對甲苯基氯化鎂、鄰乙苯基氯化鎂、間乙苯基氯化鎂、對乙苯基氯化鎂、鄰丙苯基氯化鎂、間丙苯基氯化鎂、對丙苯基氯化鎂、鄰異丙苯基氯化鎂、間異丙苯基氯化鎂、對異丙苯基氯化鎂、鄰正丁苯基氯化鎂、間正丁苯基氯化鎂、對正丁苯基氯化鎂、鄰異丁苯基氯化鎂、間異丁苯基氯化鎂、對異丁苯基氯化鎂、鄰仲丁苯基氯化鎂、間仲丁苯基氯化鎂、對仲丁苯基氯化鎂、鄰戊苯基氯化鎂、間戊苯基氯化鎂、對戊苯基氯化鎂、鄰己苯基氯化鎂、間己苯基氯化鎂、對己苯基氯化鎂、鄰甲氧基苯基氯化鎂、間甲氧基苯基氯化鎂、對甲氧基苯基氯化鎂、鄰乙氧基苯基氯化鎂、間乙氧基苯基氯化鎂、對乙氧基苯基氯化鎂、鄰正丙氧基苯基氯化鎂、間正丙氧基苯基氯化鎂、對正丙氧基苯基氯化鎂、鄰正丁氧基苯基氯化鎂、間正丁氧基苯基氯化鎂、對正丁氧基苯基氯化鎂、鄰異丁氧基苯基氯化鎂、間異丁氧基苯基氯化鎂、對異丁氧基苯基氯化鎂、鄰仲丁氧基苯基氯化鎂、間仲丁氧基苯基氯化鎂、對仲丁氧基苯基氯化鎂、鄰叔丁氧基苯基氯化鎂、間叔丁氧基苯基氯化鎂、對叔丁氧基苯基氯化鎂、鄰戊氧基苯基氯化鎂、間戊氧基苯基氯化鎂、對戊氧基苯基氯化鎂、鄰己氧基苯基氯化鎂、間己氧基苯基氯化鎂、對己氧基苯基氯化鎂、苯基溴化鎂、鄰甲苯基溴化鎂、間甲苯基溴化鎂、對甲苯基溴化鎂、鄰乙苯基溴化鎂、間乙苯基溴化鎂、對乙苯基溴化鎂、鄰丙苯基溴化鎂、間丙苯基溴化鎂、對丙苯基溴化鎂、鄰異丙苯基溴化鎂、間異丙苯基溴化鎂、對異丙苯基溴化鎂、鄰正丁苯基溴化鎂、間正丁苯基溴化鎂、對正丁苯基溴化鎂、鄰異丁苯基溴化鎂、間異丁苯基溴化鎂、對異丁苯基溴化鎂、鄰仲丁苯基溴化鎂、間仲丁苯基溴化鎂、對仲丁苯基溴化鎂、鄰戊苯基溴化鎂、間戊苯基溴化鎂、對戊苯基溴化鎂、鄰己苯基溴化鎂、間己苯基溴化鎂、對己苯基溴化鎂、鄰甲氧基苯基溴化鎂、間甲氧基苯基溴化鎂、對甲氧基苯基溴化鎂、鄰乙氧基苯基溴化鎂、間乙氧基苯基溴化鎂、對乙氧基苯基溴化鎂、鄰正丙氧基苯基溴化鎂、間正丙氧基苯基溴化鎂、對正丙氧基苯基溴化鎂、鄰正丁氧基苯基溴化鎂、間正丁氧基苯基溴化鎂、對正丁氧基苯基溴化鎂、鄰異丁氧基苯基溴化鎂、間異丁氧基苯基溴化鎂、對異丁氧基苯基溴化鎂、鄰仲丁氧基苯基溴化鎂、間仲丁氧基苯基溴化鎂、對仲丁氧基苯基溴化鎂、鄰叔丁氧基苯基溴化鎂、間叔丁氧基苯基溴化鎂、對叔丁氧基苯基溴化鎂、鄰戊氧基苯基溴化鎂、間戊氧基苯基溴化鎂、對戊氧基苯基溴化鎂、鄰己氧基苯基溴化鎂、間己氧基苯基溴化鎂、對己氧基苯基溴化鎂等等。
所述的製備方法按如下步驟進行:
a.將催化劑錳或錳的氧化物、含磷的鹵化物和2-鹵代苯腈加入到以醚為底物的有機溶劑中,要求有機容劑中必須有醚,所述的錳或錳的氧化物與2-鹵代苯腈摩爾比為0.01~0.3:1,所述的含磷的鹵化物與2-鹵代苯腈摩爾比為0.003~0.3:1,所述的有機溶劑重量為2-鹵代苯腈的1~25倍;
b.待錳或錳的氧化物、含磷的鹵化物與2-鹵代苯腈在0~100℃下絡合完全後,將格氏試劑慢慢加入其中,在-50~70℃下縮合反應2~24小時,所述的格氏試劑與鹵代苯腈摩爾比為1~3:1;
c.縮合反應完全後,用稀酸溶液水解,分去水層,提取液經濃縮、重結晶步驟分離即得純品產物。
製備方法中所述的2-鹵代苯腈優選2-氯代苯腈。
製備方法所述的含磷的鹵化物可為下式之一:①PCl3②PCl5③POCl3④PBr3⑤PBr5⑥POBr3;其中最優選含磷的氯化物。
製備方法所用的錳或錳的氧化物,優選錳金屬;所述的錳的氧化物可為下式之一:①MnO②MnO2③Mn3O4;所述的錳的氧化物優選二氧化錳。
製備方法中所用的有機溶劑中需含有醚,即以醚為底物的有機溶劑,可為下式之一或者下式任意組合的混合物,或者為下式之一與不與格氏試劑反應的烷烴或芳烴的任意組合的混合物:①乙醚②四氫呋喃③異丙醚④叔丁基甲醚⑤二氧六環等等。
所用的以醚為底物的有機溶劑優選四氫呋喃。
前面所述的有機溶劑還可以是醚和不與格氏試劑反應的烷烴組合成的混合物,不與格氏試劑反應的烷烴可為下式之一:①戊烷②己烷③甲基環己烷④庚烷⑤石油醚等等。如以叔丁基甲醚和二氧六環組成的混合物為溶劑。
前面所述的有機溶劑還可以是醚和不與格氏試劑反應的芳烴組合成的混合物,不與格氏試劑反應的芳烴可為下式之一:①苯②甲苯③二甲苯。如以四氫呋喃與甲苯組成的混合物為溶劑。
縮合反應完全後所用的稀酸溶液可為下式之一:①稀HCl②稀H2SO4③HBr④NH4CL;其中優選稀HCl。
製備方法中的較優選條件為:所用有機溶劑的最合適的重量為2-鹵代苯腈的2~25倍;所述的錳或錳的氧化物與2-鹵代苯腈摩爾比優選為0.02~0.2:1;所述的含磷的鹵化物與2-鹵代苯腈摩爾比優選為0.006~0.2:1;所述的格氏試劑與2-鹵代苯腈摩爾比為1.2~2:1。
反應中所述的絡合溫度優選30~70℃;縮合溫度優選-20~10℃。
所述的催化劑優選金屬錳及三氯化磷。
所述的製備2-腈基聯苯衍生物式(I)的方法更優選按如下步驟進行:
a.將活性金屬錳、PCl3和2-鹵代苯腈加入到以四氫呋喃為底物的溶劑中;
b.待活性金屬錳、PCl3和2-鹵代苯腈在35~45℃下絡合完全後,將格氏試劑慢慢加入其中,在-10~0℃下縮合反應;
c.縮合反應完全後,用稀鹽酸溶液水解,保持0.5~1小時,分去水層,提取液經蒸餾、重結晶等步驟分離即得純品產物。
所述的2-腈基聯苯衍生物式(I)中的R1為甲基即為4‘-甲基-2-腈基聯苯,該化合物是沙坦類藥物的關鍵中間體,其較優選的製備方法按如下步驟進行:
a.將活性金屬錳、PCl3和2-鹵代苯腈加入到四氫呋喃溶劑中;
b.待活性金屬錳、PCl3和2-鹵代苯腈在35~45℃保溫,絡合完全後,將對甲苯基氯化鎂慢慢加入其中,在0~10℃下縮合反應;
c.縮合反應完全後,用稀鹽酸溶液水解,保持0.5~1小時,分去水層,提取液經蒸餾、重結晶等步驟分離即得純品產物。
在反應過程中,可採取惰性氣體對反應液進行隔離保護,防止吸水、吸氧、吸收CO2等。
改善效果
該發明所述的製備2-腈基聯苯衍生物的方法的有益效果主要表現在:
1.用無機物質替代了有機物質TMSiCl,其催化效果保持不變,具有原料易購、環保、經濟的特點;
2.催化劑錳或錳的氧化物有較少的吸濕性,其純度高、質量好、產量大,價廉、經濟、易購;
3.反應在醚類環境下進行,污染物少、催化效率高,有較好的收率和選擇性。
4.生產成本降低,該發明使用MnO2和三氯化磷作催化劑生產4‘-甲基-2-腈基聯苯比用MnO2和TMSiCl作催化劑節約成本近十倍。
權利要求
1.一種製備2-腈基聯苯衍生物的方法,該系列化合物結構如式(I)所示:
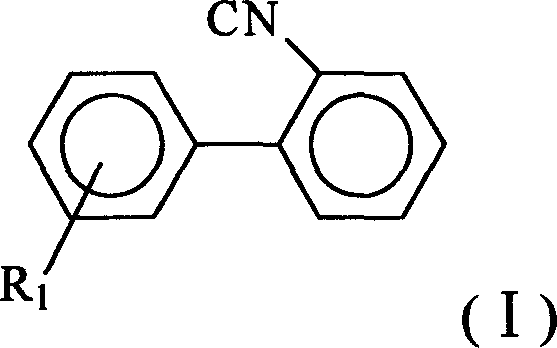
它由格氏試劑(II)與2-鹵代苯腈(III)縮合而成,

X=Cl、BrR2=Cl、Br
其中結構式(I)、結構式(II)中R1為含有1~6個碳原子的烷基、或含有1~6個碳原子烷氧基、或氫;結構式(III)中R2為Br或Cl;其特徵在於所述的製備方法是將催化劑錳或錳的氧化物及含磷的鹵化物和反應物2-鹵代苯腈(III)加入以醚為底物的有機溶劑中,和反應物格氏試劑(II)反應,生成2-腈基聯苯衍生物(I)。
2.如權利要求1所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的製備方法按如下步驟進行:
a.將催化劑錳或錳的氧化物、含磷的鹵化物和2-鹵代苯腈加入到以醚為底物的有機溶劑中,所述的錳或錳的氧化物與2-鹵代苯腈摩爾比為0.01~0.3:1,所述的含磷的鹵化物與2-鹵代苯腈摩爾比為0.003~0.3:1,所述的有機溶劑重量為2-鹵代苯腈的1~25倍;
b.待錳或錳的氧化物、含磷的鹵化物與2-鹵代苯腈在0~100℃下絡合完全後,將格氏試劑慢慢加入其中,在-50~70℃下縮合反應2~24小時,所述的格氏試劑與2-鹵代苯腈摩爾比為1~3:1;
c.縮合反應完全後,用稀酸溶液水解,分去水層,提取液經濃縮、重結晶步驟分離即得純品產物。
3.如權利要求1或2所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的含磷的鹵化物為下式之一:①PCl3,②PCl5,③POCl3,④PBr3,⑤PBr5,⑥POBr3。
4.如權利要求3所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的含磷的鹵化物優選含磷的氯化物。
5.如權利要求1或2所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的錳的氧化物為下式之一:①MnO②MnO2③Mn3O4。
6.如權利要求5所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的錳的氧化物優選二氧化錳。
7.如權利要求1或2所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的以醚為底物的有機溶劑為下式之一或者下式任意組合的混合物,或者為下式之一與不與格氏試劑反應的烷烴或芳烴的任意組合的混合物:①乙醚,②四氫呋喃,③異丙醚,④叔丁基甲醚,⑤二氧六環。
8.如權利要求7所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的以醚為底物的有機溶劑為四氫呋喃。
9.如權利要求7所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的不與格氏試劑反應的烷烴為下式之一:①戊烷,②己烷,③甲基環己烷,④庚烷,⑤石油醚。
10.如權利要求7所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的不與格氏試劑反應的芳烴類為下式之一:①苯②甲苯③二甲苯。
11.如權利要求1-3之一所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的稀酸溶液為下式之一:①稀HCl②稀H2SO4③HBr④NH4CL。
12.如權利要求1或2之一所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的結構式(I)、結構式(II)中R1可為直鏈烷基。
13.如權利要求1或2之一所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的結構式(I)、結構式(II)中R1可為支鏈烷基。
14.如權利要求2所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的有機溶劑重量為2-鹵代苯腈的2~25倍;,所述的錳或錳的氧化物與2-鹵代苯腈摩爾比為0.02~0.2:1;所述的含磷的鹵化物與2-鹵代苯腈摩爾比為0.006~0.2:1;所述的格氏試劑與2-鹵代苯腈摩爾比為1.2~2:1。
15.如權利要求2所述的製備2-腈基聯苯衍生物的方法,其特徵在於絡合溫度為30~70℃。
16.如權利要求2所述的製備2-腈基聯苯衍生物的方法,其特徵在於縮合溫度為-20~10℃。
17.如權利要求2所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的催化劑優選金屬錳及三氯化磷。
18.如權利要求2所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的方法按如下步驟進行:
a.將活性金屬錳、PCl3和2-鹵代苯腈加入到以四氫呋喃為底物的溶劑中;
b.待活性金屬錳、PCl3和2-鹵代苯腈在35~45℃下絡合完全後,將格氏試劑慢慢加入其中,在-10~0℃下縮合反應;
c.縮合反應完全後,用稀鹽酸溶液水解,保持0.5~1小時,分去水層,提取液經濃縮、重結晶等步驟分離即得純品產物。
19.如權利要求18所述的製備2-腈基聯苯衍生物的方法,其特徵在於所述的2-腈基聯苯衍生物式(I)中的R1為甲基即生成物為4-甲基-2-腈基聯苯的製備方法按如下步驟進行:
a.將活性金屬錳、PCl3和2-鹵代苯腈加入到四氫呋喃溶劑中;
b.待活性金屬錳、PCl3和2-鹵代苯腈在35~45℃保溫,絡合完全後,將對甲苯基氯化鎂慢慢加入其中,在-10~0℃下縮合反應;
c.縮合反應完全後,用稀鹽酸溶液水解,保持0.5~1小時,分去水層,提取液經蒸餾、重結晶等步驟分離即得純品產物。
實施方式
實例1
向1500升反應釜中投入金屬錳粉5.4千克和900升的四氫呋喃,同時開啟攪拌,滴加9千克的三氯化磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到40℃,在35~45℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時,反應完畢,將反應液冷卻至0~5℃,待用。
將1200千克含對甲苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品200千克,收率為94.8%,經高效液相色普分析(HPLC)含量為78.5%。
該粗品再經1500升正己烷和5千克活性炭重結晶等純化操作得4′-甲基-2-腈基聯苯純品140千克,總收率為66.4%,純度為99.7%。
①產品外觀呈類白色針狀結晶,熔點為50.5~51.3℃;
②′H-NMR(DMSO-d6)&(ppm)7.95(d,1H,J=8Hz),7.78(t,1H,J=8Hz),7.69~7.32(m,6H),2.39(S,3H)。
實例2
向1500升反應釜中投入二氧化錳9.3千克(0.09818千摩爾)和900升四氫呋喃,同時開啟攪拌,滴加三氯化磷18千克(0.1309千摩爾),滴加完畢,繼續攪拌0.5小時後,加熱升溫至40℃,在35~45℃之間保溫反應2.5小時。向該反應釜中投入鄰氯苯腈150千克(1.091千摩爾),繼續攪拌,保持回流反應4小時,反應完畢,將反應液冷卻至0~5℃待用。
將1000千克含對甲苯基溴化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加格氏液,控制料溫在0~10℃左右。滴加完畢,繼續保溫攪拌2小時。
反應結束後,向反應液中加入500升10%的稀硫酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品約205千克,收率為97.1%,經分析含量為73.2%(HPLC)。
該粗品再經活性炭處理、重結晶等純化處理,得純度為99.6%的4′-甲基-2-腈基聯苯純品135千克,總收率為64%。
實例3
向1500升反應釜中投入一氧化錳7.0千克和1000升的異丙醚,同時開啟攪拌,慢慢加入8.2千克的五氯化磷。加入完畢,繼續攪拌0.5小時後,加熱升溫到50℃,在45~55℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時,反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含對甲苯基氯化鎂25.0%的異丙醚溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-30~-20℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀硫酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品190千克,收率為90.0%,經分析含量為70.0%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得4′-甲基-2-腈基聯苯純品120千克,總收率為56.9%,純度為99.5%。
實例4
向1500升反應釜中投入二氧化錳9.0千克、600升的叔丁基甲醚和900升二氧六環,同時開啟攪拌,滴加20.1千克的三氯氧磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到50℃,在50~55℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含鄰甲苯基氯化鎂25.0%的叔丁基甲醚溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在0~10℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集2′-甲基-2-腈基聯苯粗品195千克,收率為92.4%,經分析含量為71.3%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得2′-甲基-2-腈基聯苯純品128千克,總收率為60.7%,純度為99.6%。
實例5
向1500升反應釜中投入四氧化三錳7.5千克和1200升的異丙醚,同時開啟攪拌,滴加13.4千克的三氯化磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到40℃,在35~45℃之間保溫反應2.5小時,向該反應釜中投入鄰溴苯腈200千克,繼續攪拌,保持回流反應4小時,反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含鄰甲苯基溴化鎂32.4%的異丙醚溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀氫溴酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集2′-甲基-2-腈基聯苯粗品200千克,收率為94.8%,經分析含量為73.2%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得2′-甲基-2-腈基聯苯純品140千克,總收率為66.4%,純度為99.7%。
實例6
向1500升反應釜中投入一氧化錳7.0千克、700升四氫呋喃和800升正己烷,同時開啟攪拌,滴加18.8千克的三溴氧磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到40℃,在35~45℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含對甲苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品202千克,收率為95.7%,經分析含量為73.1%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得4′-甲基-2-腈基聯苯純品141千克,總收率為66.8%,純度為99.7%。
實例7
向1500升反應釜中投入四氧化三錳7.5千克、400升二氧六環和600升苯,同時開啟攪拌,滴加13.4千克的氧氯化磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到50℃,在50~60℃之間保溫反應2.5小時,向該反應釜中投入鄰溴苯腈200千克,繼續攪拌,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含對甲苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在0~10℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品198千克,收率為93.8%,經分析含量為70.7%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得4′-甲基-2-腈基聯苯純品130千克,總收率為61.6%,純度為99.5%。
實例8
向1500升反應釜中投入金屬錳粉5.4千克和1000升的四氫呋喃和1000升甲苯,同時開啟攪拌,滴加18.8千克的三溴氧磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到50℃,在50~60℃之間保溫反應2.5小時,向該反應釜中投入鄰溴苯腈200千克,繼續攪拌,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含間甲氧基苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀氯化氨溶液水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集3′-甲氧基-2-腈基聯苯粗品205千克,收率為97.2%,經分析含量75.5%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得3′-甲氧基-2-腈基聯苯純品145千克,總收率為68.7%,純度為99.7%。
實例9
向1500升反應釜中投入單質錳5.4千克和900升的四氫呋喃,同時開啟攪拌,滴加18.8千克的三溴氧磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到40℃,在35~45℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含對甲苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品204千克,收率為96.7%,經分析含量為75.4%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得4′-甲基-2-腈基聯苯純品143千克,總收率為67.8%,純度為99.7%。
實例10
向1500升反應釜中投入二氧化錳9.3千克和900升的四氫呋喃,同時開啟攪拌,滴加20.1千克的三氯氧磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到40℃,在35~45℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時,反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含對甲苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品200千克,收率為94.8%,經分析含量為72.2%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得4′-甲基-2-腈基聯苯純品136千克,總收率為64.5%,純度為99.6%。
實例11
向1500升反應釜中投入單質錳0.6千克和900升的四氫呋喃,同時開啟攪拌,滴加2.1千克的三溴氧磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到30℃,在25~35℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含對甲苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品170千克,收率為80.6%,經分析含量為65.4%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得4′-甲基-2-腈基聯苯純品105千克,總收率為49.8%,純度為99.2%。
實例12
向1500升反應釜中投入二氧化錳20.6千克和900升的四氫呋喃,同時開啟攪拌,滴加78.8千克的三溴化磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到30℃,在25~35℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含對甲苯基氯化鎂25.0%的四氫呋喃溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集4′-甲基-2-腈基聯苯粗品204千克,收率為96.7%,經分析量為75.4%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得4′-甲基-2-腈基聯苯純品143千克,總收率為67.8%,純度為99.5%。
實例13
向1500升反應釜中投入一氧化錳7.0千克和1000升的異丙醚,同時開啟攪拌,慢慢加入8.2千克的五氯化磷。加入完畢,繼續攪拌0.5小時後,加熱升溫到50℃,在45~55℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,,保持回流反應4小時,反應完畢,將反應液冷卻至0~5℃,待用。
將800千克含苯基氯化鎂22.3%的異丙醚溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-30~-20℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀硫酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集2-腈基聯苯粗品190千克,收率為90.0%,經分析含量為70.0%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得2-腈基聯苯純品120千克,總收率為56.9%,純度為99.5%。
實例14
向1500升反應釜中投入二氧化錳9.0千克、600升的叔丁基甲醚和900升二氧六環,同時開啟攪拌,滴加20.1千克的三氯氧磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到50℃,在50~55℃之間保溫反應2.5小時,向該反應釜中投入鄰氯苯腈150千克,繼續攪拌,保持回流反應4小時。反應完畢,將反應液冷卻至0~5℃,待用。
將1000千克含鄰乙苯基氯化鎂36.0%的叔丁基甲醚溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在0~10℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀鹽酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集2′-乙基-2-腈基聯苯粗品195千克,收率為92.4%,經分析含量為71.3%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得2′-乙基-2-腈基聯苯純品128千克,總收率為60.7%,純度為99.6%。
實例15
向1500升反應釜中投入四氧化三錳7.5千克和1200升的異丙醚,同時開啟攪拌,滴加13.4千克的三氯化磷。滴加完畢,繼續攪拌0.5小時後,加熱升溫到40℃,在35~45℃之間保溫反應2.5小時,向該反應釜中投入鄰溴苯腈200千克,繼續攪拌,保持回流反應4小時,反應完畢,將反應液冷卻至0~5℃,待用。
將2300千克含鄰異丁苯基氯化鎂18.3%的乙醚溶液抽至高位槽,向反應釜中滴加該格氏液,控制料溫在-10~0℃之間。滴加完畢,繼續保溫反應2小時。
反應結束後,向反應液中加入500升10%的稀氫溴酸水解,保持反應0.5小時以上,分去水層,濃縮回收溶劑,蒸餾濃縮液,收集2′-異丁基-2-腈基聯苯粗品200千克,收率為94.8%,經分析含量為73.2%(HPLC)。
該粗品再經活性炭處理、重結晶等純化操作得2′-異丁基-2-腈基聯苯純品135千克,總收率為62.4%,純度為99.1%。
榮譽表彰
2014年11月6日,《製備2-腈基聯苯衍生物的方法》獲得第十六屆中國專利優秀獎。

