基本介紹
- 中文名:脫氰基
- 類型:化學名詞
簡介,機理研究,還原脫氰基反應操作的標準步驟,
簡介
常見的還原脫氰基反應的底物較多的是α-三級氨基腈化合物,其在化學計量的活化劑的作用下,經歷一個SN1的過程,從而形成一個亞胺鎓中間體,繼而被反應體系中的還原劑(氫負離子)所捕獲,得到氰基脫除的胺類化合物。常用的還原體系有如下幾種:LiAlH4, NaBH4, AgBF4/Zn(BH4)2, BH3等等。這些反應條件在以α-三級氨基腈為底物的還原脫氰基反應中具有很好的普適性。然而對於α-二級氨基腈化合物而言,這些條件往往不適用,或者效率很差。究其原因是因為二級胺體系較難形成亞胺中間體,同時該亞胺中間體相較於亞胺鎓而言反應活性有所降低,從而導致了α-二級氨基腈化合物的還原脫氰基反應仍是一個挑戰。
最近報導了以氰基作為無痕活化基團,通過1,3-偶極環加成反應和還原脫氰基組合,構建多官能化的5-未取代吡咯烷類化合物的新方法,並將之套用於吡咯烷天然產物Isoretronecanol的全合成中。在此研究工作中,我們發現了一個全新的由硼氫化鈉引發的二級胺基腈的還原脫氰基反應,本文將就該反應的機理進行細緻的研究。
機理研究
硼氫化鈉的作用及可能的反應機理
基於上述的一系列的實驗結果,我們已經確認硼烷作為主要還原劑來還原亞胺中間體,而硼氫化鈉也在該反應中起到了至關重要的作用。因催化量的硼氫化鈉的加入不但大大加速了還原脫氰基反應,而且還有利於獲得高的反應收率。通常情況下,硼烷與硼氫化鈉的組合,一般認為硼氫化鈉作為還原劑,而硼烷作為硼氫化鈉的再生氫源,而在上個世紀80年代Brown等人也觀察到類似的加速現象。然而我們新發展的還原脫氰基反應似乎經過一條完全不同的反應歷程。
基於大量的文獻調研和實驗結果,我們提出了如下的反應機理(如圖1所示):首先,化合物1a與硼烷形成N-B絡合物,該絡合物的裂解為亞胺中間體II的速率往往非常慢,但是在鹼性的硼氫化鈉的協助下,通過對絡合物I中酸性較強的N-H進行去質子來促進這一碎裂;同時在BH3CN的輔助下,亞胺會被硼烷迅速還原產生氮負離子III,而新生成的中間體III再次充當鹼,攫取絡合物I中的質子,從而再次產生亞胺硼烷絡合物II和BH3CN。這兩步形成一個循環,作為鏈增長的過程來源源不斷地產生絡合物IV和V。最後,化合物IV和V通過一些後處理方法轉化為裸露的吡咯烷2a。在這一過程中,NaBH4作為一種鹼引發了一個還原型的負離子鏈反應,其中硼烷不僅充當了形成亞胺所需的路易斯酸活化劑,還充當了還原亞胺的還原劑。
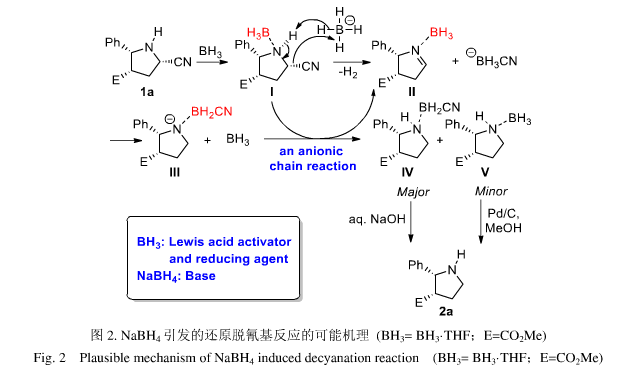
圖1 NaBH4引發的還原脫氰基反應的可能機理
還原脫氰基反應操作的標準步驟
向裝有α-氨基腈1a(0.5 mmol)的THF(5 mL)溶液中,加入BH3·THF硼烷-四氫呋喃溶液。該反應體系在室溫條件下反應10分鐘後,加入NaBH4(3.8mg, 0.1 mmol)。然後攪拌20 min後,加入5ml冰水和3mL20%NaOH水溶液淬滅反應。攪拌10分鐘後,用乙酸乙酯萃取,有機相再加入2mL 20%NaOH水溶液洗滌,水相再用乙酸乙酯萃取,有機相用飽和食鹽水洗滌後,無水硫酸鎂乾燥,過濾,除去溶劑後,溶解於5mL的甲醇中,加入12mgPd/C (10% wet.)。攪拌合適的時間後(10 min),濃縮,柱色譜(CHCl3/MeOH = 200:1 to 100:1)分離即可得到脫氰基產物2a。

