簡介
維生素A是一種極其重要、極易缺乏的,為人體維持正常代謝和機能所必需的
脂溶性維生素,它是由美國科學家Elmer Mc Collum和MArgAret Davis在1912~1914年之間發現的。其實早在1000多年前,中國唐代醫學家
孫思邈(公元581~ 682年)在《千金方》中就記載了用動物肝臟可治療夜盲症,而有關巴西土人以魚肝油治療乾眼病、丹麥人以橄欖油治療乾眼病的文獻也有記載。在MArgAret DAvis等人從鱈魚肝臟中提取出一種黃色黏稠液體——維生素A以前,人們並不了解維生素的存在,因此他首先將其命名為“脂溶性A”(A是德文乾眼病“AugendArre”的第一個字母)。隨著陸續有新的為人體所必需的脂溶性物質被科學家發現,到1920年,“脂溶性A”被英國科學家正式命名為維生素A。
維生素A並不是單一的化合物,而是一系列包括
視黃醇(retinol)、
視黃醛(retinene)、
視黃酸(retinoic Acid)、視黃醇乙酸酯(retinyl AcetAte)和視黃醇棕櫚酸酯(retinyl palmitate)等在內的視黃醇的衍生物,它們的分子結構如圖《維生素A的分子結構》所示。維生素A只存在於動物體中,在魚類特別是魚肝油中含量很多。植物中並不含有維生素A,但許多蔬菜和水果卻都含有
維生素A原——
胡蘿蔔素,它在小腸中可分解為維生素A,其中1分子β-胡蘿蔔素可分解為2分子維生素A,而1分子A-胡蘿蔔素或γ-蘿蔔素只能產生1分子維生素A。
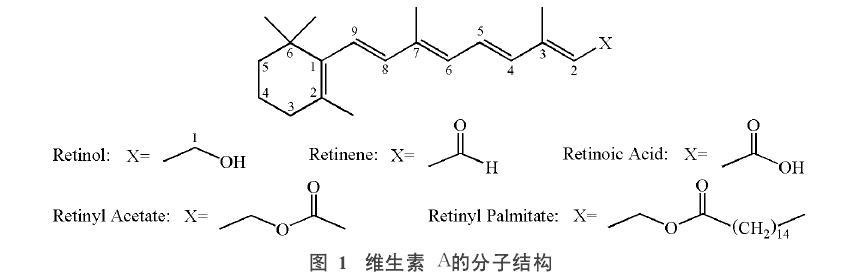
維生素A的分子結構
維生素A呈黃色片狀晶體或結晶性粉末,不溶於水和甘油,能溶於醇、醚、烴和鹵代烴等大多數有機溶劑。它的化學性質相對穩定,但暴露於熱、光或空氣中則會被輕易破壞,通常應避光保存。維生素A的主體——視黃醇的化學名稱為全反式3,7-二甲基-9-(2,6,6-三甲基-1-環己烯基-1)-2,4,6,8-壬四烯-1-醇,其側鏈上有4個
共軛雙鍵,理論上有16個
幾何異構體,由於立體位阻效應,自然界存在的幾何異構體只有無位阻的全反式體、9-順式體、13-順式體、9,13-雙順式體和有位阻的11-順式體,其中以全反式的
生物活性最高。由於維生素A醋酸酯(視黃醇乙酸酯)比維生素A醇(視黃醇)穩定,所以市場上稱為“維生素A”的商品,實際上都是維生素A的醋酸酯,它為淡黃色的油狀液體,冷凍後可固化,幾乎無臭或有微弱魚腥味,但無酸敗味,極易溶於三氯甲烷或酯中,也溶於無水乙醇和植物油,但不溶於丙三醇和水,在空氣中和遇光時不穩定。
結構與理化性質
維生素A是指所有具有視黃醇生物活性的化合物。有兩大類物質可以提供視黃醇生物活性。其一是指視黃醇、其代謝產物以及具有相似結構的合成類似物,這一類也稱為類視黃醇(Retinoids)物質,也稱為預先形成的維生素A,主要膳食來源為動物性食物中含有的視黃醇和視黃醯酯。另一類物質是維生素A原類胡蘿蔔素,是指來自於植物性食物的在體內可以轉化生成視黃醇的類胡蘿蔔素,它們是膳食視黃醇的前體物質,主要包括β-胡蘿蔔素、α-胡蘿蔔素和β一隱黃質。
維生素A是一組由20碳結構構成的、具有一個β-紫羅酮環、一個由四個頭尾相連的類
異戊二烯單元組成的側鏈以及在碳-15位結合了一個羥基(視黃醇)、或者醛基(視黃醛)、或者羧酸基(視黃酸)、或者酯基(視黃酯)的分子集合。類胡蘿蔔素為
聚異戊二烯化合物或
萜類化合物,已經發現自然界中存在600多種形式的類胡蘿蔔素,其中只有部分具有維生素A原營養活性,但是具有膳食維生素A意義的只有β-胡蘿蔔素、α-胡蘿蔔素和β-隱黃質三種。全反式異構體是每一種類胡蘿蔔素最常見的和穩定的形式,但是,也存在許多順式異構體。類胡蘿蔔素通常包含40碳原子,具有廣泛的共軛雙鍵系統,在其共軛碳鏈的末端,具有一個或兩個環狀結構。番茄紅素是一個例外,它沒有環狀結構,也沒有維生素A活性。
維生素A屬於脂溶性維生素,可以不同程度地溶於大部分有機溶劑,但不溶於水。維生素A及其衍生物很容易被氧化和異構化,特別是在暴露於光線(尤其是紫外線)、氧氣、性質活潑的金屬以及高溫環境時,可加快這種氧化破壞。但一般烹調過程不至於對食物中的維生素A造成太多破壞。在理想條件下,如低溫冷凍等,血清、組織或結晶態的類視黃醇可保持長期穩定。在無氧條件下,視黃醛對鹼比較穩定,但在酸中不穩定,可發生脫氫或雙鍵的重新排列。油脂在酸敗過程中,其所含的維生素A和胡蘿蔔素會受到嚴重的破壞。食物中的磷脂、維生素E或其他
抗氧化劑有提高維生素A穩定性的作用。在維生素A的衍生物中,視黃酸和視黃醯酯的穩定性最好。
視黃醇和其他類視黃醇都具有連續共軛雙鍵,它們都能產生特有的紫外光或可見光吸收光譜。在乙醇中的最大吸收波長為全反式視黃醇325nm,全反式視黃醛381nm,全反式視黃酸350nm。視黃醇在325nm波長紫外光照射下,可以產生470nm螢光。目前最常見的類視黃醇檢測方法,就是利用其上述特性,採用
反相高效液相色譜,配合紫外光/
螢光檢測器來完成。維生素A在體內主要儲存於肝臟中,約占總量的90%-95%,少量存在於脂肪組織。
β-胡蘿蔔素是類胡蘿蔔素中最為突出的一個成分,原因在於它是最早被認識的類胡蘿蔔素組分;它幾乎是人體內含量高的類胡蘿蔔素組分;它在我們食物中分布最廣、含量最豐富,特別是在蔬菜、水果中最突出,幾乎所有的蔬菜、水果,或多或少都有其蹤跡;此外,它也是類
胡蘿蔔素組分中維生素A原活性最強的。
β-胡蘿蔔素分子式為C40H56,分子量為536.87,其分子結構中具有許多共軛雙鍵,這些雙鍵即可吸收可見光中的某些光譜,使其呈現特殊顏色,同時又使其具有極強的淬滅活性氧自由基的能力,可減輕機體抗氧化損傷,從而發揮疾病預防作用。β-胡蘿蔔素分子實際上就是兩個尾部相連的視黃醇分子,通過中心裂解或偏心裂解,可轉變成兩個或一個維生素A。β一胡蘿蔔素又分為全反式和順式異構體。全反式β-胡蘿蔔素經過中心裂解,可以生成兩分子全反式視黃醇(維生素A),順式β-胡蘿蔔素轉換為維生素A的產量則較低。
α-胡蘿蔔素與β-胡蘿蔔素分子結構相似,為同分異構體,差別在於一端的
β-紫羅酮環中5’,6’雙鍵發生變化,而此β-紫羅酮環是維生素A活性所必需的結構。因此,α-胡蘿蔔素轉變為維生素A的產量只有β-胡蘿蔔素的一半。除維生素A活性外。α-胡蘿蔔素的性質和功效與β-胡蘿蔔素相似。
β穩黃質,也被稱為β-隱黃素、β-胡蘿蔔素-3-醇,是一種含氧的葉黃素類的類胡蘿蔔素,其分子式為C40H56O,分子量為552.87。與β-胡蘿蔔素相比,β-隱黃質分子結構是在3位由一個輕基取代原來的一個氫原子,其分子比β-胡蘿蔔素多一個氧原子,由此造成β一紫羅酮環結構變化,使這一半分子失去維生素A活性可能,故β隱黃質和α-胡蘿蔔素一樣,轉變為維生素A的產量只有β-胡蘿蔔素的一半。除了維生素A活性外,β隱黃質也同樣具有較強的抗氧化活性。
膳食中的類胡蘿蔔素相對比較穩定,烹調過程中破壞較少,並且食物的加工和熱處理有助於提高
植物細胞內胡蘿蔔素的釋出,提高其吸收率。但長時間的高溫,特別是在有氧和紫外線照射的條件下,損失會明顯的增加。我國的炒菜方法,胡蘿蔔素的保存率為70%一90%。
維生素A的合成
雖然維生素A可從動物組織中提取,但資源相對分散,步驟繁雜,成本較高,因此商品維生素A都是化學合成產品。國內外維生素A的工業合成,主要有瑞士Roche和德國BASF兩條合成工藝路線。前者以
β-紫羅蘭酮為起始原料,格氏反應為特徵,經DArzens反應、格氏反應、選擇加氫、羥基溴化和脫溴化氫,完成
維生素A醋酸酯的合成;後者的典型特徵則是Wittng反應,其合成路線如圖《BASF法合成維生素A》所示,它是以β-紫羅蘭酮為起始原料和乙炔進行格氏反應生成乙炔-β-紫羅蘭醇,選擇加氫得到乙烯-β-紫羅蘭醇,再經Wittng反應之後,以醇鈉為催化劑,與C5醛縮合生成維生素A醋酸酯。
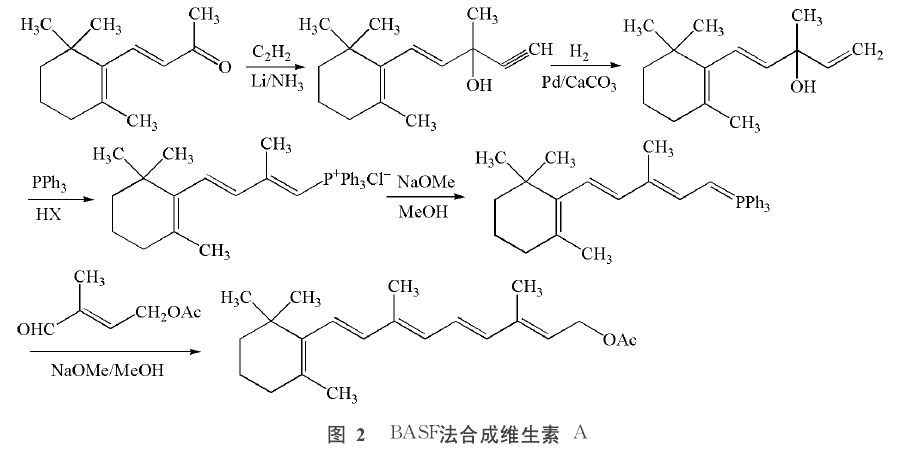
BASF法合成維生素A
維生素A的測定
常見的檢測維生素A的方法主要有
比色法、
紫外分光光度法、
近紅外光譜法和
高效液相色譜法。比色法測定維生素A的原理是基於維生素A能和各種酸反應,生成藍紫色到桃紅色的有色化合物,其中維生素A與
三氯化銻-
三氯甲烷溶液(或三氟醋酸-三氯甲烷溶液)生成的藍色化合物在620nm波長處有特徵吸收,是套用較早的一種靈敏的方法。隨著紫外分光光度法和高效液相色譜法等的發展,該方法已很少用於定量檢測,僅用於定性檢測。紫外分光光度法的原理是根據維生素A在325或328nm波長處有最大吸收而進行定量檢測的。
近紅外光譜法則基於維生素A在1721和1872nm波長處有兩個較穩定的特徵吸收峰。高效液相色譜法通常是基於維生素A在紫外區的特徵吸收以及維生素A的天然螢光特性。
生理功能
維生素A在人體具有廣泛而重要的生理功能,概括起來主要包括視覺、細胞增殖分化調節、細胞間信息交流和免疫應答這幾個方面,其缺乏會導致的生理功能異常和病理變化。
視覺功能
維生素A經典的或最早被認識的功能是在視覺細胞內參與維持暗視感光物質循環。視網膜上的桿狀細胞含有的
視紫紅質,是由11-順式視黃醛與視蛋白結合而成,其對暗光敏感。視紫紅質感光後,11-順式視黃醛轉變為全反式視黃醛並與視蛋白分離,產生視覺電信號。解離後的全反式視黃醛在桿狀細胞內被還原為全反式視黃醇,被轉運到視網膜色素上皮細胞,與來自血漿的全反式視黃醇一起,開始複雜的異構化過程,參與重新合成視紫紅質所需的11-順式視黃醛的供應,維持暗光適應。因此要維持良好的暗光視覺,就需要源源不斷地向桿狀細胞供給充足的11-順式視黃醛。
維生素A缺乏時,11-順式視黃醛供給減少,暗適應時間延長。
維持皮膚黏膜完整性
維生素A是調節糖蛋白合成的一種輔酶,對
上皮細胞的細胞膜起穩定作用,維持上皮細胞的形態完整和功能健全。維生素A的這種對組織功能與完整性的作用,是通過介導臨近細胞間的信息交流而實現的。維生素A缺乏會造成上皮組織乾燥,正常的柱狀上皮細胞轉變為角狀的覆層
鱗狀細胞,導致細胞角化。全身各種組織的上皮細胞都會受到影響,但受累最早的是眼睛結膜、角膜和淚腺上皮細胞,淚腺分泌減少導致乾眼症,結膜或角膜乾燥、軟化甚至穿孔。皮膚毛囊、皮脂腺、汗腺、舌味蕾、呼吸道和腸道薪膜、泌尿和生殖薪膜等上皮細胞均會受到影響,從而產生相應臨床表現和黏膜屏障功能受損。
細胞核激素樣作用
維生素A通過細胞核內類視黃酸受體,調節和控制細胞核內
信使RNA的激活與表達。細胞核記憶體在類視黃醇受體,包括三種視黃酸受體RARα,β和γ以及三種其9順式異構體類視黃醇x受體RxRα,β和γ。RARs可以結合併對視黃酸及異構體產生反應,而RXRs則特異性地結合視黃酸異構體(9-順式視黃酸)。這些核受體通過兩兩聚合,形成各種同二聚體或異二聚體,與相應的視黃酸反應原件RARE或RXRE結合,從而調控靶細胞基因的相應區域。類視黃醇受體的最重要功能是調控細胞分裂和分化。包括RXR在內的信息物質降低
細胞增殖並促進
細胞程式化死亡(凋亡)。對於
細胞分化,細胞內類視黃醇的調控功能主要通過RAR影響細胞周期蛋白而發揮作用。這種調控結果可影響到機體的各個方面,包括生長發育、生殖功能、免疫功能、造血功能等。
維持和促進免疫功能
類視黃醇對維護免疫功能是必需的,後者依賴於免疫刺激引發的細胞分化和增殖。類視黃酸通過核受體對靶基因的調控,可以提高細胞免疫功能,促進
免疫細胞產生抗體,以及促進
T淋巴細胞產生某些
淋巴因子。視黃酸對維持循環血液中足量水平的
自然殺傷細胞極為重要,後者具有抗病毒、抗腫瘤活性。已經證明視黃酸可提高鼠類
巨噬細胞的吞噬活性,增加白介素1和其他
細胞因子的生成,後者是炎症反應的介導因子和T、
B淋巴細胞生產的激活因子。此外,B淋巴細胞的生長、分化和激活也需要視黃醇。維生素A缺乏時,免疫細胞內視黃酸受體表達相應下降,影響機體免疫功能。維生素A缺乏和邊緣缺乏的兒童,感染性疾病發病風險和死亡率升高。
促進生長發育和維持生殖功能
生殖組織和哺乳動物的
胚胎髮生依賴RAR進行基因調節,通過相關方式,維生素A對這些組織具有極其重要的作用。這些作用也是通過對細胞增殖、分化的調控實現的,尤其是參與軟骨內成骨。維生素A缺乏時,長骨形成和牙齒髮育均受障礙;男性睪丸萎縮,精子數量減少、活力下降。
與維生素D活性的對抗及對骨骼代謝的影響
目前的許多研究結果顯示,維生素A與骨質代謝存在密切的關係。維生素A缺乏可使
破骨細胞數目減少,
成骨細胞的功能失控,導致骨膜骨質過度增生,骨腔變小。維生素A過量對骨礦物化和結構完整性的不良影響,更成為近來關注的問題。過量維生素A可刺激骨的重吸收,並抑制骨的再形成。這種影響可能與慢性維生素A中毒時的
高鈣血症有著共同的機制。考慮到維生素A和
維生素D都廣泛參與許多細胞的核受體調節,維生素A缺乏和過量對骨質代謝的影響,可能與其對維生素D活性的對抗有關。
抗細胞增殖作用
除影響正常健康相關進化功能外,維生素A還有糾正多種病理狀態的調節作用。維生素A及其異構體能夠促進終末分化、抑制增殖、促進凋亡,該作用對組織惡變過程中的腫瘤發揮作用。體外多種癌細胞系研究發現,大劑量類視黃醇具有抗癌能力。
促進血紅蛋白生成,增加食物中鐵的攝取
早期的研究發現,維生素A干預實驗可增加多種營養素缺乏性貧血人群的
血紅蛋白和血細胞計數。維生素A和維生素A原,可能通過阻斷植酸的干擾而改善鐵吸收。研究發現,維生素A營養狀況對血液系統的影響,不僅僅是膳食維生素A促進鐵吸收的直接作用,還存在對鐵營養狀況的某種調控作用,包括刺激造血母細胞、促進抗感染、動員鐵進入紅細胞系。從胚胎初期卵黃囊階段,到子宮內胎兒肝生成期,再到骨髓生成期,都有相關文獻證明類視黃醇調控造血作用的存在。維生素A狀況不僅對骨髓造血細胞系增殖產生影響,而且對血小板生成和
血栓形成也具有影響。
套用及副作用
維生素A主要用於防治夜盲症、乾眼病,也用於燒傷後皮膚的局部
化膿性感染。人體攝取的維生素A成人不能超過3mg/天,兒童不能超過2mg/天。若服用大劑量維生素A,因為排出比不高而會發生急性
維生素A過多症,主要症狀為短期腦積水與嘔吐,部分可有頭痛、嗜睡與噁心等症狀[9]。幼兒長期服用大劑量維生素A後,會發生維生素A過多症狀,主要是
肝脾腫大、紅細胞和白細胞均減少、骨髓生長過速以及長骨變脆,易發生骨折等。瑞典一項最新研究表明,血液中含有高濃度維生素A的中年男性在他們老年時期發生骨折的機率要比那些血液中維生素A含量低的人群高得多。因此,對人體而言,維生素A不可或缺,也不可濫用,只要保證飲食含有豐富的維生素A或胡蘿蔔素的食物,即可有效地預防維生素A缺乏,而無須額外服用維生素A補充劑。
過量的危害
維生素A的毒副作用主要取決於視黃醇及視黃醯酯的攝入量,並與機體的生理及營養狀況有關。肝臟維生素A濃度超過300mg/g被認為是過量,並會引起相應臨床毒性表現。急性維生素A過量的臨床表現包括嚴重皮疹、頭痛、假性腦瘤性昏迷而導致快速死亡。慢性過量相對更為常見,臨床表現包括中樞神經系統紊亂性症狀、
肝臟纖維化、腹水和皮膚損傷。最近有報導嬰兒維生素A過量導致的骨髓抑制、成人慢性維生素A過量導致的高血鈣症。研究發現,油基維生素A或肝臟來源維生素A的毒性只有水合的、乳化的和固體視黃醇補充劑毒性的1/10。
致畸作用
研究證實,13-順-視黃酸具有致畸作用,因而擔心人類大劑量補充維生素A可能會有致畸作用。大量動物實驗證實,過量維生素A可致胚胎畸形。流行病學資料顯示,過量攝入預先形成的維生素A可導致
出生缺陷。最敏感的時期為胚胎生成期(孕早期),維生素A過量引起的出生缺陷主要發生於由腦神經靖演變的器官,如顱面畸形、
中樞神經系統畸形(不包括神經管畸形)、甲狀腺和心臟畸形等。估計長期每日攝入預先形成的維生素A超過1萬IU就可致畸。口服視黃醇類似物治療皮膚病可能出現這些出生缺陷。妊娠早期局部使用維生素A類似物,導致生長畸形的風險很小、甚至沒有風險。
骨礦物質丟失和骨質疏鬆症風險
動物實驗發現,長期維生素A過量可導致骨礦物質丟失,推測在人類也可能會有類似的影響。1998年報導的在瑞典婦女中進行的橫斷面調查和
病例對照研究結果顯示,在每日攝入量不超過1.5mg的情況下,骨礦物質密度隨維生素A攝入量的增加而提高;但每日攝入量大於1.5mg時,增加維生素A攝入量可提高
骨質疏鬆和髓骨骨折的風險。
由於流行病學研究受到各種因素限制,所獲結論既有支持又有反對維生素A過量影響骨健康的證據,目前對此給予了高度關注,但尚未形成明確結論。尤其是目前尚遠不能確證將預先形成的維生素A攝入量作為骨健康的危險因素,尚不能建立確定對骨骼健康產生明顯影響的視黃醇攝入量界定值,但可以肯定的是過量維生素A攝入對骨骼健康應該沒什麼好處。
肝臟損傷
動物實驗和人體實驗資料證實,維生素A過量與
肝功能異常之間存在非常明確的因果關係,這是因為肝臟是維生素A的主要儲存器官,也是維生素A毒性的主要靶器官。維生素A過量引起的肝臟異常包括可逆性的肝臟酶活性升高、肝臟纖維化、肝硬化和死亡。
增加心血管疾病風險
對
心血管疾病的
觀察性研究發現,維生素A過量可能會增加心血管疾病風險。在美國成人的
佇列研究中,高血清視黃醇水平與高心血管疾病風險有關,但僅限於男性。目前的研究資料顯示,β-胡蘿蔔素等類胡蘿蔔素的毒性很低。與維生素A不同,目前尚沒有類胡蘿蔔素缺乏或毒性的報導。過多攝入β-胡蘿蔔素可導致胡蘿蔔素血症,出現暫時性皮膚黃染。有報導,受試者長期攝入大量胡蘿蔔等食物或每日補充30mg或更多的β一胡蘿蔔素時,即可發生胡蘿蔔素血症。減少這樣的類胡蘿蔔素攝入後數天或數周,這些症狀即可逆轉。
缺乏的危害
維生素A缺乏具有臨床和機能性表征。對於原發性維生素A缺乏,每個人的耐受性不同,這取決於一系列的地理和流行病學的因素。
維生素A缺乏症的臨床表現主要是眼部和視覺以及其它上皮功能異常的症狀和體徵。
眼部和視覺表現
乾眼症是維生素A缺乏的典型臨床特徵之一。根據特異的眼部表現,可以將乾眼症分為若干期。XN期是最早階段,主要出現暗適應功能損傷導致的夜盲症。之後為X1A期,
杯狀細胞分泌粘液減少,造成的結膜乾燥;接下來為X1B期,在結膜額側表面出現泡末狀畢脫氏斑。X2期為疾病進展期,表現為單純的角膜乾燥。當角膜出現軟化或潰瘍,或兩者兼有的液化過程,則為X3期。此時,如液化表面不足角膜面積的1/3為X3A期,大於1/3為X3B期。角膜軟化導致的眼球損傷稱為乾眼病眼底病,也稱為XF期。
其它上皮功能異常的表現
毛囊增厚(
毛囊角質化)是維生素A缺乏的皮膚表征。黏膜內粘蛋白生成減少,黏膜形態、結構和功能異常,可導致疼痛和黏膜屏障功能下降,可累及咽喉、扁桃體、支氣管、肺臟和消化道黏膜。維生素A缺乏和邊緣缺乏導致兒童感染性疾病風險和死亡率升高。
胚胎生長和發育異常
維生素A缺乏會損傷胚胎生長。嚴重缺乏維生素A的實驗動物多發生胚胎吸收,而存活下來的胚胎也會出現眼睛、肺、泌尿道和心血管系統畸形。人體缺乏維生素A時較少出現形態異常,但可見肺臟的功能異常。
免疫功能受損
維生素A缺乏可導致血液
淋巴細胞數、自然殺傷細胞減少和特異性抗體反應減弱。維生素A攝入不足時,可觀察到白細胞數下降,淋巴器官重量減輕,T細胞功能受損和對免疫原性腫瘤抵抗力降低。在實驗動物以及人體實驗中,維生素A缺乏多導致體液和細胞免疫功能異常。
感染性疾病的患病率和死亡率升高
維生素A缺乏可導致實驗動物和人類感染性疾病發病率和死亡率增加,尤其是在開發中國家。患有輕度到中度維生素A缺乏症的兒童
呼吸道感染和腹瀉風險升高;患輕度乾眼症兒童的死亡率是無乾眼症兒童的四倍。給患麻疹的住院患兒補充大劑量維生素A,能明顯降低兒童不病死率,減輕併發症的嚴重程度。研究顯示,補充維生素A可降低幼兒腹瀉和瘧疾的嚴重程度。
缺乏的預防與治療
維生素A缺乏是引起開發中國家兒童失明的主要原因,也是開發中國家兒童常見的
營養缺乏症。由於VAD(維生素A缺乏症)和SVAD(維生素A邊緣性缺乏)對兒童健康的影響,使得預防和控制VAD和SVAD已經成為世界範圍內亟待解決的公共衛生問題之一。
WHO和
聯合國兒童基金會以多種方式進行維生素A的干預,包括增加含維生素A食物的消費、食物強化維生素A、提高母乳餵養、定期大劑量維生素A補充等。
維生素A營養狀況評估
準確地評價易感個體和人群的維生素A營養水平對於研究VAD、SVAD以及營養干預策略的制訂、實施和評估有著極為重要的意義。在實際工作中檢查群體或個體維生素A營養狀況常用的方法主要包括:乾眼病的臨床檢查、膳食調查、暗適應能力的測定、夜盲史的詢問、血清視黃醇含量的測定、相對劑量反應試驗、
同位素稀釋法、肝臟維生素A含量的測定及結膜印跡細胞法等。
營養教育及合理配膳措施
通過營養教育、合理配膳,提高對本地區現存富含維生素A食物攝入的膳食干預方法,長期以來被認為是最為持久的、能從根本上改善VAD和SVAD狀況的方法。營養教育應側重於提倡母乳餵養,增加乳類、蛋類及深色蔬菜等的供給。

均衡營養
食物強化維生素A
食物強化維生素A是防治VAD和SVAD的一種直接、有效、低廉的方法。中國國家公眾營養項目組的食物強化總體構想中確定了維生素A、維生素Bl、
維生素B2、葉酸、尼可酸、鐵、碘、鋅和鈣為我國營養強化的主要營養素。
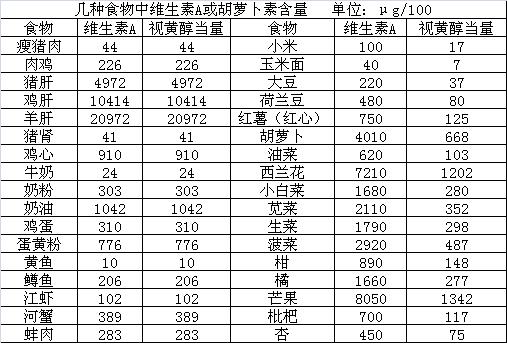
食物中維生素A和視黃醇當量含量
定期補充維生素A製劑
定期補充維生素A製劑是一種快速、直接改善維生素A營養狀況的方法。它包括針對臨床乾眼病、麻疹、
營養不良患兒的臨床補充,利用現有衛生服務機構覆蓋面的目標投放以及針對所有高危人群的預防性補充。
目前WHO對不同高危人群維生素A缺乏的防治及未來研究需要提出以下幾點建議:
①5個月以下的嬰兒(包括新生兒):不推薦補充維生素A,維生素A補充對降低嬰兒發病率、死亡率的作用還待將來的
隨機對照試驗進一步證實,並對母親VAD高發地、維生素A和免疫功能的關係、確定該年齡組VAD的合適評價指標作進一步的研究。
②6~59個月的幼兒:建議對VAD是公共衛生問題(即該人群VAD發病率≥20%或夜盲症發病率≥1%)的6~59個月幼兒推行高劑量補充維生素A,其中6~11個月嬰兒(HIV+或-)補充10萬IU,12~59個月幼兒每4~6個月補充20萬IU。將來還需要進一步研究更好的維生素A補充方法,提高對維生素A和疫苗的共同干預作用的認識,以尋求更好的臨床和生化VAD的評價指標。
③孕婦:不推薦將維生素A補充作為預防孕婦和嬰兒發病、死亡的常規產前保健的一部分,而對VAD是嚴重公共衛生問題(即孕婦或24~59個月幼兒夜盲症發病率≥1%)的地區或國家(孕婦)的孕婦,可補充維生素A預防夜盲症,補充劑量:孕12以上的孕婦每天補充1萬IU或每周補充2.5萬IU,但補充的持續時間和補充頻率還需進一步研究。將來更多研究應關注孕期補充維生素A,尤其是聯合其他干預措施對死亡率的影響及孕後期3個月補充維生素A對母乳維生素A水平的影響的綜合回顧。
④乳母:不推薦對乳母補充維生素A作為預防母親和嬰兒發病、死亡的干預措施。對產後6周的乳母補充20萬IU的維生素A對母乳中視黃醇水平的影響作用及其新陳代謝、劑量分布、如何排泄等還待進一步研究。
⑤母嬰HIV感染:尚不建議對HIV陽性的母親進行維生素A的補充。