綠汀諾(注射用還原型谷胱甘肽),適應症為用於酒精及某些藥物(化療藥、抗腫瘤藥、抗結核藥、精神抑鬱藥、抗抑鬱藥、撲熱息痛)導致的中毒的輔助治療。用於酒精、病毒、藥物及其他化學物質導致的肝損傷的輔助治療。用於電離射線所致治療性損傷的輔助治療。用於各種低氧血症的輔助治療。
基本介紹
- 藥品名稱:綠汀諾
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:抗腫瘤輔助用藥
成份,性狀,適應症,規格,用法用量,不良反應,禁忌,注意事項,孕婦及哺乳期婦女用藥,兒童用藥,老年用藥,藥物相互作用,藥物過量,藥理毒理,藥代動力學,貯藏,包裝,有效期,執行標準,批准文號,生產企業,核准日期,修訂日期,
成份
本品主要成份:還原型谷胱甘肽
化學名稱:還原型谷胱甘肽
化學結構式:
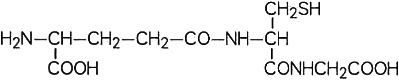
分子式:C10H17N3O6S
分子量:307.32
輔料:氫氧化鈉
性狀
本品為白色疏鬆塊狀物或粉末。
適應症
用於酒精及某些藥物(化療藥、抗腫瘤藥、抗結核藥、精神抑鬱藥、抗抑鬱藥、撲熱息痛)導致的中毒的輔助治療。用於酒精、病毒、藥物及其他化學物質導致的肝損傷的輔助治療。用於電離射線所致治療性損傷的輔助治療。用於各種低氧血症的輔助治療。
規格
0.3g;0. 6g;1.2g;1.8g
用法用量
可用於化療(順鉑,環磷醯胺,阿黴素,柔紅黴素,博來黴素)的輔助用藥,可以減輕化療造成的損傷而不影響療效,從而增加化療的劑量。首次給藥劑量1500mg/m[sup]2[/sup],溶於100ml生理鹽水或5%GS,15分鐘內靜脈輸注,在第2到5天,肌注,600mg每天。環磷醯胺治療後,應立即靜脈15分鐘輸注以減輕化療對泌尿系統的影響。對於順鉑治療,還原型谷胱甘肽劑量不超過35mg/mg順鉑,以免影響化療。或遵醫囑。
可用於酒精、病毒、藥物及其他化學物質導致的肝損傷的輔助治療。對於病毒性肝炎,1200mg,qd,iv,30天;重症肝炎,1200-2400mg,qd,iv,30天;活動性肝硬化,1200mg,qd,iv,30天;脂肪肝,1800mg,qd,iV,30天;酒精性肝炎,1800mg,qd,iv,14-30天;藥物性肝炎,1200-1800mg,qd,iv,14-30天。
用於放療輔助用藥,照射後給藥,劑量1500mg/m[sup]2[/sup],或遵醫囑。
對於低氧血症的治療,劑量1500mg/m[sup]2[/sup],溶於100ml生理鹽水,靜脈給藥,以後每天300-600mg肌注維持。
產品(300-600mg)肌注時必須完全溶於溶解液,溶解液需清澈無色。
靜脈注射給藥,藥物能夠被溶解液溶解然後緩慢注射,靜脈滴注給藥至少需要20ml溶解液。
不良反應
偶見臉色蒼白,血壓下降,脈搏異常等類過敏症狀,應停藥。偶見皮疹等過敏症狀,應停藥。偶有食欲不振、噁心、嘔吐、胃痛等消化道症狀,停藥後消失。注射局部輕度疼痛。
禁忌
對本品有過敏反應者禁用。
注意事項
1.如在用藥過程中出現皮疹、面色蒼白、血壓下降、脈搏異常等症狀,應立即停藥。
2.溶解後的溶液立即使用,剩餘的藥液不能再用。
3.肌內注射僅限於需要此途徑給藥使用,並避免同一部位反覆注射。
孕婦及哺乳期婦女用藥
缺少相關資料,尚不明確。
兒童用藥
新生兒、早產兒、嬰兒和兒童應謹慎用藥,尤其是肌內注射。
老年用藥
老年患者應適當減少用藥劑量。並在用藥過程中嚴密監視。
藥物相互作用
本品和下列藥物應避免混合使用:維生素B12、維生素K3、泛酸鈣、乳清酸、抗組胺製劑、長效磺胺藥及四環素。
藥物過量
尚未見有關本品藥物過量的資料。如發生藥物過量應對症治療。
藥理毒理
還原型谷胱甘肽是含有巰基(SH)的三肽類化合物,在人體內具有活化氧化還原系統,激活SH酶、解毒作用等重要生理活性。
本品參與體內三羧酸循環和糖代謝,促進體內產生高能量,起到輔酶作用。是甘油醛磷酸脫氫酶的輔基,又是乙二醛酶及磷酸丙糖脫氫酶的輔酶。本品能激活體內的SH酶等,促進碳水化合物。脂肪及蛋白質的代謝,以調節細胞膜的代謝過程。本品參與多種外源性、內源性有毒物質結合生成減毒物質。
藥代動力學
還原型谷胱甘肽以2g/m[sup]2[/sup]的劑量靜脈15分鐘輸液後,在輸液終點平均血漿達峰濃度為444毫摩爾/L(平均基礎濃度為6.9毫摩爾/L),平均分布容積為15L,平均消除半衰期為10分鐘,清除率為850ml/分/m[sup]2[/sup]。輔液後90分鐘由尿中主要以原形和半胱氨酸排出。
貯藏
密閉保存。
包裝
玻璃管制注射劑瓶包裝,每小盒10瓶。
有效期
24個月
執行標準
0.3g:WS-900(X-665)-2002(1);
0.6g:WS-900(X-665)-2002(2);
1.2g:WS-900(X-665)-2002(1);
1.8g:WS-900(X-665)-2002(1).
批准文號
0.3g:國藥準字H20030001;
0.6g:國藥準字H20030002;
1.2g:國藥準字H20041619;
1.8g:國藥準字H20041620。
生產企業
山東綠葉製藥股份有限公司
核准日期
2007年03月30日
修訂日期
2007年07月23日 2009年02月10日
