企業文化
真實醫藥創新 改善人類健康
以創新為驅動,致力於成為一家有世界競爭力的生物醫藥公司
發展歷程
2012年9月12日,河南真實生物科技有限公司成立。
2013年,真實生物提交阿茲夫定用於治療愛滋病感染的IND臨床試驗註冊申請,並於當年4月獲國家藥監局批准,隨後開始在中國進行阿茲夫定用於治療愛滋病感染的臨床試驗。
2014年,在中國開展阿茲夫定治療HIV的I期臨床試驗。
2015年,在中國完成阿茲夫定治療HIV的I期臨床試驗。
2017年,在中國開展阿茲夫定治療HIV的II期臨床試驗。
2019年,在中國完成阿茲夫定用於治療HIV的II期臨床試驗。
2020年,成立深圳真實生物醫藥科技有限公司和深圳研發中心;獲得國家藥監局批准並開展阿茲夫定治療COVID-19的III期臨床試驗。
2020年11月10日,真實生物分別與深圳市倚鋒投資管理企業、金百臨(香港)資產管理有限公司進行A輪融資簽約。
2021年2月,真實生物完成A輪投資,籌集約人民幣1.495億元。
2021年7月,真實生物自國家藥監局獲得一項阿茲夫定在中國治療愛滋病的附條件NDA批准。
2021年8月26日,真實生物宣布完成一億美元B輪融資,本輪戰略融資由倚鋒資本、盈科資本領投,迪賽諾、亞商資本、富強金融跟投,融資資金將用於產品研發、臨床項目註冊和已獲批上市的全球首個雙靶點抗愛滋病1類新藥阿茲夫定的商業化拓展等。
2022年,完成阿茲夫定治療COVID-19的國內III期臨床試驗;4月,完成B輪投資,籌集約人民幣5.633億元。
2022年7月,國家藥品監督管理局附條件批准阿茲夫定片增加治療新冠病毒肺炎適應症註冊申請,用於治療普通型COVID-19成年患者,標誌著阿茲夫定成為中國首個自主研發並擁有全球專利的口服小分子新冠肺炎治療藥物。
2022年7月15日,河南真實生物科技有限公司宣布,已正式向國家藥品監督管理局提交
阿茲夫定治療新型冠狀病毒適應症的上市申請。
2022年7月25日,國家藥監局根據《
藥品管理法》相關規定,按照藥品特別審批程式,進行應急審評審批,附條件批准河南真實生物科技有限公司阿茲夫定片增加治療新冠病毒肺炎適應症註冊申請。
2022年7月25日,河南真實生物科技有限公司與復星醫藥的附屬公司復星醫藥產業就阿茲夫定的聯合開發及復星醫藥產業獨家商業化達成戰略合作協定。
2022年8月2日,河南真實生物科技有限公司新冠口服藥阿茲夫定片投產儀式在平頂山市舉行。
2022年8月4日晚間港交所訊息,真實生物科技有限公司向港交所遞交上市申請書。
2022年8月7日,河南真實生物科技有限公司訊息,治療新冠肺炎的阿茲夫定片價格初定,每瓶不到300元,每瓶35片,每片1mg。
2022年8月9日,阿茲夫定片被納入《新型冠狀病毒肺炎診療方案(第九版)》,用於治療普通型新型冠狀病毒肺炎(COVID-19)成年患者。
2022年10月,河南真實生物科技有限公司宣布自主研發的新一代口服長效HIV候選藥物CL-197的臨床試驗申請(IND)正式獲得國家藥品監督管理局(NMPA)藥品審評中心(CDE)批准。
2022年11月,河南真實生物科技有限公司研發的國產新冠口服藥阿茲夫定片已在北京部分藥店正式線上開售,目前每瓶售價350元,每瓶35片。11月18日晚,有媒體報導稱,國產新冠口服藥阿茲夫定片已在北京部分藥店正式線上開售。對此,真實生物相關人士對《科創板日報》記者表示,已經第一時間就相關情況與相關藥店作出溝通,將即刻做下架處理。2022年12月,阿茲夫定開放網售可線上處方。
2023年1月,阿茲夫定片被納入《新型冠狀病毒感染診療方案(試行第十版)》。
2023年1月9日,真實生物聯合復星醫藥向中西部農村地區180個縣捐贈價值1億元的阿茲夫定片。
2023年1月18日,國產抗新冠口服藥阿茲夫定片正式納入國家醫保目錄。自2023年4月1日起,阿茲夫定片醫保支付價為175元/瓶。
2023年2月,阿茲夫定獲俄羅斯聯邦衛生部註冊批准上市,正式成為俄羅斯治療新冠病毒感染用藥。
公司核心研發高管
真實生物執行董事、董事長、執行長兼首席科學家

杜錦發博士
• 擁有超過25年的生物製藥行業藥物研發經驗
• 曾擔任Gilead Sciences, Inc. 的高級研究科學家
• 曾擔任Pharmasset Inc.的化學研究副總監
• 於Pharmasset任職期間,杜博士參與研發的索非布韋(亦被稱為索磷布韋),是一種革命性的治療C肝藥物,該藥物於2014年榮獲蓋倫基金會頒發的蓋倫獎; Gilead Sciences, Inc. 於2012年以約112億美元完成收購Pharmasset Inc.,從而獲得索非布韋。
• 已發表60篇學術論文並在全球參與發明逾300個註冊專利,其中40個專利註冊於美國
真實生物執行董事、總裁兼首席商務官

黨群博士
• 擁有將近30年的生物製藥行業研發、管理經驗
• 曾擔任石藥集團有限公司的全資附屬公司石藥集團中奇製藥技術(石家莊)有限公司副總裁,齊魯製藥有限公司副總裁
• 曾擔任禮來公司的禮來中國研發中心內分泌及心血管業務外部創新系統亞洲負責人
• 曾擔任Merck Sharp & Dohme Corp.外國合作化學項目總監、Metabasis Therapeutics, Inc.藥物化學總監
• 參與研發多種臨床套用藥物及候選藥物,包括用於治療II型糖尿病的第一代及第二代FBPase抑制劑
真實生物副總裁、深圳真實生物總經理

郭昌月博士
• 醫學、理學雙博士
• 擁有超20年的臨床醫學行業經驗
• 曾在美國University of Virginia Health System工作
• 曾於深圳維世達勝凱國際醫療中心擔任醫師和國際醫療中心主任
真實生物副總裁

李磐博士
擁有超過21年的創新藥研發經驗
• 曾擔任石藥集團有限公司附屬公司上海翊石醫藥科技有限公司的副總經理
• 曾擔任杭州阿諾生物醫藥科技有限公司藥物化學部執行總監
• 曾擔任美國Vertex公司主任研究員
產業布局
研發
• 深圳研發子公司:核苷類藥物發現技術平台、大分子新藥研發、ADC藥物發現藥物合成
• 上海研發子公司:FIC-BIC新藥研發、計算機輔助設計平台、AI輔助新藥研發(對外合作)、ADC全新payload發現
• 平頂山研究院:河南省現代醫藥研究院、基礎研發實驗室
運營
• 平頂山:註冊地、生產基地
• 北京:臨床管理、註冊報批、MAH管理、行銷管理、運營中心
• 深圳:全資子公司、資本運營中心、證券事務管理
研發平台
深圳真實生物醫藥科技有限公司坐落於福田國際生物醫藥產業園,以研發創新型大分子生物藥及小分子藥物為目標,以滿足臨床未滿足之需求為使命。深圳真實生物已搭建單克隆抗體、多肽藥物高通量篩選平台、小核酸藥物平台、藥理藥效測試平台和小分子藥物篩選平台,瞄準已被證實在腫瘤、炎症等多類型疾病中發揮關鍵生物學作用但尚未有藥物問世之靶點,自主開發包含單克隆抗體、雙抗、抗體偶聯藥物、多肽偶聯藥物、小核酸藥物以及新核苷類似物新藥、小分子致癌基因、蛋白降解劑類新藥等創新藥物。
上海翊維康醫藥有限責任公司為真實生物的研發子公司之一,科研團隊有近30年的新藥研發經驗,致力於FIC和BIC藥品的研發與創新,尤其在抗腫瘤和老年化疾病領域有著專業的研發經驗,該公司專注於全新靶點的藥物設計的同時也關注創新藥物在適用症、用藥途徑、毒副作用的差異化設計,利用藥物結構設計的經驗,達到創新藥物在臨床上具有優效性的目的。
• FIC-BIC 新藥研發
• 計算機輔助設計平台
• AI 輔助新藥研發
• ADC 全新 payload 發現
2021年10月16日,河南首批省產業研究院和中試基地揭牌儀式在鄭州舉行。其中,河南省現代醫藥產業研究院正式落地真實生物。河南省現代醫藥產業研究院圍繞創新藥物設計與研發、創新藥物產業化等方向開展研究,致力於為河南省醫藥人才培養、交流合作、成果轉化與市場推廣,將產業研究院建設成為國內領先的集研發、產業化於一體的創新聯合體。
上市藥品
阿茲夫定是中國首個具有完全自主智慧財產權的口服小分子新冠病毒治療藥物,於2022年7月25日獲國家藥監局附條件批准。2022年8月9日,國家衛生健康委辦公廳、國家中醫藥局辦公室將阿茲夫定納入《新型冠狀病毒肺炎診療方案(第九版)》。2022年12月7日納入廣東省藥學會最新版《新型冠狀病毒肺炎抗病毒治療臨床藥學指引》。2022年12月17日,河南省藥學會發布《阿茲夫定治療新型冠狀病毒肺炎河南藥學專家共識》。2023年1月6日阿茲夫定再次被納入第十版《新型冠狀病毒感染診療方案》。2023年1月18日,阿茲夫定片正式納入國家醫保藥品目錄。
阿茲夫定於2021年7月20日獲國家藥監局附條件批准用於治療高病毒載量的成年HIV-1感染患者。這是全球首款同時針對逆轉錄酶和病毒感染因子的雙靶點治療HIV感染核苷類口服藥物,獲得國家“重大新藥創製”科技重大專項立項支持,並被納入《中國愛滋病診療指南》。
產品管線
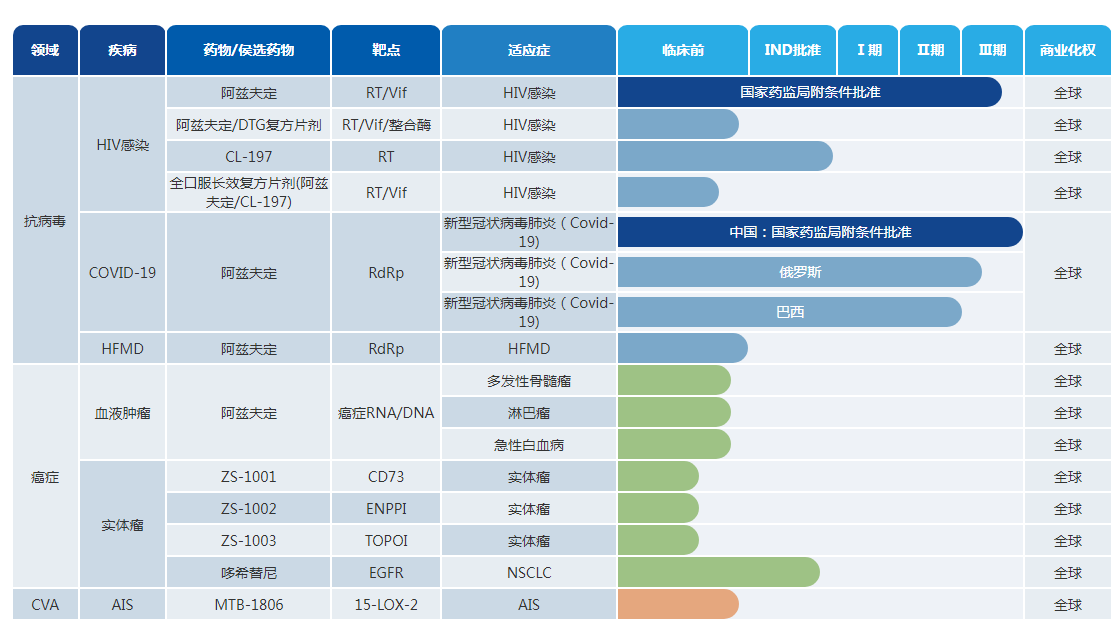
產品管線
阿茲夫定
阿茲夫定是全球首款同時針對逆轉錄酶和病毒感染因子的雙靶點治療HIV感染核苷類口服藥物。2021年7月,國家藥監局附條件批准阿茲夫定治療年齡為18歲以上攜帶高病毒載量的HIV-1感染患者(HIV-1感染患者占全球所有HIV感染患者的90%以上)的上市申請。阿茲夫定具有3個顯著優勢:1、活性更高,在臨床療效上,3mg 阿茲夫定≈ 300mg 拉米夫定;2、低耐藥風險:可治療對當前NRTI(包括拉米夫定)耐藥的患者雙靶點作用機制,耐藥機會減少;3、有潛力成為長效口服藥物:正如人體藥代動力學研究顯示,給藥120個小時後活性形式可在外周血單個核細胞中檢測到。
阿茲夫定可與不同機制的抗病毒藥物聯合用藥,作為多種二藥或三藥抗逆轉錄病毒治療方案中的骨幹藥物發揮作用。在II期臨床試驗中,阿茲夫定以低得多的劑量水平達到與另一種流行的NRTI相當的臨床療效,與單靶點 NRTI相比,其雙靶點機制可降低耐藥性風險。此外,阿茲夫定因其長效特性而已被證明有潛力成為治療HIV感染的長效口服治療藥物的一部分。為了進一步發掘阿茲夫定的優勢,公司還計畫開發以阿茲夫定為主要成分的複方片劑以治療HIV感染,並與其他藥物聯合,以提高療效。
CL-197
CL-197是一種開發中的新型口服長效HIV候選藥物,在中國提交的IND申請已於2022年10月獲得批准。臨床前研究結果表明CL-197能夠有效抑制HIV毒株的複製。CL-197將口服給藥,有望每周僅需服藥一次。這種相對方便的服藥方案亦可能提高服藥依從性,從而改善臨床結果。阿茲夫定與CL-197均在臨床前試驗中顯示出長效特徵,其組合用藥有潛力成為全球首款全口服長效HIV創新治療方案。
阿茲夫定╱DTG複方片劑
鑒於阿茲夫定具有雙靶點作用機制,有潛力與其他不同機制和功能的抗逆轉錄病毒藥物聯合開發成多種HIV複方片劑。阿茲夫定╱DTG 複方片劑正在開發中,用於治療HIV感染,將以阿茲夫定作為主要活性成分,與商業化抗逆轉錄病毒藥物多替拉韋(DTG)相結合,以提升潛在療效。阿茲夫定和DTG各自通過不同的靶點攻擊HIV,可預防長期使用單一藥物治療產生的耐藥性。一項藥物相互作用臨床研究已經開展,以評估複方片劑中阿茲夫定及 DTG之間的相互作用。
全口服長效複方片劑
基於阿茲夫定與CL-197在預防及治療HIV感染方面的潛在聯合長效特性及聯合作用機制,計畫開發一款全口服長效複方片劑,有望實現每周服藥並提高藥物依從性。2022年10月,CL-197在中國的IND申請已獲批。
阿茲夫定
阿茲夫定是一種廣譜RNA病毒抑制劑,作為一種人工合成的病毒RNA依賴的RNA聚合酶(RdRp)的核苷類似物,在細胞內代謝成具有抗病毒活性的5’-三磷酸鹽代謝物(阿茲夫定三磷酸鹽),能特異性作用於新冠病毒聚合酶(RdRp),在新冠病毒RNA合成過程中嵌入病毒RNA,從而抑制新冠病毒複製,達到治療新冠病毒感染的作用。
哆希替尼
在研候選藥物哆希替尼,是一種高活性、選擇性的口服表皮生長因子受體(EGFR)靶向候選藥物,用於治療晚期EGFR突變陽性非小細胞肺癌(NSCLC)。在臨床前研究中,哆希替尼對患者衍生的EGFR突變陽性非小細胞肺癌細胞系BaF3、HCC827及NCI-H1975的異種移植模型顯示出劑量依賴性抑制活性。其中,HCC827對哆希替尼最敏感對於三種選定的癌細胞系,在相同劑量水平下,哆希替尼的抑制活性與奧希替尼相當,且具有劑量依賴性。動物研究表明,與奧希替尼相比,哆希替尼可將毒性代謝產物(其中主要為AZ5104)水平降低多達80%。
哆希替尼已獲得國家藥監局批准進行I期/II期臨床試驗,以評估該藥物治療晚期 EGFR突變陽性局部晚期或轉移性非小細胞肺癌患者的安全性、耐受性、藥代動力學特徵及初步療效。已啟動患者招募流程,計畫2026年完成I期/II期試驗。
阿茲夫定
阿茲夫定作為核苷類藥物有潛在抗腫瘤活性(已被證明會干擾癌細胞中核酸的合成),公司也在開發阿茲夫定以治療若干類型的血液腫瘤。臨床前體外研究結果表明,阿茲夫定對多發性骨髓瘤、淋巴瘤及急性白血病癌細胞系具有有效活性,公司已完成臨床前研究。
ZS-1001
ZS-1001,是一種CD73的抑制劑。CD73可以促進腫瘤的免疫逃逸,靶向CD73的藥物可以遏制腫瘤發展轉移,並能與腫瘤免疫治療藥物聯用產生協同效應。
ZS-1002
ZS-1002,是ENPP1抑制劑。通過抑制ENPP1可以在腫瘤內選擇性地上調激發免疫反應的信號分子cGAMP,從而提高現有IO療法的有效率。
ZS-1003
ZS-1003是一款靶向TOPO1的抗腫瘤藥物。TOPO1參與DNA的正超螺旋或負超螺旋,在裂解反應中極易受TOPO1抑制劑影響,這意味著利用抗腫瘤藥物可在他們裂解癌細胞的DNA時將其捕獲。
MTB-1806
MTB-1806是用於治療AIS的小分子候選藥物。
生產製造
平頂山生產基地
公司平頂山生產基地總建築面積22262平米,2022年5月,基地順利通過省藥監局組織的藥品生產質量管理規範符合性檢查,標誌著公司自有的生產基地可以合規進行藥品的生產和經營。
生產廠房為阿茲夫定及其他候選藥物而設計及建造,涵蓋整個製造周期,包括生產、配藥、灌裝、包裝和質量核證以支持內部生產。
社會責任
2022年8月,真實生物聯合復星醫藥、復星基金會共同向西藏自治區政府捐贈5000瓶阿茲夫定片。
2023年1月9日,真實生物聯合復星醫藥通過上海復星公益基金會向中國農村地區捐贈價值1億元人民幣的阿茲夫定片。據統計,截至2023年2月28日,真實生物聯合復星醫藥通過上海復星公益基金會已向中國農村地區累計捐贈近30萬瓶阿茲夫定,覆蓋安徽、雲南、貴州、河南、甘肅、新疆、西藏、黑龍江、廣東、上海等地的250個市、縣。
公司榮譽
2022年4月20日,由證券時報舉辦的“2021藥物創新濟世獎年度評選”獲獎名單正式公布,真實生物自主研發的阿茲夫定片獲評“年度藥物創新成就獎”,阿茲夫定研發團隊獲評“年度十大藥物創新研究團隊”。
2023年1月12日,華夏時報社2022年度金手杖獎獲獎名單揭曉,真實生物榮獲“年度生物科技創新獎”。
2023年3月,“阿茲夫定治療新冠肺炎技術開發及套用”項目榮獲河南省技術發明獎一等獎。
2023年6月,河南真實生物科技有限公司榮獲“2022河南社會責任年度企業獎”。
2023年6月,《2022年度中國生物醫藥企業創新力百強系列榜單》發布,真實生物榮登“中國小分子藥物企業創新力TOP30排行榜”。
2023年10月13日,E藥經理人正式發布“2023中國醫藥創新種子企業100強”榜單,真實生物獲選入榜。
2023年11月17日,由華夏時報社主辦的第三屆金手杖獎揭曉儀式在京舉行,真實生物榮獲“2023年度生物科技十大創新企業獎”。
地理位置
平頂山市新城區復興路中段10號院內1號樓
北京市朝陽區八里莊街道慈雲寺北里遠洋國際中心二期E座16層1601
中國(上海)自由貿易試驗區碧波路690號1幢301室
深圳市福田區保稅區海紅道1號國際生物醫藥產業園一期三層330-332號






