污染物地質大循環是指環境中的污染物隨地質循環周而復始地運移過程。
基本介紹
- 中文名:污染物地質大循環
- 外文名:geological major cycle of pollutants
- 學科:環境科學
- 主體:污染物
釋文,循環過程,汞循環,鎘循環,砷循環,鉻循環,鉛循環,
釋文
污染物地質大循環是指環境中的污染物隨地質循環周而復始地運移過程。環境污染物的地質大循環遵循自然界的循環規律。環境中的污染物有的來自自然過程,如岩石風化的有害元素、火山噴發的有害氣體、大氣降塵、水流沖刷等過程,把污染物輸送入環境。有的來自人為釋放,如自然資源的開發利用,工業的廢水、廢氣、廢渣的排放等,都會把污染物排入大氣、河流、土壤之中,參與地質大循環。
循環過程
某些污染物如汞、鎘、砷、鉻、鉛的循環過程如下。
汞循環
環境中的汞主要是元素汞、二價汞化合物等。元素汞比重大,不溶於水,往往在廢水排放口附近沉積、富集。二價汞離子能被有機膠體和無機膠體吸附,並隨著這些載體一起在水體中運動。這些微粒如果聚集成顆粒較大的聚集體,就能在水體中沉降到底層,成為沉積物,並在微生物的作用下,生成甲基汞和二甲基汞。甲基汞溶於水中,被水生生物吸收和富集,通過食物鏈傳遞。二甲基汞揮發後進入大氣而擴散。二價汞也可以與羥基或絡離子結合,生成Hg(OH)、Hg(OH)2、Hg(OH)3和Hg(OH)4,以及HgCl、HgCl2、HgCl3等。汞與氯離子的絡合特別明顯,當環境中含Cl-為0.0001摩爾時,Hg(OH)2和HgS的溶解度可以增加55~408倍。因此河流中懸浮物吸附的汞和沉積物中的汞進入海洋後,又可以解吸出來。在還原條件下,二價汞又可以被還原成元素汞,揮發後以汞蒸汽的形態進入大氣。在含H2S的還原環境中汞可以形成硫化汞。

鎘循環
由於含鎘的岩石風化,鎘礦床的開採,特別是隨著工業上大量使用鎘作為電鍍、染料以及熱塑性塑膠的穩定劑後,鎘在環境中的循環量增加了。鎘的溶解度較汞大,因此環境中有簡單的鎘離子存在。河流底泥對水中的鎘有很強吸附作用,底泥對鎘的濃集係數在5000~50000之間。腐殖質是河水中鎘離子的主要吸附劑,吸附速度很快。腐殖質又可以對鎘進行螯合,因此鎘便隨著河水遷移。鎘與羥基和氯離子絡合,生成Cd(OH)、Cd(OH)2、Cd(OH)3,以及CdCl、CdCl2等絡合物,環境中的 Cl對鎘的絡合僅次於汞。被吸附、螯合和絡合的鎘被河水攜帶入海,在河口處和海水逐步混合,因水相的鹽度不斷升高,吸附的鎘在不同程度上被海水中的 Na、Mg所代替,使鎘又重新洗脫回到水相中。所以河水中的懸浮固體或腐殖質實質上起著把鎘輸送入海洋的作用。另一方面,被膠體吸附的鎘入海以後,由於海水的鹽度大而絮凝沉澱到海底,在還原條件下,鎘便生成硫化鎘而沉澱,最後作為海洋沉積物繼續參與地質大循環。
砷循環
在自然狀態下,從岩石和礦物中風化出來的砷,以及人為排放的砷,大都存在於地表水體和沉積物中。砷在水體中有四種價態 (+5、+3、0、-3)。元素砷只有在很少情況下存在,負三價砷只在還原條件下產生。因此,自然界中的砷主要是以砷酸鹽和亞砷酸鹽的形式存在。前者毒性只有後者的1/60。砷酸鹽很易被水合氧化鐵所吸附而共沉。亞砷酸鹽在行為上也類似於砷酸鹽,可以被氫氧化鐵吸附而共沉。砷對硫有親合力,易形成砷的硫化物而被固定下來。在富氧的表層湖水中,低價砷有被氧化成砷酸鹽的傾向。砷酸鹽在轉入缺氧的低層湖水後,被硫化氫還原成HAsO2和AsS2,最後轉變為難溶的砷的硫化物。微生物的甲基化作用能使砷再度溶於水中,參與生物循環。除了局部循環外,大部分淋溶出來的砷隨著地表徑流進入江河,最終輸往海洋。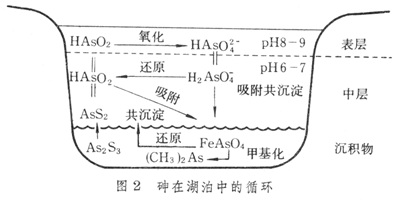

鉻循環
鉻在環境中的循環與環境氧化-還原條件有密切關係。在強氧化條件下,鉻可以形成具有很高的遷移能力的易溶性鉻酸鹽;在還原條件下,鉻則形成難溶性化合物沉澱下來。因此在氧化-還原電位發生劇變的地方,常出現鉻的富集。鉻也可以被腐殖質吸收,以溶膠狀態發生遷移。
鉛循環
鉛的地質大循環特點同鎘相似。鉛很容易被有機膠體或無機膠體吸附:被有機膠體的吸附順序為Pb>Cu>Ni>Zn>Cd>Fe>Mn;被蒙脫石等無機膠體吸附的順序也是鉛占第一位。因此鉛在河流的遷移時很易進入底泥沉積物中。據研究,鉛在離排污口10公里處,就有90%被淨化。而溶液中的鉛則隨河水進入海洋,並參與海洋沉積物的地質大循環。
含有上述污染物的顆粒物通過大氣傳輸,在環境中遷移。其中大的在一定條件下沉降到地面,小的則可被降水淋洗,進入河、湖、海等水體,參與地質大循環。
