像冰這樣熔融時體積收縮的物質統稱為水型物質,但這些物質並不多,鉍、鐐、鍺、三氯化鐵等少數物質屬於水型物質。印刷用的鉛字用鉛鉍合金燒鑄,就是利用其共凝固時的體積膨脹以充填鑄模。對於大多數物質來說,熔融時體積膨脹,相圖上的熔點點曲線向右傾斜。 壓力增加,熔點升高。這類物質統稱為硫型物質。
基本介紹
- 中文名:水型物質
- 外文名:Water-type substances
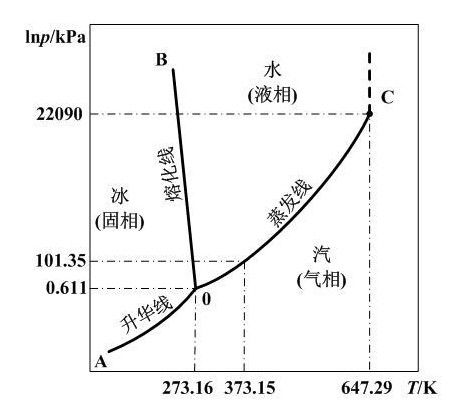
利用水的一元相圖,對理解 一元相圖如何通過不同的幾何要素(點線、面)來表達系統的不同平南狀態是有幫助的。在水的-元相圖上.整個圖面被三條曲線劃分為三個相區aob. coa及boc .分別代表冰、汽、水的單相區。在這三個單相區內,顯然溫度和壓力都可以在相區范聞內獨立改變而不會造我用相消失或新相產生。因而自由度為2。我們稱這時的系統是雙變數系統,或說系統是雙變數的。把三個單相區劃分開來的三條界線代表了系統中的兩相平衡狀態:OC代表水汽兩相平衡共存,因而液態水oc線實際上是水的飽和蒸氣壓曲線(蒸發曲線);ao代表冰汽兩相的平衡共存.因而oa線實際上是凍的飽和蒸氣壓曲線(升華曲線);0b線則代表冰水兩相平衡共存,因而ob線是凍的熔融曲線。在這三條界線上,顯然在溫度和壓力中只有一個是獨立變數,當一個參數獨立變化時,另參量必須沿著曲線指示的數值變化,而不能任意改變,這樣才能維持原有的兩相平衡,否則必然造成某一相的消失。因而此時系統的自由度為1,是單變數系統。三個單相區,三條界線會聚與o點,o點是一個三相點,反映了系統中的冰、水、汽三相平衡共存的狀態。 三相點的要度和壓力是嚴格恆定的。要想保持系統的這種三項平衡狀態,系統的壓力都不能有任何改變,否則系統的狀態點必然要離開三相點,進入單項區或界線三相平衡狀態,即從系統中消失一個或兩單相區或兩個舊相。因此,此時系統的自由度為0,處於無變數狀態。
水的相圖是個生動的例子,說明相圖如何用幾何語言把一個系統所處的平衡狀態直觀而形象地表示出來。只要知道了系統的溫度.壓力,即只要確定了系統點在相圖上的位置,便可以立即根據相圖判斷出此時系統所處的平衡狀態:有幾個相平衡共存,是哪幾個相。
在水的相圖上值得一提的是凍的熔點曲線ob向左傾斜.斜率為負值。這意味著壓力增大凍的熔點下降。這是由於冰熔化成水時體積收縮而造成的(0b的斜率可以根據克拉貝龍-克勞修斯方程計算: dp/dT =△H/(T△V).冰熔化成水時吸熱△H>0,而體積收縮△V<0,因而dp/dT<0。