《氯吡格雷硫酸鹽的固體製劑及其製備方法》是深圳信立泰藥業有限公司於2006年10月18日申請的專利,該專利的公布號為CN1935119,授權公布日為2007年3月28日,發明人是葉澄海。
《氯吡格雷硫酸鹽的固體製劑及其製備方法》涉及一種氯吡格雷硫酸鹽的固體製劑以及其製備方法。該固體製劑中加入了甘油棕櫚酸硬脂酸脂與微粉矽膠,並通過一種研磨等量遞增法製備,有效地減少了氯吡格雷的右旋異構體轉化為氯吡格雷左旋異構體,增加了固體製劑的穩定性和安全性。
2015年11月27日,《氯吡格雷硫酸鹽的固體製劑及其製備方法》獲得第十七屆中國專利獎金獎。
基本介紹
- 中文名:氯吡格雷硫酸鹽的固體製劑及其製備方法
- 申請人:深圳信立泰藥業有限公司
- 申請日:2006年10月18日
- 申請號:2006100631517
- 公布號:CN1935119
- 公布日:2007年3月28日
- 發明人:葉澄海
- 地址:廣東省深圳市福田區深南大道6007號創展中心1901、1902、1903、1923室
- Int.Cl.:A61K9/00(2006.01)、A61K31/4365(2006.01)、A61P7/02(2006.01)
- 類別:發明專利
專利背景,發明內容,專利目的,技術方案,有益效果,技術領域,權利要求,實施方式,榮譽表彰,
專利背景
氯吡格雷是一種誘導性的血小板凝集抑制劑,通過抑制磷酸腺苷與其受體相結合而起作用。氯吡格雷是一種無活性的前體藥物,經肝細胞色素P450代謝轉化成活性代謝物發揮藥效。專利FR2215948和FR2530247公開了氯吡格雷具有顯著的抗血小板聚集和抗血栓形成的作用。氯吡格雷通過抑制血小板凝集減少了動脈阻塞的機會,達到預防中風和心臟病發作的療效,並能有效地治療和預防動脈粥樣硬化。
氯吡格雷通常以其硫酸鹽形式給藥。其結構如下:
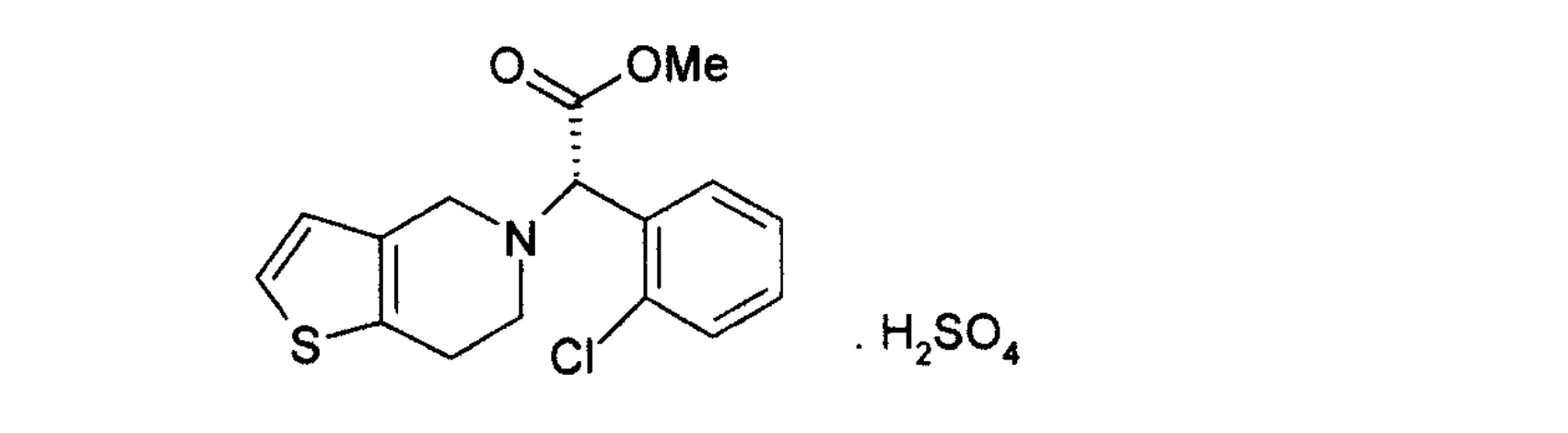
2006年10月之前市售的氯吡格雷硫酸鹽的片劑存在很多缺陷,長期以來,對氯吡格雷硫酸鹽固體製劑研究主要集中於解決氯吡格雷降解為氯吡格雷酸的問題,提高其穩定性。
專利EP1310245中報導了氯吡格雷與常用潤滑劑硬脂酸鎂之間的相互作用會導致氯吡格雷降解為氯吡格雷酸。該專利中公開了使用硬脂酸鋅、硬脂酸或者硬脂富馬酸鈉代替硬脂酸鎂作為潤滑劑解決氯吡格雷降解為氯吡格雷酸的問題。其片劑的製備採用乾法或濕法制粒壓片。
專利US5520928(1996-05-28)公開了用硬脂酸代替硬脂酸鎂作為潤滑劑的處方,其片劑的製備採用乾法壓片,解決氯吡格雷降解為氯吡格雷酸的問題;專利WO0001364公開了用聚乙二醇代替硬脂酸鎂作為潤滑劑的處方,其片劑的製備採用濕法制粒,解決氯吡格雷降解為氯吡格雷酸的問題;US4591592(1986-05-27)公布了將硬脂酸、安息香酸、酒石酸或反丁烯二酸作抗氧劑與硬脂酸鎂一同使用解決氯吡格雷降解為氯吡格雷酸的問題,其片劑的製備採用濕法制粒。
WO2005/070464公開了通過使用氫化植物油和羧甲基澱粉鈉合用作為潤滑劑克服片劑中氯吡格雷降解為氯吡格雷酸的問題。該專利中公開的片劑的製備採用直接粉末壓片。
但是,在實踐中發現,氯吡格雷硫酸鹽片劑中,氯吡格雷的右旋異構體會轉化為較多量的氯吡格雷左旋異構體。現有技術報導氯吡格雷的左旋異構體幾乎沒有抗血小板凝集的作用,並且動物實驗結果顯示氯吡格雷的左旋異構體的毒性顯著高於氯吡格雷的右旋異構體。臨床上氯吡格雷主要用於心臟和血管支架手術中,該手術風險高,即使氯吡格雷左旋物的含量稍有增加,對於手術的成功率也有很大影響,現有片劑中氯吡格雷的右旋異構體極易轉化為氯吡格雷左旋異構體,增加毒性和手術風險。因此臨床上對該藥物的質量要求非常高,氯吡格雷左旋物的含量已成為生產質量控制的一個重要參數。而對氯吡格雷左旋物的含量的控制問題一直未得到解決。
發明內容
專利目的
《氯吡格雷硫酸鹽的固體製劑及其製備方法》的目的是提供一種氯吡格雷硫酸鹽的固體製劑,解決了氯吡格雷硫酸鹽固體製劑中氯吡格雷右旋異構體轉化為氯吡格雷左旋異構體的問題,提高氯吡格雷固體製劑的安全性和穩定性,使其更有效的發揮治療作用。
技術方案
《氯吡格雷硫酸鹽的固體製劑及其製備方法》採用如下技術方案:以氯吡格雷硫酸鹽作為主藥,以無水乳糖、預膠化澱粉、聚甘油硬脂酸酯、羧甲基澱粉鈉、微粉矽膠、甘油棕櫚酸硬脂酸脂等作為輔料,乾法壓片。
該發明中,發現使用甘油棕櫚酸硬脂酸脂與微粉矽膠可以很好的抑制氯吡格雷固體製劑中氯吡格雷右旋異構體轉化為氯吡格雷左旋異構體。
上述氯吡格雷硫酸鹽其含量為固體製劑重量的14.3~40.0%。
上述甘油棕櫚酸硬脂酸脂為潤滑劑,其含量為固體製劑重量的0.8~1.2%,微粉矽膠的含量為固體製劑重量的3.3~4.8%。
上述輔料中,無水乳糖的含量為固體製劑重量的19.7~28.5%;預膠化澱粉的含量為固體製劑重量的12.5~18.0%;聚甘油硬脂酸酯的含量為固體製劑重量的17.1~24.7%;羧甲基澱粉鈉作為崩解劑,其含量為固體製劑重量的5.9~8.5%。
上述固體製劑包括:片劑,膠囊劑、顆粒劑等。
該發明提供了一種氯吡格雷硫酸鹽固體製劑的製備方法,該方法通過研磨等量遞增法製備。
上述方法為:
1)將聚甘油硬脂酸酯與氯吡格雷硫酸鹽混合後均勻壓片,將所得片劑粉碎後過篩制粒。
2)將操作1)所得顆粒與無水乳糖、預膠化澱粉、微粉矽膠混合均勻後再壓片,將所得片劑粉碎後過篩制粒。
3)將操作2)所得顆粒與羧甲基澱粉鈉和甘油棕櫚酸硬脂酸脂混合均勻後經適宜方法製成相應固體製劑。
上述操作1)中,為了能夠充分混合,將上述物料於球型粉碎機中混合粉碎30分鐘後,再將粉碎腔體及其內的物料升溫至攝氏45度至55度再研磨粉碎30分鐘。所述的壓製得片劑,硬度為2.0千克/平方厘米至2.8千克/平方厘米;所述粉碎的顆粒是通過快速整粒機1.0毫米篩網整粒粉碎,篩取60目以上的細顆粒。
上述操作2)中壓製得片劑硬度為2.0千克/平方厘米至2.8千克/平方厘米;所述粉碎的顆粒是通過快速整粒機1.0毫米篩網整粒粉碎,篩取40目至60目的顆粒。
上述操作3)中適宜的方法製成固體製劑,包括直接壓製得到片劑、混合均勻裝制膠囊等。
意外的發現,該發明的研磨等量遞增法製得的氯吡格雷硫酸鹽片劑在穩定性試驗中顯示其中的氯吡格雷左旋異構體的含量幾乎沒有明顯增加,進一步提高了氯吡格雷硫酸氫鹽片劑的穩定性,同時提高了臨床安全性。
有益效果
下面經過檢測說明《氯吡格雷硫酸鹽的固體製劑及其製備方法》的有益效果。
一、檢測指標及方法
以ULTRONES-OVM為填充劑,在柱溫25℃,檢測波長為220納米條件下,以乙腈-0.01摩爾/升的磷酸二氫鉀溶液(25:75)為流動相,進行加速和長期穩定性試驗檢測左旋氯吡格雷的含量。國家標準規定,氯吡格雷左旋物的含量不得超過1%。
二、實施例樣品與現有技術對照品中左旋氯吡格雷的檢測結果
1、長期穩定性試驗
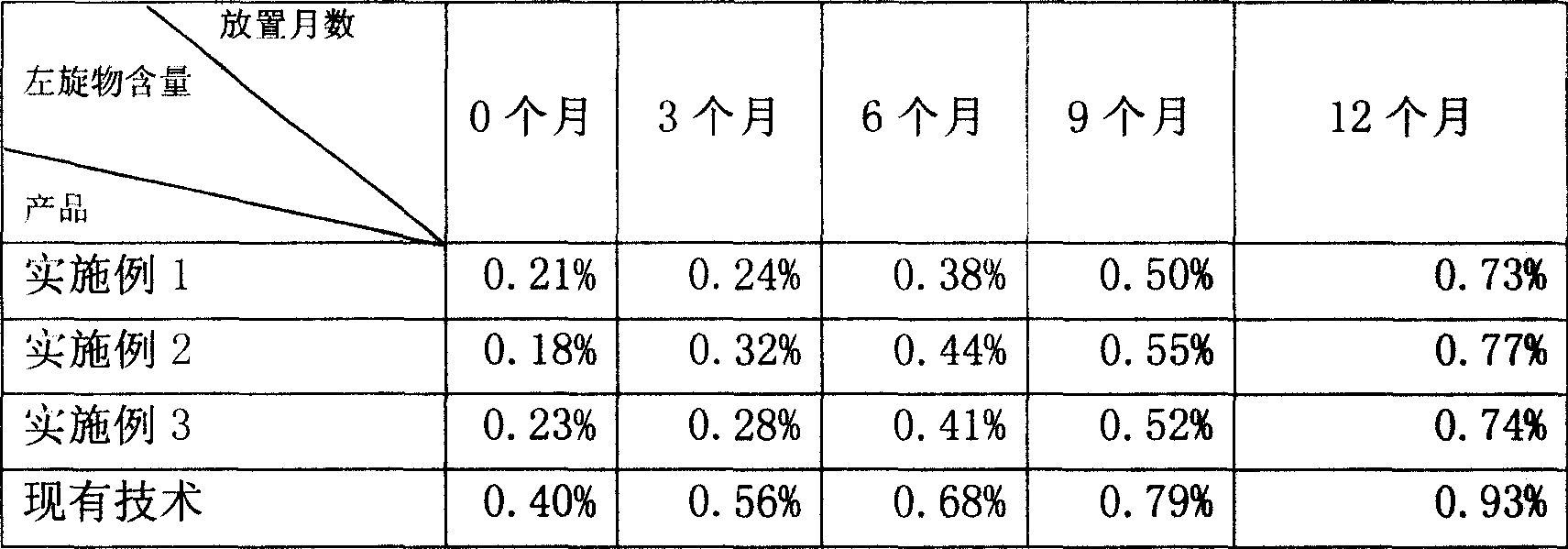
2、加速穩定性試驗
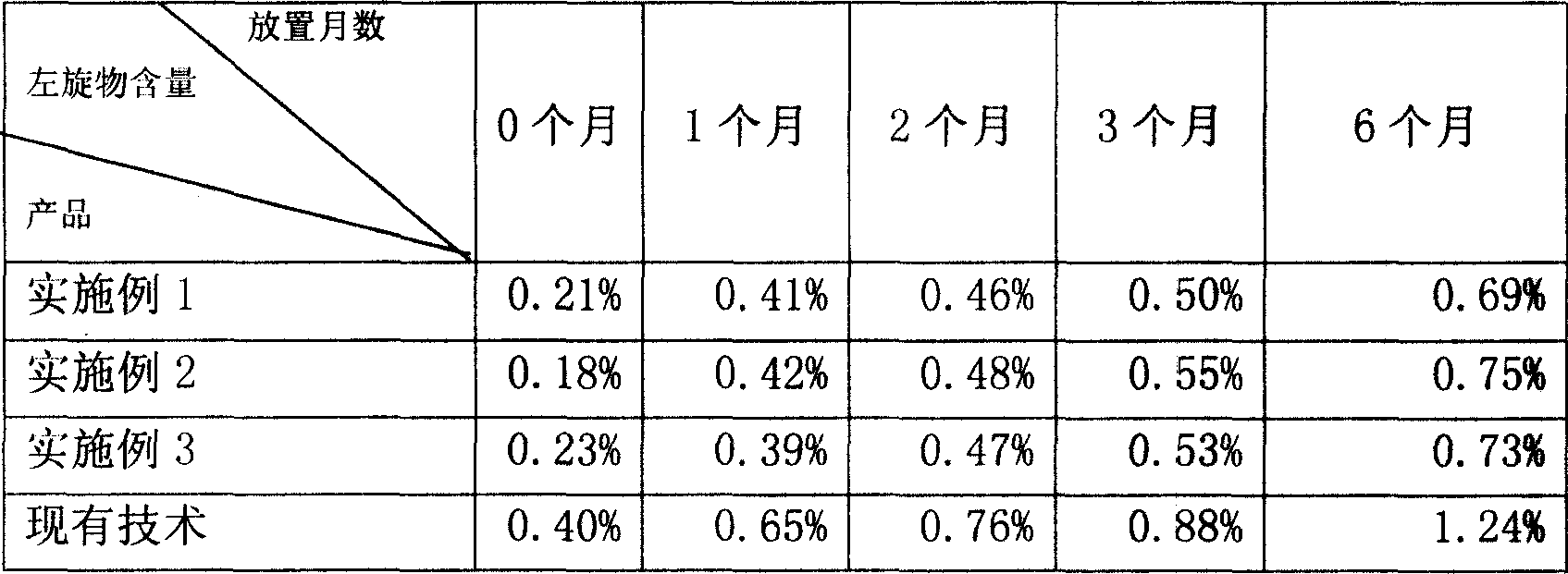
技術領域
《氯吡格雷硫酸鹽的固體製劑及其製備方法》涉及一種藥物的固體製劑及其製備方法,尤其是氯吡格雷硫酸鹽的固體製劑和通過研磨等量遞增法製備該固體製劑的方法。
權利要求
1、一種氯吡格雷硫酸鹽的固體製劑,其特徵是:以氯吡格雷硫酸鹽作為主藥,配入以無水乳糖、預膠化澱粉、聚甘油硬脂酸酯、羧甲基澱粉鈉、微粉矽膠和甘油棕櫚酸硬脂酸脂為輔料。
2、如權利要求1所述固體製劑,其特徵是:所述的甘油棕櫚酸硬脂酸脂含量為固體製劑重量的0.8~1.2%,微粉矽膠的含量為固體製劑重量的3.3~4.8%。
3、如權利要求1或2所述固體製劑,其特徵是:所述的無水乳糖的含量為固體製劑重量的19.7~28.5%;預膠化澱粉的含量為固體製劑重量的12.5~18.0%;聚甘油硬脂酸酯的含量為固體製劑重量的17.1~24.7%;羧甲基澱粉鈉的含量為固體製劑重量的5.9~8.5%。
4、如權利要求1或2所述的氯吡格雷硫酸鹽固體製劑的製備工藝,其特徵是:
1)將聚甘油硬脂酸酯與氯吡格雷硫酸鹽混合後均勻壓片,將所得片劑粉碎後過篩制粒。
2)將操作1)所得顆粒與無水乳糖、預膠化澱粉、微粉矽膠混合均勻後再壓片,將所得片劑粉碎後過篩制粒。
3)將操作2)所得顆粒與羧甲基澱粉鈉和甘油棕櫚酸硬脂酸脂混合均勻後經適宜方法製成應固體製劑。
實施方式
- 具體實施例
1、單位片重為0.175克,氯吡格雷含量25毫克/片的片劑處方及研磨等量遞增法製備工藝
組成 | 含量(克) |
氯毗格雷硫酸氫鹽 | 32.6 |
無水乳糖 | 64.78 |
預膠化澱粉 | 41.0 |
聚甘油硬脂酸酯 | 56.17 |
梭甲基澱粉鈉 | 19.27 |
微粉矽膠 | 10.91 |
甘油棕梱酸硬脂酸脂 | 2.75 |
1)將氯吡格雷硫酸氫鹽32.6克與聚甘油硬脂酸酯56.17克混合均勻,壓片,將所得片劑粉碎後過60目篩。
2)將操作1)得到的顆粒與無水乳糖64.78克、預膠化澱粉41.0克和微粉矽膠10.91克充分混合壓片,將所得片劑粉碎後過40-60目篩。
3)將操作2)所得物料與羧甲基澱粉鈉19.27克和甘油棕櫚酸硬脂酸脂2.75克混合均勻後壓片。
2、單位片重為0.150克,氯吡格雷含量25毫克/片的片劑處方及研磨等量遞增法製備工藝
組成 | 含量(克) |
氯毗格雷硫酸氫鹽 | 32.6 |
無水乳糖 | 55.2 |
預膠化澱粉 | 34.9 |
聚甘油硬脂酸酯 | 47.8 |
梭甲基澱粉鈉 | 13.9 |
微粉矽膠 | 8.3 |
甘油棕桐酸硬脂酸脂 | 2.24 |
1)將氯吡格雷硫酸氫鹽32.6克與聚甘油硬脂酸酯47.8克混合均勻,壓片,將所得片劑粉碎後過60目篩。
2)將操作1)得到的顆粒與無水乳糖55.2克、預膠化澱粉34.9克和微粉矽膠8.3克充分混合壓片,將所得片劑粉碎後過40-60目篩。
3)將操作2)所得物料與羧甲基澱粉鈉13.9克和甘油棕櫚酸硬脂酸脂2.24克混合均勻後壓片。
3、單位片重為0.063克,氯吡格雷含量25毫克/片的片劑處方及研磨等量遞增法製備工藝
組成 | 含量(克) |
氯毗格雷硫酸氫鹽 | 32.6 |
無水乳糖 | 15.8 |
預膠化澱粉 | 10.0 |
聚甘油硬脂酸酯 | 13.7 |
梭甲基澱粉鈉 | 4.7 |
微粉矽膠 | 2.66 |
甘油棕桐酸硬脂酸脂 | 0.67 |
1)將氯吡格雷硫酸氫鹽32.6克與聚甘油硬脂酸酯56.17克混合均勻,壓片,將所得片劑粉碎後過60目篩。
2)將操作1)得到的顆粒與無水乳糖64.78克、預膠化澱粉41.0克和微粉矽膠10.91克充分混合壓片,將所得片劑粉碎後過40-60目篩。
3)將操作2)所得物料與羧甲基澱粉鈉19.27克和甘油棕櫚酸硬脂酸脂2.75克混合均勻後壓片。
榮譽表彰
2015年11月27日,《氯吡格雷硫酸鹽的固體製劑及其製備方法》獲得第十七屆中國專利獎金獎。

