離子化合物(例如氯化鈉)所含的陽離子和陰離子緊密而有規律地排列,形成巨型離子結構。帶相反電荷的離子借著強大的離子鍵連線。
基本介紹
- 中文名:巨型離子結構
- 外文名:giant ionic structrue


離子化合物 | 氯化鈉 | 氧化鎂 |
化學式 | NaCl | MgO |
熔點(℃) | 808 | 2852 |
沸點(℃) | 1465 | 3600 |
在常溫常壓下的狀態 | 固體 | 固體 |
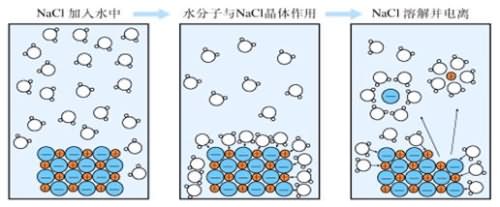
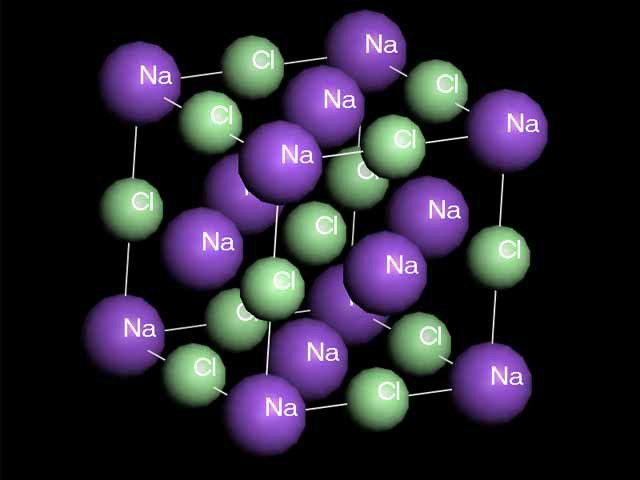
離子化合物(例如氯化鈉)所含的陽離子和陰離子緊密而有規律地排列,形成巨型離子結構。帶相反電荷的離子借著強大的離子鍵連線。


離子化合物 | 氯化鈉 | 氧化鎂 |
化學式 | NaCl | MgO |
熔點(℃) | 808 | 2852 |
沸點(℃) | 1465 | 3600 |
在常溫常壓下的狀態 | 固體 | 固體 |

離子化合物(例如氯化鈉)所含的陽離子和陰離子緊密而有規律地排列,形成巨型離子結構。帶相反電荷的離子借著強大的離子鍵連線。定義:離子化合物(例如氯化鈉)所含的陽離子和陰離子緊密而有規律地排列,形成巨型離子結構。帶相反電荷的...
《“巨型”量子點基太陽能電池研究》是依託蘇州大學,由鄒貴付擔任項目負責人的青年科學基金項目。項目摘要 擬構建新型量子點結構太陽能電池實現高效光伏轉化。量子點具有潛在高效的光伏效應,但由於主要發生在量子點界面的電子與孔穴Auger 複合和表面有機配體阻礙了它光伏轉化效能。消除界面和替代表面的有機配體是實現量子...
巨型超大類星體群(英文:Huge Large Quasar Group,簡稱Huge-LQG,也被稱為U1.27)是由73個類星體組成的超大類星體群,其跨度大約有40億光年。在其被發現時,被認為是當時可見宇宙中已經確認的最大、質量最重的結構,直到2013年發現跨度更長達到100億光年的武仙-北冕座長城。發現 2013年1月11日,來自英國...
1965年,有科學家提出均由碳原子組成的巨型籠狀分子結構是可能存在的。1970年,日本科學家大澤映二根據量子化學理論提出自然界中還應該還存在其他類型的碳同素異形體,並預測其結構與足球相似。1984年,美國科學家羅爾文等人在用質譜儀研究超聲氦氣流中被雷射氣化的石墨凝聚物時,發現了一族全新的碳原子簇C₃₀-C...
原子晶體,是指相鄰原子間以共價鍵相結合形成的具有空間立體網狀結構的晶體。整塊晶體是一個三維的共價鍵網狀結構,它是一個“巨分子”,又稱共價晶體。原子晶體一般具有熔、沸點高,硬度大,不導電,難溶於常見的溶劑等性質。由於共價鍵具有方向性和飽和性,所以每箇中心原子周圍排列的原子數目是有限的;所有原子間均...
3、獲得了一系列新的銦-有機框架結構和過渡金屬-有機框架結構,並研究了它們潛在的磁性和發光性質;4、獲得了一類具有獨特的具有"結構記憶"功能的金屬配合物,研究了其對異金屬的捕獲而引起的結構及性質變化;5、發現了一類前所未有的集s,3d,4d,5d和4f金屬於一體的巨型高核異金屬氧簇及其拓展的三維結構材料...
猶他州立大學的文章共同作者Alex Boldyrev說:“極高的壓力,比如在地球的核心或者其他巨型星體中,能夠完全改變氦的化學特性。”研究人員通過“晶體結構預測”模型進行演算發現,在極度的壓力之下,一種穩定的氦鈉化合物能夠形成。然後他們在金剛石壓腔實驗中真的創造出了前所未見的化合物:Na₂He。實驗可以為氦和...
