酯酸催化水解機理:酯在酸性溶液中水解是不可逆的,酸的酯化和酯的水解在機理上是等同的,平衡位置在於水和醇的相對濃度。單分子酸催化烷氧斷裂,縮寫為Aal1。
基本介紹
- 中文名:單分子酸催化烷氧斷裂
- 外文名:Aal1
背景知識,羧酸衍生物的物化性質,羧酸衍生物的水解,單分子酸催化烷氧斷裂的機理,影響因素,相關知識,
背景知識
羧酸衍生物的物化性質
酯常為液體,低級酯具有香味,酯的比重小,在水中溶解度低,是優良的有機溶劑。羧酸衍生物的化學性質可以分為兩大類:一是衍生物的相互轉化;另外是衍生物自身的特性反應。
羧酸衍生物的水解
根據酸鹼的催化,烷氧基和醯氧基的斷裂,可以分為8種類型,其中Bac1和Aal2尚未被發現。

單分子酸催化烷氧斷裂的機理
酯酸催化水解機理:酯在酸性溶液中水解是不可逆的,酸的酯化和酯的水解在機理上是等同的,平衡位置在於水和醇的相對濃度。酯中有兩個具有未共同電子對的氧原子,它們在酸中都有可能被質子化。NMR研究表明,質子化主要發生在羰基氧上。因羰基氧質子化後正電荷離域在兩個氧原子上,熱力學上比較穩定,並提高羧基與親核試劑反應的能力。烷基氧質子化的酯較少,但質子化後可促使烷氧基離去,對某些酯的水解起著促進作用。
單分子酸催化烷氧斷裂,縮寫為 ;叔醇酯和二苯甲醇酯在酸催化下按
;叔醇酯和二苯甲醇酯在酸催化下按 機理水解:
機理水解:


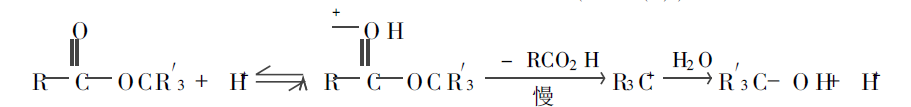
反應的第一步是酯中羰基質子化,從而增加羰基碳的正電性,有利於親核試劑的進攻。第二步是質子化的羰基與水加成形成帶正電荷的四面體結構的中間體。第三步是質子轉移和消除醇分子,生成羧酸。
影響因素
羧酸酯水解影響因素:RCOOR′的水解決定於R、R′的結構和性質,而R、R′對水解速率的影響又因反應機理而不同。影響酯水解的因素為電子效應和空間效應。
該反應速率取決於形成四面體結構中間體的穩定性。與鹼溶液水解反應一樣,R和基閉體積增大,反應速率降低;與鹼液水解不同的是中間體帶正電荷,所以R基團供電子能力增強,使中間體穩定而水解反應速率加快。即控速步驟是質子化酯的離解,生成比較穩定的叔碳正離子中間體。因叔烷基的空間位阻降低了水的進攻能力,如 、
、 的酸性水解。
的酸性水解。


相關知識
羧酸酯鹼的機理:
酯在鹼性溶液中的水解,產生鹼性較強的烷氧基負離子和酸性較弱的羧酸,二者發生反應使平衡移向產物,故酯的鹼性水解是不可逆的。羥基進攻酯的羰基碳,形成帶負電荷的四面體結構的中間體,是反應速率最慢的一步。緊接著烷氧基離去,形成羧酸和烷鋮基負離子,兩者迅速發生酸鹼中和反應(不可逆反應),生成醯氧基負離子(鹽〉和醇。
酯在鹼溶液中的水解反應的速率主要取決於四面體的中間體的穩定性,凡能分散負電荷的取代基,即在酯羰基附近連有的吸電子基越多,可使中間體穩定,反應越易進行。

