伊匹木單抗注射液是由百時美施貴寶研製開發的一種重組人源化單克隆抗體,可與細胞毒性T淋巴細胞相關抗原-4(CTLA-4)結合。
2011年3月25日,美國食品藥品監督管理局(FDA)批准逸沃(3 mg / kg)單藥療法用於治療無法手術切除或轉移性黑色素瘤患者。逸沃已在50多個國家獲批用於治療無法手術切除或轉移性黑色素瘤。逸沃正在多個腫瘤類型中開展更廣泛的探索。
2021年6月,中國食品藥品監督管理局(NMPA)批准歐狄沃(PD-1抑制劑)聯合逸沃(CTLA-4抑制劑)用於治療不可手術切除的、初治的非上皮樣惡性胸膜間皮瘤成人患者。歐狄沃聯合逸沃(又稱“免疫雙子星”)成為中國首個且唯一的雙免疫治療。
基本介紹
- 中文化學名:伊匹木單抗注射液
- 外文化學名:Ipilimumab Injection
- 開發公司:百時美施貴寶
- 獲批時間:2021年6月
- 商品名:Yervoy 逸沃
作用機制,歐狄沃聯合逸沃的適應證,在全球,在中國,逸沃相關全球適應症,CSCO指南對歐狄沃聯合逸沃的推薦,
作用機制
伊匹木單抗可與細胞毒性T淋巴細胞相關抗原4(CTLA-4)結合。CTLA-4是一種T細胞活化的負調控因子,伊匹木單抗與CTLA-4結合後,能阻斷CTLA-4與其配體CD80/CD86的相互作用。阻斷CTLA-4已被證明能夠增強T細胞的活化和增殖,包括腫瘤浸潤性效應T細胞的活化和增殖。抑制CTLA-4信號傳導還可減弱調節性T細胞的功能,這可能有助於T細胞反應性(包括抗腫瘤免疫反應)的普遍提升。
除CTLA-4外,PD-1/PD-L1也是位於腫瘤細胞表面,抑制T細胞抗癌能力的另一關鍵信號通路。目前,逸沃已被證實,與另一不同機制的免疫腫瘤藥物PD-1抑制劑歐狄沃聯合治療,可產生協同增效的抗癌能力。
作為CTLA-4抑制劑,逸沃在T 細胞發育早期的活化階段作用於淋巴結,通過抑制CTLA-4信號通路,解除癌細胞對T細胞增殖的抑制,從而幫助T細胞大量增殖、活化;逸沃激活的部分T細胞還可以分化為記憶T細胞,從而牢記戰鬥,保持長期作戰實力。同時,PD-1抑制劑歐狄沃則在T 細胞成熟後的效應階段作用於腫瘤微環境,通過切斷腫瘤細胞表面的PD-1/PD-L1信號通路,幫助T細胞恢復識別腫瘤細胞,以殺滅腫瘤細胞。
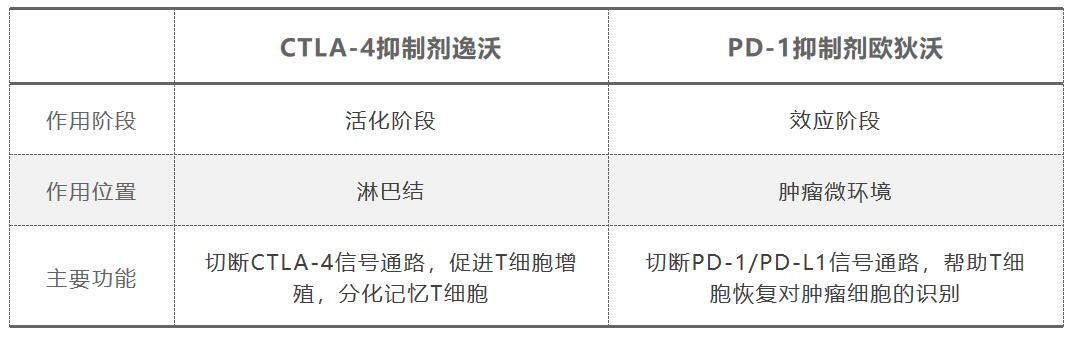
產品對比
歐狄沃聯合逸沃是兩種免疫檢查點抑制劑的獨特組合,能夠系統作用於腫瘤免疫的不同環節和維度,共同促進抗腫瘤免疫反應的發生和維持,幫助殺傷腫瘤細胞,助力抗癌實現1+1>2的協同效應。
歐狄沃聯合逸沃的適應證
在全球
2015年10月獲批成為全球首個獲得監管機構批准的免疫腫瘤藥物組合療法,目前適應症涵蓋:黑色素瘤、晚期腎細胞癌、結直腸癌、肝細胞癌、轉移性非小細胞肺癌、惡性胸膜間皮瘤。
開發歐狄沃與逸沃所基於的早期研究均已被授予諾貝爾獎。歐狄沃和逸沃也是全球唯一由諾貝爾生理學或醫學獎得主直接參與開發的免疫檢查點抑制劑。百時美施貴寶擁有本庶佑博士的PD-1專利獨家使用權。
在中國
2021年6月,歐狄沃聯合逸沃成為國內首個且目前唯一獲批的雙免疫治療。逸沃成為第一個也是目前唯一在國內獲批的CTLA-4抑制劑。
-歐狄沃聯合逸沃成為15餘年來首個為胸膜間皮瘤患者帶來生存獲益的系統性療法。
-歐狄沃聯合逸沃是首個且目前唯一經III期臨床研究證實與標準化療相比,一線雙免疫治療能夠為惡性胸膜間皮瘤患者帶來總生存獲益的治療方案。
逸沃相關全球適應症
# | 藥品 | 適應症 | 首次獲批 | |
日期 | 國家 | |||
1 | 逸沃 | 不可切除晚期或轉移性黑色素瘤 | 2011年3月25日 | 美國 |
2 | 歐狄沃聯合 伊匹木單抗注射液 | BRAF野生型不可切除或轉移性黑色素瘤 | 2015年10月1日 | 美國 |
歐狄沃聯合 伊匹木單抗注射液 | 轉移性黑色素瘤(不限BRAF突變狀態) | 2016年1月23日 | 美國 | |
3 | 歐狄沃聯合 伊匹木單抗注射液 | 中高危晚期腎細胞癌 | 2018年4月16日 | 美國 |
4 | 歐狄沃聯合 伊匹木單抗注射液 | 既往接受化療(氟尿嘧啶、奧沙利鉑、伊立替康)後疾病進展的高微衛星不穩定性(MSI-H)或錯配修復缺陷(dMMR)的轉移性結直腸癌兒童(12歲及以上)和成人患者 | 2018年7月10日 | 美國 |
5 | 歐狄沃聯合 伊匹木單抗注射液 | 既往接受過索拉菲尼治療的晚期肝細胞癌 | 2020年3月11日 | 美國 |
6 | 歐狄沃聯合 伊匹木單抗注射液 | 轉移性或復發性非小細胞肺癌(PD-L1≥1%)一線治療 | 2020年5月15日 | 美國 |
7 | 歐狄沃聯合 伊匹木單抗注射液及2個周期的含鉑化療 | 轉移性或復發性非小細胞肺癌一線治療 | 2020年5月26日 | 美國 |
8 | 歐狄沃聯合 伊匹木單抗注射液 | 既往未經治療的、不可切除的惡性胸膜間皮瘤患者 | 2020年10月2日 | 美國 |
CSCO指南對歐狄沃聯合逸沃的推薦
在最新發布的《中國臨床腫瘤學會(CSCO)免疫檢查點抑制劑臨床套用指南(2021年版)》中,歐狄沃聯合逸沃一線治療非上皮樣型和上皮樣型胸膜間皮瘤成為唯一獲得I級(1類證據)和II級推薦(2A類證據)的治療藥物。
# | 癌種 | 具體推薦 | 推薦級別及證據類別 |
1 | 胸膜間皮瘤 | 納武利尤單抗聯合伊匹木單抗被推薦用於一線治療非上皮型胸膜間皮瘤 | I級推薦 I類證據 |
2 | 納武利尤單抗聯合伊匹木單抗被推薦用於一線治療上皮型胸膜間皮瘤 | II級推薦 2A類證據 | |
3 | 納武利尤單抗單藥或聯合伊匹木單抗被推薦用於二線治療胸膜間皮瘤 | III級推薦 3類證據 | |
4 | 非小細胞肺癌 | 納武利尤單抗聯合伊匹木單抗被推薦用於一線治療無驅動基因突變的非鱗狀/晚期鱗狀非小細胞肺癌患者 | III級推薦 |
5 | 納武利尤單抗聯合伊匹木單抗和2周期培美曲塞+鉑類藥物被推薦用於一線治療無驅動基因突變的非鱗狀/晚期鱗狀非小細胞肺癌患者 | III級推薦 | |
6 | 肝癌 | 納武利尤單抗聯合伊匹木單抗被推薦用於二線治療Child肝功能分級A級或較好B級(≤7分)的晚期肝癌患者 | III級推薦 2A類證據 |
7 | 腎細胞癌 | 納武利尤單抗與伊匹木單抗聯合治療方案被推薦用於轉移性或不可切除性透明細胞型腎細胞癌(中危、高危)患者一線治療 | I級推薦 1A類證據 |
納武利尤單抗與伊匹木單抗聯合治療方案被推薦用於TKI治療失敗的轉移性或不可切除性透明細胞型腎細胞癌患者的二線治療 | III級推薦 2B類證據 | ||
8 | 黑色素瘤 | 納武利尤單抗聯合伊匹木單抗被推薦用於轉移性或不可切除Ⅲ或IV 期的皮膚黑色素瘤的晚期一線治療 | Ⅲ級 2A類證據 |
納武利尤單抗聯合伊匹木單抗被推薦用於轉移性或不可切除Ⅲ或IV 期的肢端黑色素瘤的晚期一線治療 | Ⅲ級 2A類證據 |
