專利背景
鹽酸伊立替康,英文名稱:Irinotecan Hydrochloride Injection,分子式為C 33H38N4O6·HCl·3H2O,分子量為677.19,其化學名稱為(+)-(4S)-4,11-二乙基-4-羥基-9-[(4-哌啶基哌啶)羰基]-1H-吡喃並[3,4:6,7]吲哚嗪[1,2b]喹啉-3,14-(4H,12H)-二酮鹽酸鹽三水合物,室溫下為淡黃色粉末或淡黃色結晶性粉末,無臭,在水、乙醇或氯仿中微溶,在丙酮中不溶。是日本第一製藥和Yakult Honsha公司於1994年開發上市的抗腫瘤藥物,抗癌活性強,以鹽酸鹽的形式存在,結構式如下:
鹽酸伊立替康(CPT-11)是一種半合成的可溶性喜樹鹼類衍生物,主要作用於細胞周期的S期,通過抑制拓撲異構酶I,干擾DNA複製和細胞分裂。在體內經羧酸酯酶的催化作用,代謝成活性產物7-乙基-10-羥基喜樹鹼(SN-38),其抗癌活性為前者的100~1000倍。鹽酸伊立替康注射液是一種有效的、具有代表性的抗腫瘤新藥,作為特異性的拓撲異構酶I(Topo I)抑制劑,與傳統的酶抑制劑不同,它並不阻礙Topo I的結合,而是將這種核酶轉變成對DNA有害的物質,與Topo I酶和DNA形成的複合物牢固結合,特異性抑制DNA重連步驟,引起DNA單鏈斷裂,使DNA產生不可逆損傷,引起細胞死亡。
中國腫瘤引起的死亡率在所有病因中居第2位(約占17.9%),並且發病率呈上升趨勢,其中肺癌、腸癌的發病率較高。鹽酸伊立替康是治療晚期大腸癌的特效藥物,對5-氟尿嘧啶產生耐藥性的病例仍然有效,同時對小細胞和非小細胞肺癌及宮頸癌和卵巢癌亦有療效。該藥已獲得美國FDA和歐盟的共同批准,在全球100多個國家上市,它是美國FDA 40多年來繼5-氟尿嘧啶(5-FU)以來,唯一批准用於晚期大腸癌一線治療的化療藥。
伊立替康與神經肌肉阻滯劑之間的相互作用不可忽視,具有抗膽鹼酯酶活性,可延長湖泊膽鹼的神經肌肉阻滯作用,而非去極化藥物的神經肌肉阻滯作用可能被拮抗。
CN101277694A公開了一種鹽酸伊立替康的新晶型,提供了鹽酸伊立替康的新的晶型及其製備方法,含有所述新的晶型的藥物組合物和利用其治療結腸或直腸轉移癌的方法。
CN101318964A公開了一種鹽酸伊立替康的晶體,該晶型的鹽酸伊立替康具有較好的儲存穩定性,雜質含量少。
2012年3月前的相關技術中,不同晶型的鹽酸伊立替康均帶有3個結晶水,有的通過改變晶型改善了穩定性,有的通過改變晶型改善了水溶性,為了找到一種性能更為優良的鹽酸伊立替康藥物,特提出《一種鹽酸伊立替康化合物及其藥物組合物》。
發明內容
專利目的
《一種鹽酸伊立替康化合物及其藥物組合物》目的在於提供一種鹽酸伊立替康化合物,所提供的鹽酸伊立替康化合物不易稀釋,易於儲存,具有更好的儲存穩定性,雜質含量少,大大提高了用藥安全。
《一種鹽酸伊立替康化合物及其藥物組合物》另一目的在於提供了含有上述鹽酸伊立替康化合物的藥物組合物。
技術方案
一種鹽酸伊立替康,所述鹽酸伊立替康的分子式為C33H38N4O6·HCl·1.5H2O。
《一種鹽酸伊立替康化合物及其藥物組合物》提供的鹽酸伊立替康化合物中,其分子式中只帶有1.5個結晶水,單個分子在堆積結晶的過程中,由於結晶水的減少,其晶體內部結構也發生了變化。2012年3月前的相關技術中鹽酸伊立替康易吸濕,意外發現《一種鹽酸伊立替康化合物及其藥物組合物》所提供的鹽酸伊立替康化合物的特殊結晶形式不易吸濕,具有較強的儲存穩定性。
所述鹽酸伊立替康晶體使用Cu-Kα射線測量得到的X-射線粉末衍射在2θ為9.7度、10.1度、13.1度、13.3度、16.1度、19.0度、20.5度、21.6度、23.4度、28.6度、29.2度、30.7度、33.2度、35.7度處顯示有特徵峰。
所述鹽酸伊立替康的熔點為278-280攝氏度。
所述的鹽酸伊立替康的製備包括:取鹽酸伊立替康原料藥,加入水/乙二醇的混合溶劑,其中水和乙二醇的體積比為2~4:1,攪拌並加熱至40~60攝氏度,再加入活性炭,攪拌吸附,過濾脫碳除菌,得到澄清溶液,將澄清溶液移入反應釜中,於160~180攝氏度下放置24~36小時,均勻降溫至55~75攝氏度,打開反應釜,緩慢滴加丙酮,析晶,緩慢降溫至0~5攝氏度,過濾,用去離子水洗滌,減壓乾燥,即得。
上述製備方法中,所述鹽酸伊立替康的重量與混合溶劑的體積的比例為1克:10~15毫升。
上述製備方法中,所述滴加為在攪拌轉速25~30轉/分鐘下勻速滴加。
上述製備方法中,所述丙酮與混合溶劑的體積比為3~4:1。
所述的加入活性碳除菌為該領域常用技術手段,可以參見任何的脫色處理,該領域技術人員無需付出任何的創造性勞動,即可根據其自身掌握的相關技術進行適當的選擇,並實現《一種鹽酸伊立替康化合物及其藥物組合物》的目的。
為了進一步提高製劑產品質量,《一種鹽酸伊立替康化合物及其藥物組合物》還可優選在脫色後的過濾為使用超濾膜過濾。
《一種鹽酸伊立替康化合物及其藥物組合物》的發明人通過反覆的實驗,最終在改變包括溫度、壓力、pH、溶劑等實驗條件下,以C33H38N4O6·HCl·3H2O為原料得到了C33H38N4O6·HCl·1.5H2O,由於化合物中水分子的位置和環境發生了變化,這一新的鹽酸伊立替康化合物在分子堆積析晶的過程中內部固態結構發生了巨大的變化,發明人通過吸濕性實驗和穩定性實驗得出,該發明提供鹽酸伊立替康不易稀釋,儲存穩定性好。
《一種鹽酸伊立替康化合物及其藥物組合物》還提供了一種含有前面所述的鹽酸伊立替康的藥物組合物。
所述藥物組合物為鹽酸伊立替康注射液,按重量份計,所述鹽酸伊立替康注射液包括鹽酸伊立替康30-100份、山梨糖醇50-250份、乳酸1-5份、注射用水150-2000份。
優選的,按重量份計,所述鹽酸伊立替康注射液包括鹽酸伊立替康40份、山梨糖醇90份、乳酸1.8份、注射用水2000份。
優選的,按重量份計,所述鹽酸伊立替康注射液包括鹽酸伊立替康100份、山梨糖醇225份、乳酸4.5份、注射用水2000份。
所述鹽酸伊立替康注射液的製備方法包括如下步驟:
(1)注射用水製備:將純化水進行多效蒸餾製備無菌注射用水;
(2)配液:將處方量鹽酸伊立替康、山梨糖醇、乳酸混合均勻後,於攪拌下緩緩加入90%的注射用水中,用pH調節劑調節溶液pH值為3.0~4.0,補加剩餘的10%注射用水;
(3)滅菌:攪拌下溶液升溫至117~125攝氏度,停止加熱保溫10~15分鐘,降溫至40~50攝氏度;
(4)脫色:向澄明溶液中加入活性炭,攪拌吸附30分鐘,經脫炭及一次除菌濾器過濾,二次終端除菌濾過濾,所得濾液至藥液瓶內,檢查合格後灌裝,壓塞即得。
上述鹽酸伊立替康注射液的製備方法中,步驟(2)、(3)所述攪拌為轉速100~160轉/分鐘。
上述鹽酸伊立替康注射液的製備方法中,步驟(2)所述注射用水溫度為70~75攝氏度。
上述鹽酸伊立替康注射液的製備方法中,步驟(1)所述多效為3~6效。
上述鹽酸伊立替康注射液的製備方法中,步驟(4)所述脫色中活性碳用量為溶液體積的0.3~0.5%(克/毫升)。
上述鹽酸伊立替康注射液的製備方法中,步驟(4)中所述微孔濾膜孔徑為0.22微米。
《一種鹽酸伊立替康化合物及其藥物組合物》所述的pH調節劑為該領域所公知,該領域技術人員通常知曉pH調節劑的具體種類,譬如無機酸或無機鹼,但該發明優選的為氫氧化鈉、氫氧化鉀或鹽酸中的一種或幾種組合。將藥液的pH調節到3.0~4.0,在這個範圍內鹽酸伊立替康從配製到灌裝整個過程中的都處在一個比較穩定的體系中,這有利於提高了鹽酸伊立替康注射液的穩定性。
《一種鹽酸伊立替康化合物及其藥物組合物》中,對活性炭用量及吸附時間進行了嚴格的控制,活性炭使用得當,既能有效吸附除菌,又能減少活性炭對原料藥的吸附作用,使得所製備的鹽酸伊立替康注射液溶液澄清。
《一種鹽酸伊立替康化合物及其藥物組合物》提供的鹽酸伊立替康注射液的製備工藝簡單可行,重複性好,易實現工業化大生產,節約人力,較短的生產周期、較低的廢品率和更低的人力成本,使生產成本大幅度降低,可以產生可觀的經濟和社會效益,所製得的鹽酸伊立替康注射液澄明度好,雜質含量低,而且對人體副作用和潛在的危害小。
改善效果
(1)《一種鹽酸伊立替康化合物及其藥物組合物》的鹽酸伊立替康不易吸濕,雜質含量少,儲存穩定性好;
(2)《一種鹽酸伊立替康化合物及其藥物組合物》的鹽酸伊立替康安全性能更高。
附圖說明
圖1為《一種鹽酸伊立替康化合物及其藥物組合物》實施例1提供的鹽酸伊立替康的X-粉末衍射圖;
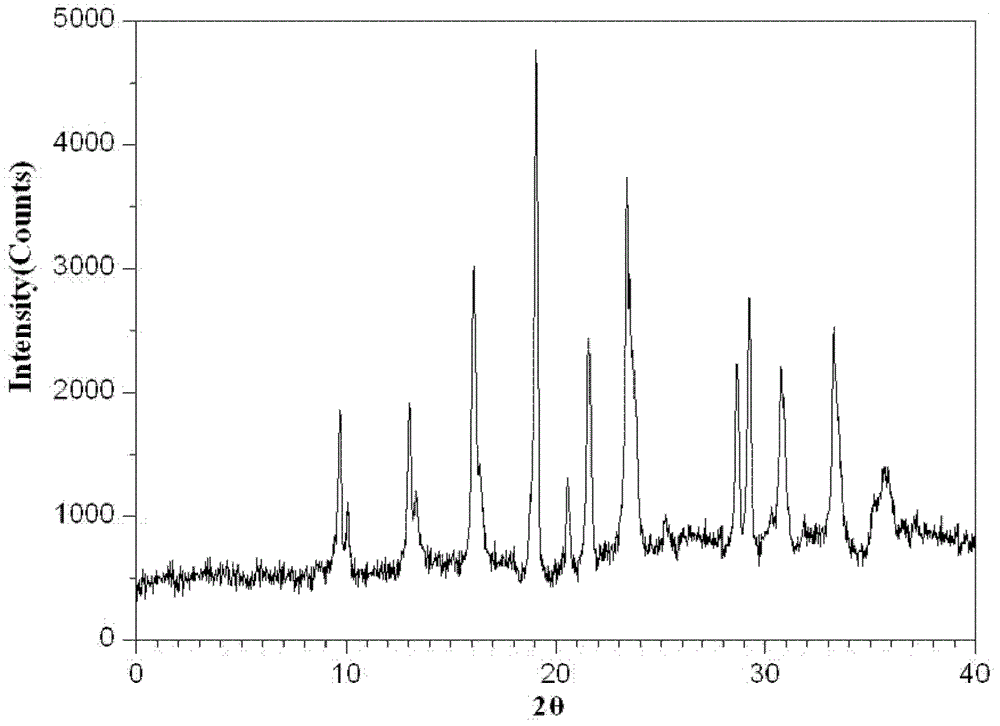
圖1
圖2為《一種鹽酸伊立替康化合物及其藥物組合物》實施例1提供的鹽酸伊立替康的熱重曲線。
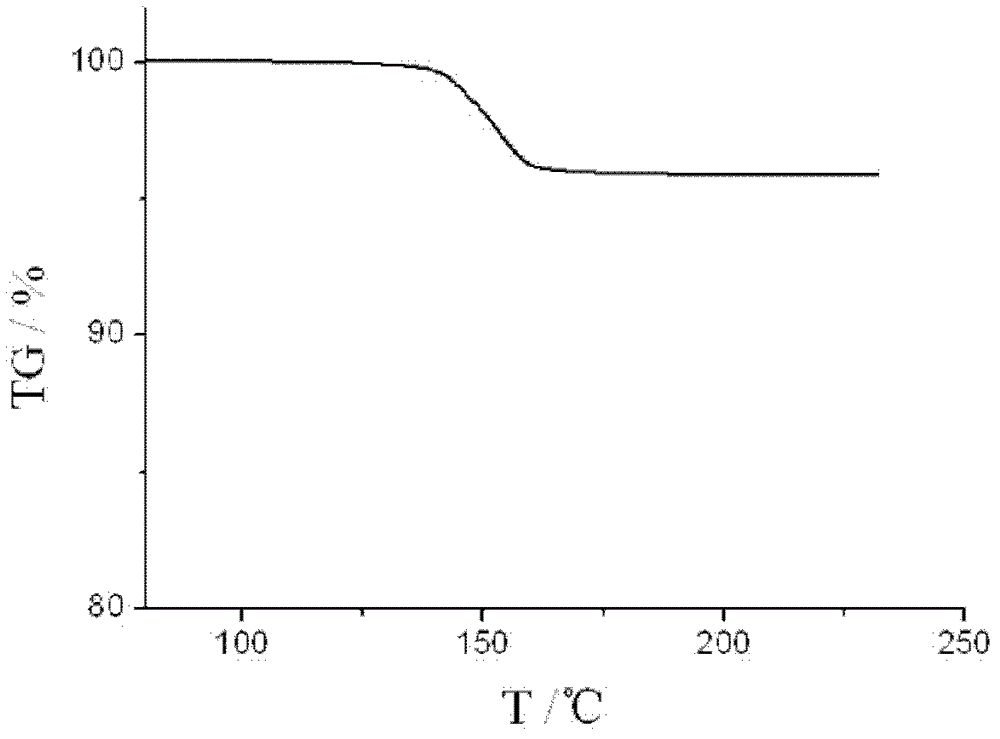
圖2
技術領域
《一種鹽酸伊立替康化合物及其藥物組合物》屬於醫藥技術領域,涉及到一種鹽酸伊立替康化合物及其藥物組合物。
權利要求
1.一種鹽酸伊立替康,其特徵在於,所述鹽酸伊立替康的分子式為C33H38N4O6·HCl·1.5H2O;所述鹽酸伊立替康使用Cu-Kα射線測量得到的X-射線粉末衍射譜圖如圖1所示。
2.一種權利要求1所述的鹽酸伊立替康的製備方法,其特徵在於,所述鹽酸伊立替康的製備包括:取鹽酸伊立替康原料藥,加入水/乙二醇的混合溶劑,其中水和乙二醇的體積比為2~4:1,攪拌並加熱至40~60攝氏度,再加入活性炭,攪拌吸附,過濾脫碳除菌,得到澄清溶液,將澄清溶液移入反應釜中,於160~180攝氏度下放置24~36小時,均勻降溫至55~75攝氏度,打開反應釜,緩慢滴加丙酮,析晶,緩慢降溫至0~5攝氏度,過濾,用去離子水洗滌,減壓乾燥,即得。
3.根據權利要求2所述的鹽酸伊立替康的製備方法,其特徵在於,所述鹽酸伊立替康的重量與混合溶劑的體積的比例為1克:10~15毫升。
4.根據權利要求2所述的鹽酸伊立替康的製備方法,其特徵在於,所述滴加為在攪拌轉速25~30轉/分鐘下勻速滴加。
5.根據權利要求2所述的鹽酸伊立替康的製備方法,其特徵在於,所述丙酮與混合溶劑的體積比為3~4:1。
6.一種含有權利要求1所述的鹽酸伊立替康的藥物組合物。
7.根據權利要求6所述的藥物組合物,其特徵在於,所述藥物組合物為鹽酸伊立替康注射液,按重量份計,所述鹽酸伊立替康注射液的組成為:鹽酸伊立替康30-100份、山梨糖醇50-250份、乳酸1-5份、注射用水150-2000份。
8.根據權利要求7所述的藥物組合物,其特徵在於,按重量份計,所述鹽酸伊立替康注射液的組成為:鹽酸伊立替康40份、山梨糖醇90份、乳酸1.8份、注射用水2000份。
9.根據權利要求7所述的藥物組合物,其特徵在於,按重量份計,所述鹽酸伊立替康注射液的組成為:鹽酸伊立替康100份、山梨糖醇225份、乳酸4.5份、注射用水2000份。
實施方式
取鹽酸伊立替康原料藥50克,加入水/乙二醇的混合溶劑500毫升,其中水和乙二醇的體積比為2:1,攪拌並加熱至40攝氏度,再加入0.15克活性炭,攪拌吸附,過濾脫碳除菌,得到澄清溶液,將澄清溶液移入反應釜中,於160攝氏度下放置24小時,均勻降溫至55攝氏度,打開反應釜,緩慢滴加1500毫升丙酮並以25轉/分鐘的速率進行攪拌,析晶,緩慢降溫至0攝氏度,過濾,用去離子水洗滌3次,減壓乾燥3小時,即得。收率65.4%,HPLC含量99.74%。mp:278-280攝氏度。
得到的鹽酸伊立替康晶體使用Cu-Kα射線測量得到的X-射線粉末衍射在2θ為9.7度、10.1度、13.1度、13.3度、16.1度、19.0度、20.5度、21.6度、23.4度、28.6度、29.2度、30.7度、33.2度、35.7度處顯示有特徵峰。
採用美國Perkin-Elmer公司PE Pyris Diamond TG熱分析儀,熱重分析實驗表明:該實施例1製備的鹽酸伊立替康晶體在137~161攝氏度時失去1.5個H2O分子。
取鹽酸伊立替康原料藥50克,加入水/乙二醇的混合溶劑750毫升,其中水和乙二醇的體積比為4:1,攪拌並加熱至60攝氏度,再加入0.3克活性炭,攪拌吸附,過濾脫碳除菌,得到澄清溶液,將澄清溶液移入反應釜中,於180攝氏度下放置36小時,均勻降溫至75攝氏度,打開反應釜,緩慢滴加3000毫升丙酮並以30轉/分鐘的速率進行攪拌,析晶,緩慢降溫至5攝氏度,過濾,用去離子水洗滌3次,減壓乾燥3小時,即得。收率68.5%,HPLC含量99.79%。mp:278-280攝氏度。
得到的鹽酸伊立替康晶體與實施例1產品的X射線粉末衍射圖譜、熱重曲線具有相同參數。
取鹽酸伊立替康原料藥50克,加入水/乙二醇的混合溶劑600毫升,其中水和乙二醇的體積比為3:1,攪拌並加熱至55攝氏度,再加入0.2克活性炭,攪拌吸附,過濾脫碳除菌,得到澄清溶液,將澄清溶液移入反應釜中,於170攝氏度下放置30小時,均勻降溫至70攝氏度,打開反應釜,緩慢滴加2400毫升丙酮並以30轉/分鐘的速率進行攪拌,析晶,緩慢降溫至0攝氏度,過濾,用去離子水洗滌3次,減壓乾燥3小時,即得。收率68.8%,HPLC含量99.77%。mp:278-280攝氏度。
得到的鹽酸伊立替康晶體與實施例1產品的X射線粉末衍射圖譜、熱重曲線具有相同參數。
將純化水進行3次蒸餾製備無菌注射用水;取實施例1製備的鹽酸伊立替康30克、山梨糖醇50克、乳酸1克混合均勻後,於攪拌下緩緩加入70攝氏度注射用水135毫升,攪拌的轉速為100轉/分鐘,用氫氧化鈉或鹽酸調節溶液pH值為3.0,補加70攝氏度的注射用水15毫升;攪拌下溶液升溫至117攝氏度,攪拌的轉速為100轉/分鐘,停止加熱保溫10分鐘,降溫至40攝氏度;向澄明溶液中加入活性炭0.45克,攪拌吸附30分鐘,攪拌的轉速為100轉/分鐘,經脫炭及一次除菌濾器過濾,二次終端除菌濾過濾,過濾的微孔濾膜孔徑為0.22微米,所得濾液至藥液瓶內,檢查合格後灌裝,壓塞即得。每瓶的裝量為0.4克:2毫升。
將純化水進行6次蒸餾製備無菌注射用水;取實施例2製備的鹽酸伊立替康100克、山梨糖醇250克、乳酸5克混合均勻後,於攪拌下緩緩加入75攝氏度注射用水1800毫升,攪拌的轉速為100轉/分鐘,用氫氧化鈉或鹽酸調節溶液pH值為4.0,補加75攝氏度的注射用水200毫升;攪拌下溶液升溫至125攝氏度,攪拌的轉速為100轉/分鐘,停止加熱保溫15分鐘,降溫至50攝氏度;向澄明溶液中加入活性炭10克,攪拌吸附30分鐘,攪拌的轉速為100轉/分鐘,經脫炭及一次除菌濾器過濾,二次終端除菌濾過濾,過濾的微孔濾膜孔徑為0.22微米,所得濾液至藥液瓶內,檢查合格後灌裝,壓塞即得。每瓶的裝量為0.1克:2毫升。
將純化水進行4次蒸餾製備無菌注射用水;取實施例3製備的鹽酸伊立替康40克、山梨糖醇90克、乳酸1.8克混合均勻後,於攪拌下緩緩加入75攝氏度注射用水1800毫升,攪拌的轉速為160轉/分鐘,用氫氧化鈉或鹽酸調節溶液pH值為4.0,補加75攝氏度的注射用水200毫升;攪拌下溶液升溫至125攝氏度,攪拌的轉速為160轉/分鐘,停止加熱保溫15分鐘,降溫至50攝氏度;向澄明溶液中加入活性炭6克,攪拌吸附30分鐘,攪拌的轉速為160轉/分鐘,經脫炭及一次除菌濾器過濾,二次終端除菌濾過濾,過濾的微孔濾膜孔徑為0.22微米,所得濾液至藥液瓶內,檢查合格後灌裝,壓塞即得。每瓶的裝量為0.1克:5毫升。
將純化水進行4次蒸餾製備無菌注射用水;取實施例3製備的鹽酸伊立替康40克、山梨糖醇90克、乳酸1.8克混合均勻後,於攪拌下緩緩加入75攝氏度注射用水1800毫升,攪拌的轉速為160轉/分鐘,用氫氧化鈉或鹽酸調節溶液pH值為4.0,補加75攝氏度的注射用水200毫升;攪拌下溶液升溫至125攝氏度,攪拌的轉速為160轉/分鐘,停止加熱保溫15分鐘,降溫至50攝氏度;向澄明溶液中加入活性炭6克,攪拌吸附30分鐘,攪拌的轉速為160轉/分鐘,經脫炭及一次除菌濾器過濾,二次終端除菌濾過濾,過濾的微孔濾膜孔徑為0.22微米,所得濾液至藥液瓶內,檢查合格後灌裝,壓塞即得。每瓶的裝量為0.04克:2毫升。
將純化水進行4次蒸餾製備無菌注射用水;取實施例3製備的鹽酸伊立替康100克、山梨糖醇225克、乳酸4.5克混合均勻後,於攪拌下緩緩加入75攝氏度注射用水1800毫升,攪拌的轉速為160轉/分鐘,用氫氧化鈉或鹽酸調節溶液pH值為4.0,補加75攝氏度的注射用水200毫升;攪拌下溶液升溫至125攝氏度,攪拌的轉速為160轉/分鐘,停止加熱保溫15分鐘,降溫至50攝氏度;向澄明溶液中加入活性炭6克,攪拌吸附30分鐘,攪拌的轉速為160轉/分鐘,經脫炭及一次除菌濾器過濾,二次終端除菌濾過濾,過濾的微孔濾膜孔徑為0.22微米,所得濾液至藥液瓶內,檢查合格後灌裝,壓塞即得。每瓶的裝量為0.1克:2毫升。
該試驗例對實施例1~3所製備的鹽酸伊立替康中有關物質進行了檢測,該試驗按照中國藥典2010版第二部附錄VIII P殘留溶劑測定法、附錄XIX F藥品雜質分析指導原則進行,其結果見表1:
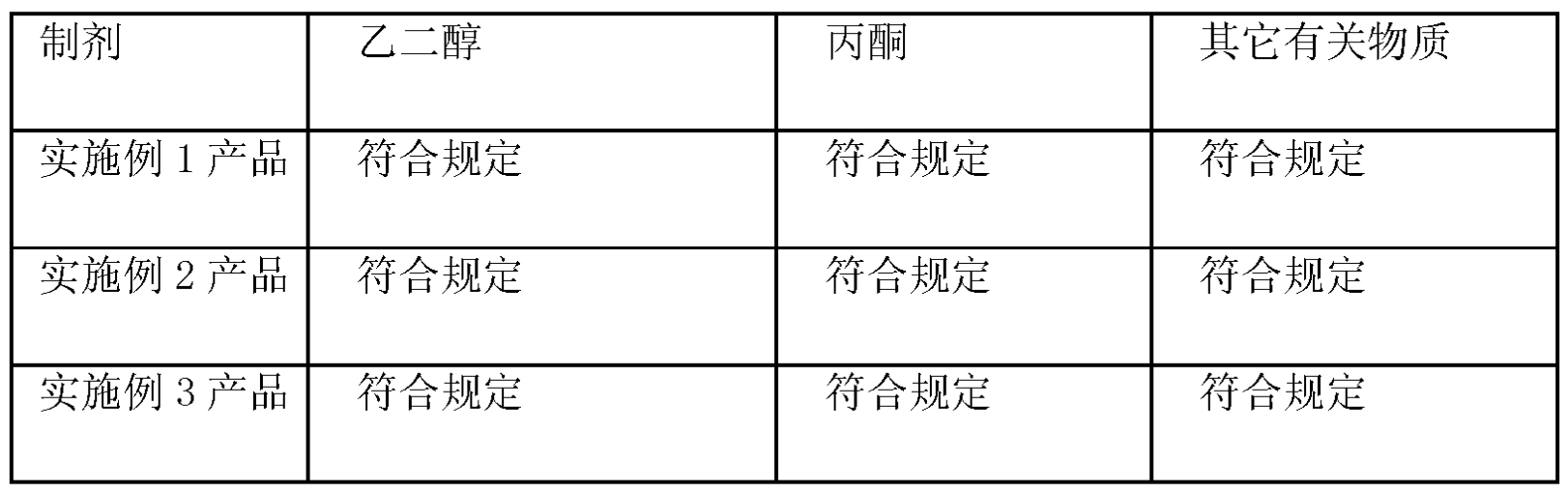
表1 有關物質的檢驗結果
該試驗例考察了《一種鹽酸伊立替康化合物及其藥物組合物》提供的鹽酸伊立替康的吸濕性。
該試驗例分別在濕度80%和90%的條件下,各取樣品1克置於電子天平上,定時記錄重量,以檢測吸濕程度。
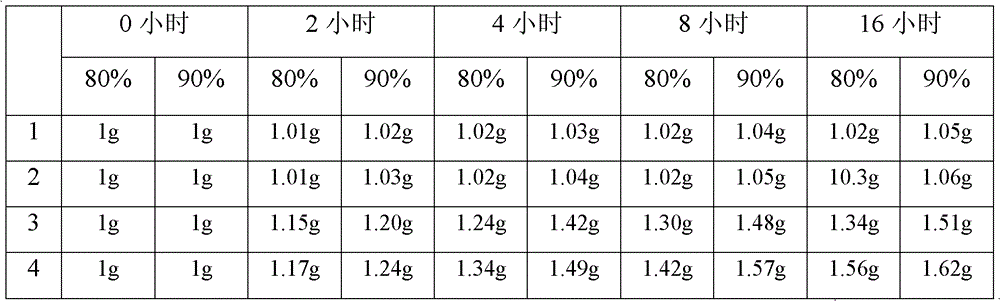
表2 吸濕性試驗結果
其中樣品1為實施例1產品;樣品2為實施例2產品;樣品3為參照CN201110247797.1實施例1製備的鹽酸伊立替康晶體,HPLC含量為99.58%;樣品4為市售鹽酸伊立替康,產自上海雅吉生物科技有限公司,含量為98.8%。
該試驗例還考察了其他實施例製備產品,得出和上表規律相同結果,即《一種鹽酸伊立替康化合物及其藥物組合物》所製備的鹽酸伊立替康吸濕性小。
該試驗例考察了《一種鹽酸伊立替康化合物及其藥物組合物》提供的鹽酸伊立替康的穩定性
該試驗按照中國藥典2005版第二部附錄XIX C藥物穩定性試驗指導原則進行,結果如下:

表3 加速試驗結果
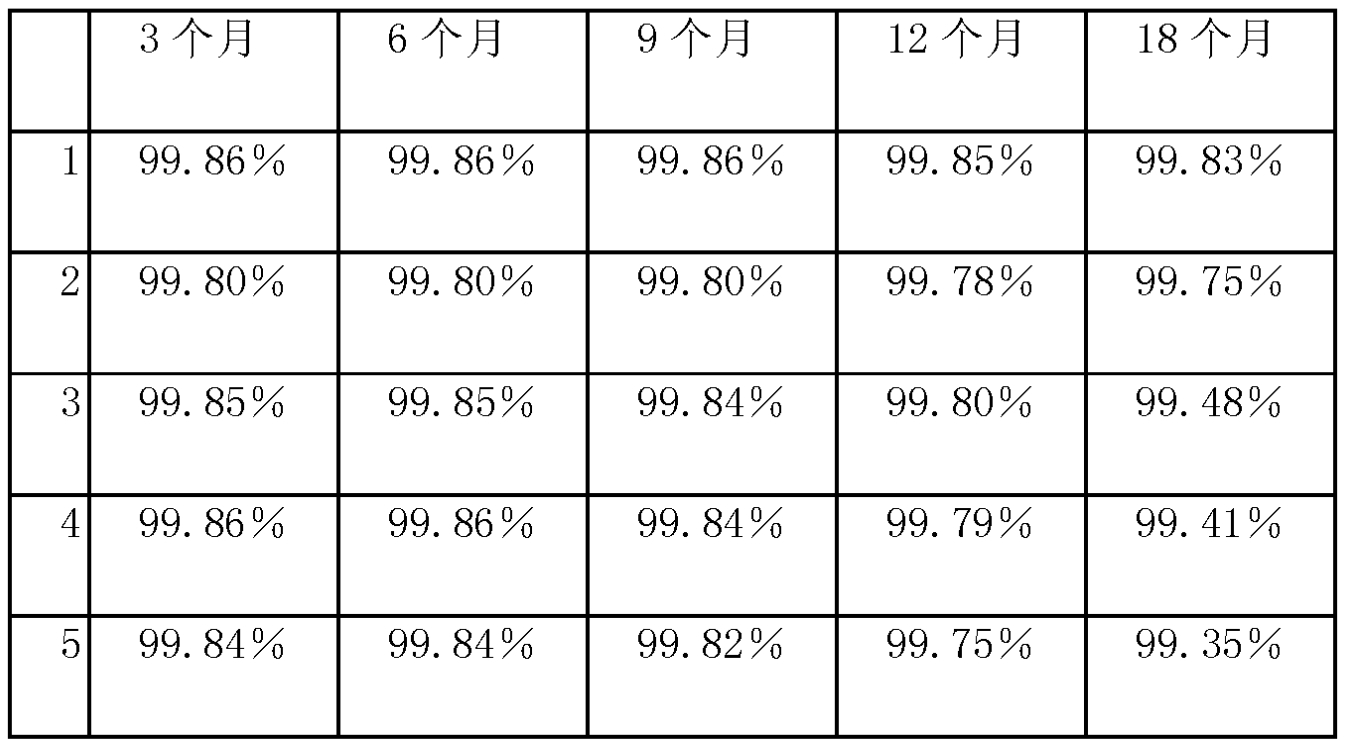
表4 長期試驗結果
其中樣品1為實施例1產品,樣品2為實施例2產品;樣品3為取市售普通鹽酸伊立替康,用水重結晶,反覆重結晶,至HPLC含量與實施例1接近;樣品4為參照CN200710041738.2實施例1製備的鹽酸伊立替康,HPLC含量為99.62%;樣品5為取市售普通鹽酸伊立替康,產自上海雅吉生物科技有限公司,含量為98.8%;該實驗說明,《一種鹽酸伊立替康化合物及其藥物組合物》提供的鹽酸伊立替康穩定性好,加速、長期試驗純度含量變化小。
專利榮譽
2021年6月24日,《一種鹽酸伊立替康化合物及其藥物組合物》獲得第二十二屆中國專利優秀獎。