專利背景
副豬嗜血桿菌(Haempohlius parasuis,HPS)是一種NAD(Nicotinamide adenine dinucleotide,煙醯胺腺嘌呤二核苷酸即輔酶Ⅰ)依賴型、不運動的革蘭氏陰性細小桿菌,屬於巴斯德菌科(Pastteurellacea)嗜血桿菌屬(Haemophilus)。HPS常引起豬的多發性漿膜炎、關節炎以及腦膜炎,由該菌引起的病又稱為豬革拉斯氏病。該菌是在1922年由Schermer和Ehrlich首次分離出來的,但是直到1992才通過SPF(Specific Pathogen Free,無特定病原體)豬證實HPS的致病性以及不同血清型菌株之間的毒力差異。據調查,HPS可以影響從2周齡到4月齡的青年豬,主要在斷奶前後和保育階段發病,通常見於5周齡~8周齡的
豬,發病率可達40%,嚴重時死亡率可達50%。HPS還可感染生產母豬,引起流產、產死胎或弱仔等。隨著養豬業的不斷發展,豬場規模化、集約化程度的不斷提高,豬群飼養密度越來越大,副豬嗜血桿菌感染有明顯增加趨勢,已成為豬場保育豬發病和死亡的一個重要原因。另外,一些免疫抑制性疾病如豬繁殖與呼吸綜合徵、豬圓環病毒病等經常與HPS混合感染或繼發感染,對全球的養豬業造成巨大的經濟損失,也給副豬嗜血桿菌病的診斷和綜合防治帶來更多的難度。
截至2011年11月,副豬嗜血桿菌病已在中國普遍流行,在中國的主要養豬區域如
廣東、河南、
湖北、
湖南、山東、江西、河北、上海、吉林、四川、浙江、甘肅、江蘇等省份都有副豬嗜血桿菌病發生以及HPS分離鑑定的報導。而HPS的真實發病率可能為實際確診的10倍之多,給中國的養豬業帶來了極大的威脅,已經引起了政府和社會上的高度重視。
由於HPS耐藥性現象越來越常見,常用的抗生素對副豬嗜血桿菌病已無明顯的療效,而且隨著人們對綠色食品需求的期望越來越高,抗生素在本病預防和控制等方面的套用必將受到嚴格限制和逐步禁止,疫苗免疫成為預防和控制副豬嗜血桿菌病的主要措施。由於HPS血清型較多,且不同血清型的菌株,其毒力與致病力差異較大,各個血清型之間免疫交叉保護力很低,不同地方分離的菌株具有較強的地方性特徵,致使2011年前中國國內外的副豬嗜血桿菌商品化疫苗不能對該病提供完全有效的免疫保護。因此發掘更多的交叉保護性好且免疫原性強的HPS並利用其研製高效的副豬嗜血桿菌疫苗是該病防控的迫切需要。
Bak、Riising於2002年在《Veterinary record》上報導了一種血清5型副豬嗜血桿菌滅活疫苗,並評估了免疫豬群對同源和異源副豬嗜血桿菌(H.parasuis)進行實驗感染後其保護性免疫的形成。5~7周齡的豬群免疫2周后,同源攻毒(血清5型非疫苗株)的保護率可達到80%(4/5);血清1型副豬嗜血桿菌攻毒的保護率可達40%(2/5);血清12型副豬嗜血桿菌攻毒的保護率可達100%(5/5);血清13型副豬嗜血桿菌攻毒的保護率可達75%(3/4);血清14型副豬嗜血桿菌攻毒的保護率可達100%(5/5)。可見,該血清5型副豬嗜血桿菌滅活疫苗不僅可保護同源攻毒,還可為異源攻毒(血清1、12、13和14)提供部分保護。
發明內容
專利目的
為了解決2011年前中國國內外的副豬嗜血桿菌商品化疫苗各個血清型之間免疫交叉保護力低、免疫原性不強的問題,《一種副豬嗜血桿菌LC株及其套用》提供了一種免疫原性強的副豬嗜血桿菌LC株。該發明還提供了所述副豬嗜血桿菌LC株在製備各個血清型之間免疫交叉保護力強的滅活疫苗中的套用。
技術方案
《一種副豬嗜血桿菌LC株及其套用》是通過以下措施實現的:
一種副豬嗜血桿菌(Haemophilus parasuis)LC株,其保藏編號為CGMCCNo.5257。
所述的副豬嗜血桿菌(Haemophilus parasuis)LC株在製備副豬嗜血桿菌滅活疫苗中的套用。
優選所述副豬嗜血桿菌滅活疫苗為油乳劑疫苗或鋁膠疫苗。
優選所述副豬嗜血桿菌滅活疫苗為鋁膠疫苗。
所述鋁膠疫苗中含菌量≥2.5×10個菌群/毫升。
有益效果
《一種副豬嗜血桿菌LC株及其套用》的副豬嗜血桿菌LC株對豬有較強的致病性,且具有良好的免疫原性,套用其製備的滅活鋁膠疫苗安全可靠,不僅能提供同源攻毒保護,還可為血清4型、5型、10型、12型、14型和15型HPS等異源攻毒提供一定的交叉保護,免疫後能夠產生較強免疫力,接種豬群的發病率和死亡率均明顯減少,其免疫效果達到或優於市場上2011年前的商品化疫苗,具備了與中國國內外同類產品競爭的優勢,能夠有效預防副豬嗜血桿菌病的流行和傳播,降低本病造成的經濟損失,有著廣闊的套用前景。
菌株保藏信息
保藏時間:2011年9月17日;
保藏單位:中國微生物菌株保藏管理委員會普通微生物中心(CGMCC);
保藏編號:CGMCCNo.5257;
保藏單位地址:北京市朝陽區北辰西路1號院3號中國科學院微生物研究所;
分類命名:副豬嗜血桿菌(Haempohliusparasuis)。
附圖說明
附圖1為攻毒試驗中腹腔注射不同劑量LC株菌液後仔豬體溫變化狀況。
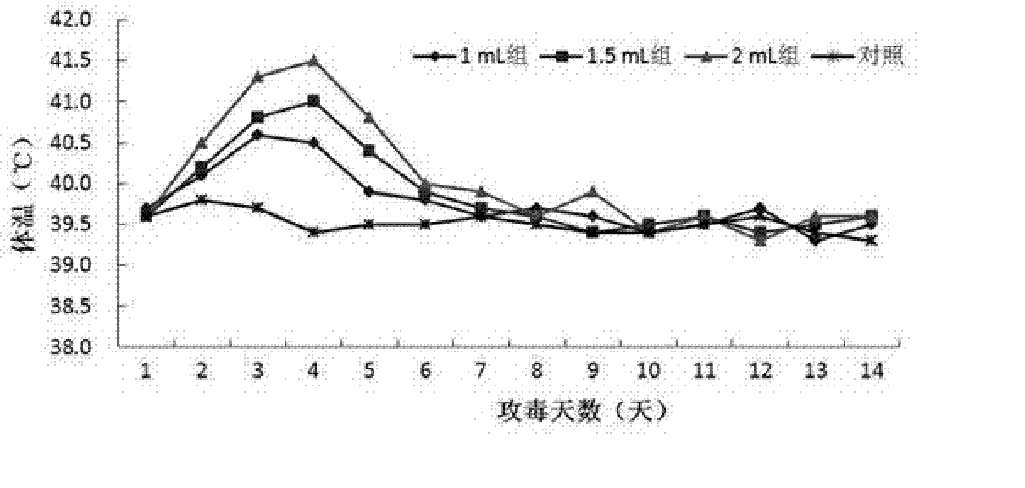
圖1
技術領域
《一種副豬嗜血桿菌LC株及其套用》涉及獸醫生物製品中副豬嗜血桿菌疫苗領域,特別涉及一種副豬嗜血桿菌LC株,還涉及所述副豬嗜血桿菌LC株的套用。
權利要求
1.一種副豬嗜血桿菌(Haemophilus parasuis)LC株,其特徵在於其保藏編號為CGMCCNo.5257。
2.權利要求1所述的副豬嗜血桿菌(Haemophilus parasuis)LC株在製備副豬嗜血桿菌滅活疫苗中的套用。
3.根據權利要求2所述的套用,其特徵在於所述副豬嗜血桿菌滅活疫苗為油乳劑疫苗或鋁膠疫苗。
4.根據權利要求2或3所述的套用,其特徵在於所述副豬嗜血桿菌滅活疫苗為鋁膠疫苗。
5.根據權利要求4所述的套用,其特徵在於所述鋁膠疫苗中含菌量≥2.5×10個菌群/毫升。
實施方式
副豬嗜血桿菌(Haemophilus parasuis)LC株,其在中國微生物菌種保藏管理委員會普通微生物中心的保藏號為CGMCCNo.5257。
生產用培養基
TSA培養基配製:稱取4克TSA粉末加入100毫升蒸餾水中,充分混勻後,121℃滅菌15分鐘,冷卻至50℃~60℃時,加入終濃度0.001%NAD和5%新生牛血清,混合均勻後傾倒平板備用。
TSB培養基配製:稱取3克TSB粉末加入100毫升蒸餾水中,121℃滅菌15分鐘。臨用前加入終濃度0.001%NAD和5%新生牛血清,混合均勻後配製而成。
1.1HPS菌株的分離純化方法
從山東省聊城疑似副豬嗜血桿菌病的某大型養豬場選取病豬,無菌採集病豬的心包積液、胸腔積液、關節液和心血劃線接種於含0.001%NAD(Nicotinamide adenine dinucleotide,煙醯胺腺嘌呤二核苷酸即輔酶Ⅰ)和5%新生牛血清的TSA(Tryptic SoyAgar,胰蛋白腖大豆瓊脂)
培養基上,置於37℃培養箱培養36小時~72小時,挑取圓形、光滑濕潤、無色透明的露珠狀小菌落革蘭氏染色鏡檢,選取革蘭氏陰性細小桿菌進行劃線純培養。
將純培養菌株分別劃線接種於鮮血瓊脂平板和普通瓊脂平板,同時水平劃線接種鮮血瓊脂平板後,再挑取金黃色葡萄球菌垂直於水平線劃線,37℃培養24小時~48小時,選取在鮮血瓊脂平板和普通瓊脂平板上不生長,但與金黃色葡萄球菌在鮮血瓊脂平板上共同培養時呈現明顯的“衛星生長現象”且不溶血的微小菌落進行純化培養。
將進一步純化培養的兩株菌株,分別接種於含NAD的微量生化反應管,37℃培養48小時,結果均為硝酸鹽還原試驗陽性,吲哚試驗陰性,脲酶試驗陰性,氧化酶試驗陰性,接觸酶試驗陽性,發酵葡萄糖、蔗糖和果糖,不發酵麥芽糖、半乳糖、木糖和甘露醇。該菌株根據其病豬的來源地命名為LC株。
1.216SrRNA基因序列測定與分析
1.2.1引物設計:根據HPS16SrRNA(GenBank No:M75065)序列設計引物,上游引物:5’-GTGATGAGGAAGGGTGGTGT-3’,下游引物:5’-GGCTTCGTCACCCTCTGT-3’,該引物擴增編碼16SrRNA長度約為822bp的特異片段,引物由上海生物工程有限公司合成。
1.2.2細菌DNA模板的製備:將被檢菌株菌液5000轉每分離心5分鐘,棄上清液,用無菌水重懸後,於沸水中煮沸10分鐘,-20℃凍結、融化後,10000轉每分離心5分鐘,取上清液作模板進行PCR擴增。
1.2.3PCR擴增:將細菌DNA模板3微升、10倍PCR緩衝液2.5微升、dNTP(10毫摩爾/升)0.5微升、引物各1微升(10微摩爾/升)和TaqDNA聚合酶0.25微升(5U/微升)混合,加水至25微升,94℃預變性5分鐘,94℃變性30s、58℃退火30秒、72℃延伸1分鐘,循環34次,最後72℃延伸10分鐘,PCR產物於1%瓊脂糖凝膠電泳,可觀察到822bp大小的特異DNA條帶。用DNA快速回收試劑盒回收PCR產物,-20℃保存備用。
1.2.416SrRNA擴增產物的克隆與測序:將回收的PCR產物與pMD19-T在16℃連線30分鐘,轉化DH5α感受態細菌,37℃過夜培養12小時~16小時。挑取平板上的單菌落於氨苄青黴素抗性的LB液體培養基中37℃過夜振盪培養,次日套用菌液PCR的方法擴增16SrRNA基因篩選陽性克隆,鑑定為陽性的菌液提取質粒交由上海生工公司測序。LC株16SrRNA基因的核苷酸序列如序列表中序列1所示,將序列在GenBank中進行BLAST比對,與已發布的副豬嗜血桿菌相應序列的同源性達到98.5%以上。
1.3HPSLC株的血清學鑑定
將LC株分別密集劃線接種於TSA培養基,37℃培養20小時~24小時後,用PBS(磷酸鹽緩衝液)洗下菌落,將懸液稀釋至含菌量為3.0×l0個菌群/毫升,121℃高壓2小時,菌液7000轉每分離心10分鐘,取上清用於瓊脂擴散試驗的分型抗原。用生理鹽水配製1%的瓊脂糖凝膠,根據需要在相應的瓊脂糖凝膠孔中加抗原和相應的抗血清,以剛加滿孔為宜,濕盒內37℃下放置24小時~48小時,可見LC株於1型血清孔與抗原孔之間出現清晰的白色沉澱線,故判定副豬嗜血桿菌LC株為血清1型。
1.4動物攻毒試驗
1.4.1攻毒菌液的製備:分別挑取HPSLC株單菌落密集劃線接種於TSA培養基,37℃培養12小時~16小時後,用PBS收穫細菌。將菌液塗布於TSA培養基,37℃培養20小時後,用PBS收穫細菌,並將菌液的活菌數調整為3.0×10個菌群/毫升。
1.4.2動物攻毒試驗結果:取3周齡~4周齡健康易感仔豬40頭,隨機分成4組,每組10頭,其中3組分別以1毫升、1.5毫升和2毫升三個不同劑量進行腹腔注射LC株菌液(3.0×109個菌群/毫升),另外1組注射滅菌生理鹽水2毫升作為對照。攻毒組大部分仔豬的體溫在攻毒第二天或第三天開始升高,持續三四天后,體溫逐漸恢復正常,如圖1所示;其還出現被毛粗亂、精神沉鬱、食慾減退、呼吸困難、關節腫大、跛行、甚至死亡等臨床症狀;剖檢可觀察到:其胸腹腔積液增多、胸腹腔內粘連甚至出現纖維素性滲出物、心包積液增多甚至心包膜增厚有纖維素滲出物、全身淋巴結腫大、或後肢關節腔內關節液增多甚至有膠凍樣滲出物。LC株的攻毒劑量越大,試驗豬的最高體溫越高,死亡越快,其發病率和死亡率越大。攻毒組仔豬的發病率和死亡率如表1所示。對照組仔豬的體溫無明顯變化,亦無發病和死亡。由於用1.5毫升菌液(3.0×10個菌群/毫升)攻毒可使仔豬發病率達到80%,所以後面的LC株攻毒試驗選用1.5毫升劑量。
1.5免疫原性的測定
1.5.1取3周齡~4周齡健康易感仔豬40頭,隨機分成4組,每組10頭。LC株菌種擴增培養物分別製成含菌量為2×10個菌群/毫升、2.5×10個菌群/毫升和3×10個菌群/毫升的滅活鋁膠疫苗(疫苗的配製和成品檢驗方法參照實施例2)。其中3組仔豬分別頸部肌肉注射上述三種疫苗,2毫升/頭,2周后按相同劑量進行二免,另外1組仔豬作為未免疫對照組。二免後2周採血通過玻片凝聚法檢測仔豬的血清抗體效價,採血後4組仔豬均腹腔注射LC株菌液(3.0×10個菌群/毫升)1.5毫升/頭。未免疫對照組仔豬的抗體為陰性,攻毒後有9頭仔豬發病,其中3頭死亡。而免疫組中,除最低劑量組(含菌量為2×10個菌群/毫升)免疫效果較差外,其餘兩組(含菌量為2.5×10個菌群/毫升和3×10個菌群/毫升)均產生較好的免疫效果,仔豬抗體效價均在1:32以上,攻毒後仔豬均健活,剖檢無明顯病理變化,詳細結果如表2所示。
1.5.2含菌量為2×10、2.5×10、3×10個菌群/毫升的LC株滅活鋁膠疫苗,分別頸部肌肉注射妊娠70天的健康母豬5頭,2毫升/頭,2周后按相同劑量進行二免,同時設未免疫對照母豬5頭。二免後2周採血通過玻片凝聚法檢測母豬的血清抗體效價,採血後4組母豬均腹腔注射LC株菌液(3.0×10個菌群/毫升)1.5毫升/頭,觀察攻毒母豬的臨床症狀和產仔狀況。不同含菌量的滅活鋁膠疫苗對懷孕母豬的免疫效果如表3所示。未免疫對照組母豬的抗體為陰性,攻毒後則表現食慾減退和發熱,有的母豬發生流產、早產或產死胎、木乃伊胎,部分死亡胎兒或弱仔的臍帶出血。含菌量為2.5×10個菌群/毫升的疫苗免疫組中,有1頭母豬攻毒後食慾下降、體溫升高(約40.0~41.0℃),並發生早產,其他母豬產仔均正常,保護率可達到80%;含菌量為3×10個菌群/毫升的疫苗免疫組保護率達100%。
上述試驗證明HPSLC株具有良好的免疫原性,其最低免疫劑量為2毫升含菌量為2.5×10個菌群/毫升的滅活疫苗。
副豬嗜血桿菌(Haemophilus parasuis)LC株在製備的副豬嗜血桿菌滅活疫苗中的套用。
取菌種保藏編號為CGMCCNo.5257的副豬嗜血桿菌(Haemophilus parasuis)LC株,活化後分別接種培養基,培養後收集菌液,經甲醛溶液滅活,與氫氧化鋁膠佐劑混合配製成滅活鋁膠疫苗。
優選操作步驟如下:
2.1菌種選擇
制苗用菌種為HPSLC株,其保藏編號為CGMCCNo.5257,其菌落形態、菌體特徵、生化特性、培養特性均穩定,對豬有較強的致病性,1.5毫升菌液(3.0×10個菌群/毫升)腹腔注射仔豬即可導致80%的仔豬發病。HPSLC株的免疫原性良好,最低免疫劑量應≥5.0×10CFU。
2.2生產用菌種製備
2.2.1一級生產種子繁殖:取菌種保藏編號為CGMCCNo.5257的HPSLC株,將其劃線接種於TSA培養基,37℃培養24小時,取活化後的HPSLC株單菌落密集劃線接種於TSA培養基,37℃培養16小時~20小時後,用PBS沖洗,收集菌液,並將菌液的活菌數調整為3.0×10個菌群/毫升。經純粹檢驗合格後,作為一級生產種子。
2.2.2二級生產種子繁殖:取一級生產種子按1%劑量接種於TSB培養基中,37℃180轉每分振盪培養12小時~14小時,該菌液經純粹檢驗合格後,作為二級生產種子。在2~8℃保存,不得超過6小時~8小時。
2.3制苗菌液製備
將二級種子液按照培養基量的1%接種於盛有TSB培養基的玻璃瓶或培養罐中,小量通氣,37℃培養20小時,收穫並取樣進行純粹檢驗和活菌計數。純粹檢驗和活菌計數均按現行《中華人民共和國獸藥典》附錄進行。每批制苗用菌液均純粹,無雜菌生長,且其活菌數為2.5×10個菌群/毫升。
2.4菌液的滅活
向菌液中分別加入終濃度為0.1%、0.2%、0.3%、0.4%的甲醛溶液,將其置於37℃滅活,期間每隔4小時~6小時振搖一次。滅活6小時、12小時、18小時、24小時、30小時、36小時、42小時和48小時時取樣檢測,觀察是否滅活完全。三組平行試驗的結果均顯示0.3%和0.4%甲醛溶液滅活HPS菌液24小時時均未檢出活菌,如表4所示。因此,菌液的滅活方法選用終濃度為0.3%甲醛溶液37℃滅活24小時,期間每隔4小時~6小時振搖一次。滅活菌液經檢驗無菌生長為合格,以該滅活菌液作為制苗用抗原。
註:“+”存在活菌;“-”無活菌。
2.5免疫佐劑的篩選
2.5.1油苗的製備:將滅活的菌液濃縮3倍,取濃縮菌液96份加入4份吐溫混勻作為水相,取白油93份加入司本-806份,硬脂酸鋁1份混合,121℃滅菌30分鐘後作為油相。按水相與油相1:2的比例進行乳化製備油乳劑滅活疫苗。成品疫苗中含菌量2.5×10個菌群/毫升。將疫苗取樣進行無菌檢驗,按現行《中華人民共和國獸藥典》方法進行,無細菌、黴菌生長。
2.5.2鋁膠疫苗的製備:取20克鋁膠加入100毫升水中,攪拌至完全溶解,121℃高壓滅菌1小時配製成20%的鋁膠,按體積比1:2加入滅活菌液中,混勻後,2~8℃靜置2天~3天,抽棄上清約濃縮成全量的三分之二,分裝保存。成品疫苗中含菌量2.5×10個菌群/毫升。將疫苗取樣進行無菌檢驗,按現行《中華人民共和國獸藥典》方法進行,無細菌、黴菌生長。
2.5.3安全檢驗:將15頭3周齡~4周齡健康易感仔豬隨機分成3組,5頭/組。其中2組分別按2毫升/頭接種鋁膠佐劑滅活疫苗和油佐劑滅活疫苗,14天后二免,對照組仔豬不免疫。連續觀察2周,結果免疫後絕大部分豬的精神、體溫、食慾均正常,但油苗組注射部位到試驗結束仍稍有腫脹,疫苗吸收不良,鋁膠苗組無腫脹和壞死,無其他不良反應。
2.5.4效力檢驗:將21日齡健康易感仔豬15頭分成3組,其中2組分別肌肉注射油苗和鋁膠苗2毫升/頭,間隔2周后以同樣劑量加強免疫1次,另外1組仔豬不免疫作為對照。再間隔2周后,三組仔豬均腹腔注射1.5毫升LC株菌液(3.0×10個菌群/毫升),連續觀察2周,記錄體溫變化和臨床表現,剖檢後觀察病理變化。
油苗組:2頭仔豬攻毒後食欲不振,精神沉鬱,體溫升高(>40.5℃),其中1頭於攻毒後第7天死亡,剖解後發現腹膜炎,另外3頭體溫變化不大,食慾正常,剖檢後無典型變化。該組疫苗的保護率為60%。
鋁膠苗組:5頭仔豬體溫、食慾均無異常,剖檢後僅有1頭出現輕微腹膜炎,其他仔豬均無異常病變。該組疫苗的保護率為80%。
對照組:5頭仔豬體溫均升高(>40.5℃),其中1頭於攻毒後第10天死亡,解剖後僅見腹膜炎;另外3頭於攻毒後精神沉鬱、呼吸困難、臥地不起,於攻毒後第14天剖解後發現腹水增多且渾濁、胸腔內有粘連、嚴重者有纖維素性滲出,另外1頭無明顯異常病變。
綜上所述,油苗和鋁膠苗均能為仔豬提供保護,但鋁膠苗的保護效果要強於油苗,因此,選用鋁膠作為疫苗佐劑。
2.6滅活鋁膠疫苗的配製
2.6.120%鋁膠的製備:取20克鋁膠加入100毫升水中,攪拌至完全溶解,121℃高壓滅菌1小時後備用。
2.6.2配苗與分裝
抗原檢驗合格後,按菌液2份加20%鋁膠1份進行配苗。同時,按疫苗總量的0.005%加入硫柳汞,充分振盪後2~8℃靜置2天~3天,抽棄上清濃縮成全量的三分之二。混勻後定量分裝,分裝過程中要隨時攪拌使其混合均勻。
2.7滅活鋁膠疫苗成品檢驗
2.7.1物理性狀測定:本品靜置後,上層為透明清亮液體,下層為灰白色沉澱,充分振搖後,呈均勻混懸液。
2.7.2無菌檢驗:按現行《中華人民共和國獸藥典》附錄進行檢驗,無菌生長。
2.7.3甲醛、硫柳汞含量測定:分別按現行《中華人民共和國獸藥典》附錄進行測定,不同批次疫苗甲醛含量為0.09~0.14%,硫柳汞含量為0.003~0.004%,符合規定。
2.7.4安全檢驗:選取3周齡~4周齡健康易感仔豬5頭,各頸部肌肉注射疫苗4毫升,觀察2周,接種仔豬體溫、精神和食慾均正常,全部健活,且注苗局部無腫脹和壞死。
2.7.5效力檢驗:取3周齡~4周齡健康易感仔豬10頭,分為2組,5頭/組。其中1組仔豬頸部肌肉注射2毫升HPS滅活鋁膠疫苗,間隔2周以相同劑量加強免疫一次,另外1組仔豬不免疫作為對照。2周后採血,分離血清,測定血清抗體效價。採血後用HPSLC株進行攻毒,每頭仔豬腹腔注射1.5毫升菌液(細菌含量3.0×10個菌群/毫升),觀察2周。免疫組仔豬抗體幾何平均效價≥1:32,對照組仔豬的抗體幾何平均效價≤1:4。攻毒後,對照仔豬至少4頭髮病或死亡,免疫仔豬至少保護4頭。
2.7.6交叉保護檢驗
選取HPS血清4、5、10、12、13、14和15型7個HPS分離株分別製備攻毒菌液,評估HPSLC株滅活鋁膠疫苗對異源血清型的交叉保護作用。
每株HPS分離株的交叉保護檢驗方法:
隨機選取3周齡~4周齡健康易感仔豬20頭,分為2組,每組10頭,1組頸部肌肉注射HPSLC株滅活疫苗2毫升/頭,間隔2周后以同樣劑量加強免疫1次,另一組仔豬不免疫作為對照組。2周后,腹腔注射HPS分離株菌液進行攻毒,每株HPS分離株的攻毒劑量見表5,連續觀察2周。
HPSLC株滅活疫苗對異源血清型的交叉保護如表5所示。
由上表可以看出,HPSLC株滅活鋁膠疫苗對血清5型和10型HPS的交叉保護率可達到80%,對血清4型、12型和15型HPS的交叉保護率可達到70%,對血清14型HPS的交叉保護率可達到60%,交叉保護率比較高,是一種具有廣闊市場套用前景的疫苗,值得推廣。限於實驗條件及原材料的限制,僅做了上述HPS血清4、5、10、12、13、14和15型7個HPS分離株的交叉保護實驗,對HPS其它血清型的交叉保護性能的研究有待於以後的進一步研究。
榮譽表彰
2016年12月7日,《一種副豬嗜血桿菌LC株及其套用》獲得第十八屆中國專利優秀獎。


