《一種三酮類化合物的合成方法》是浙江工業大學於2009年12月12日申請的專利,該專利的公布號為CN101735119A,授權公布日為2010年6月16日,發明人是杜曉華、駱大為、徐振元。
《一種三酮類化合物的合成方法》公開了一種如式(I)所示的三酮類化合物的合成方法,式(I)中,X為Cl或NO2。所述合成方法為:在有機溶劑中,式(II)所示的烯醇酯在鹼性試劑和重排催化劑的作用下發生重排反應,反應完畢後所得反應液經酸化、分離得到所述的三酮類化合物;所述的重排催化劑為嘌呤類化合物。該發明的三酮類化合物(磺草酮、硝草酮)合成方法,所用的催化劑毒性小,對環境友好,產品收率較高,適宜工業化生產。
2018年12月20日,《一種三酮類化合物的合成方法》獲得第二十屆中國專利獎優秀獎。
基本介紹
- 中文名:一種三酮類化合物的合成方法
- 公告號:CN101735119A
- 授權日:2010年6月16日
- 申請號:2009101554704
- 申請日:2009年12月12日
- 申請人:浙江工業大學
- 地址:浙江省杭州市下城區朝暉六區
- 發明人:杜曉華、駱大為、徐振元
- Int.Cl.:C07C317/24(2006.01)I; C07C315/04(2006.01)I
- 代理機構:杭州天正專利事務所有限公司
- 代理人:黃美娟、王兵
- 類別:發明專利
專利背景,發明內容,專利目的,技術方案,改善效果,技術領域,權利要求,實施方式,榮譽表彰,
專利背景
三酮類除草劑(磺草酮、硝草酮)主要用於防除玉米等作物田間的闊葉雜草和禾本科雜草,具有除草譜廣、環境相容性好、對哺乳動物和水生生物毒性很低、對後茬輪作作物無藥害等特性。
截至2009年12月12日,已有的合成方法主要是以相應的烯醇酯為起始原料,在鹼性條件下,經由重排試劑的重排作用來製備磺草酮和硝草酮。例如美國專利(US4762551、US4775411和US20030232984)報導了以三乙胺為鹼性試劑,相應的烯醇酯在丙酮氰醇的作用下,重排生成磺草酮和硝草酮。該路線的缺點主要是重排試劑丙酮氰醇劇毒。美國專利(US5886231)報導了以碳酸鈉為鹼性試劑,相應的烯醇酯在氰化鈉的作用下,重排生成磺草酮和硝草酮。該路線的缺點也主要是重排試劑氰化鈉劇毒。此外,美國專利(US6218579)報導了以碳酸鉀為鹼性試劑,相應的烯醇酯在三氮唑的作用下,重排生成磺草酮和硝草酮。該路線的缺點主要是重排反應不完全且反應時間長。
發明內容
專利目的
《一種三酮類化合物的合成方法》要解決的技術問題是提供一種對環境友好、產品收率較高、適宜工業化生產的三酮類化合物(磺草酮、硝草酮)的合成方法。
技術方案
《一種三酮類化合物的合成方法》採用的技術方案如下:
一種如式(I)所示的三酮類化合物的合成方法,其特徵在於所述合成方法為:在有機溶劑中,式(II)所示的烯醇酯在鹼性試劑和重排催化劑的作用下發生重排反應,反應完畢後所得反應液經酸化、分離得到所述的三酮類化合物;所述的重排催化劑為嘌呤類化合物;
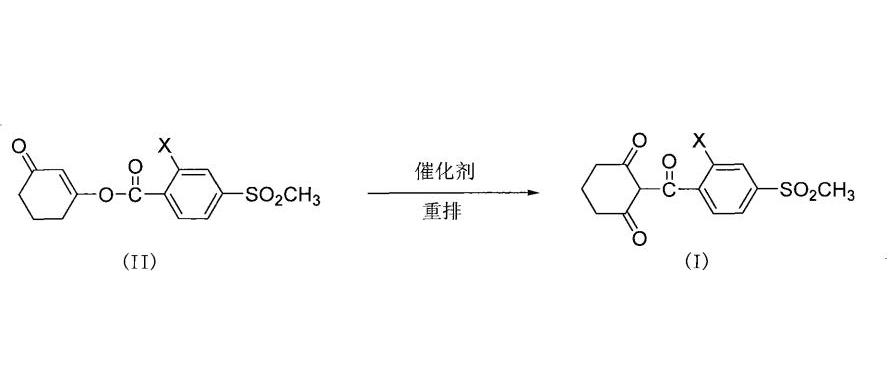
式(I)或式(II)中,X為Cl或NO2。
《一種三酮類化合物的合成方法》所述的重排催化劑的加入摩爾數優選為烯醇酯摩爾數的1~5%。所述的重排催化劑優選為嘌呤、6-氯嘌呤或6-羥基嘌呤,更優選為6-氯嘌呤。
《一種三酮類化合物的合成方法》所述的有機溶劑可選自下列之一:1,2-二氯乙烷、氯代苯、氯仿、二氯甲烷、三氟甲苯、鄰氯甲苯、間氯甲苯、對氯甲苯、乙腈、甲苯、乙酸乙酯。所述的有機溶劑的體積用量推薦為1~5升/摩爾烯醇酯。
《一種三酮類化合物的合成方法》所述的重排反應的溫度為20~80℃,以30~50℃為佳。
所述的重排反應的時間跟溫度有關,溫度低,反應時間長,溫度高,反應時間短,通常為2~5小時。
《一種三酮類化合物的合成方法》在重排反應結束後,優選使用鹽酸進行酸化,鹽酸質量濃度可在5~37%。
《一種三酮類化合物的合成方法》具體推薦所述的酸化、分離為:重排反應完成後,加入質量濃度為5~37%的鹽酸將反應液酸化至pH<1,靜置分層,有機相脫溶,得到三酮類化合物。
改善效果
《一種三酮類化合物的合成方法》的三酮類化合物(磺草酮、硝草酮)合成方法,所用的催化劑毒性小,對環境友好,產品收率較高,適宜工業化生產。
技術領域
《一種三酮類化合物的合成方法》涉及一種三酮類化合物的合成方法,尤其是磺草酮、硝草酮的合成方法。
權利要求
1.一種如式(I)所示的三酮類化合物的合成方法,其特徵在於所述合成方法為:在有機溶劑中,式(II)所示的烯醇酯在鹼性試劑和重排催化劑的作用下發生重排反應,反應完畢後所得反應液經酸化、分離得到所述的三酮類化合物;所述的重排催化劑為嘌呤、6-氯嘌呤或6-羥基嘌呤;
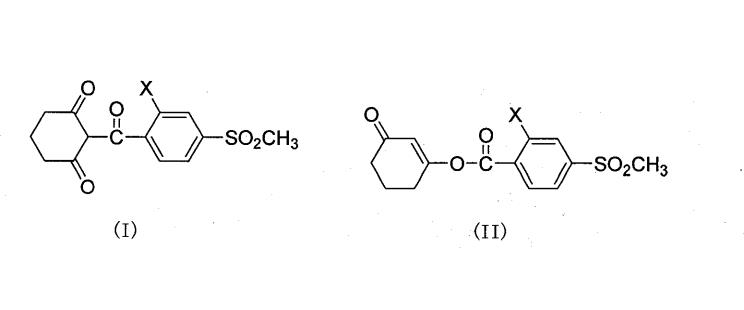
式(I)或式(II)中,X為Cl或NO2。
2.如權利要求1所述的三酮類化合物的合成方法,其特徵在於所述的重排催化劑的加入摩爾數為烯醇酯摩爾數的1~5%。
3.如權利要求1或2所述的三酮類化合物的合成方法,其特徵在於所述的有機溶劑選自下列之一:1,2-二氯乙烷、氯代苯、氯仿、二氯甲烷、三氟甲苯、鄰氯甲苯,間氯甲苯,對氯甲苯、乙腈、甲苯、乙酸乙酯。
4.如權利要求1或2所述的三酮類化合物的合成方法,其特徵在於所述的有機溶劑的體積用量為1~5升/摩爾烯醇酯。
5.如權利要求1或2所述的三酮類化合物的合成方法,其特徵在於所述的鹼性試劑選自下列之一:三乙胺、碳酸鉀、碳酸鈉、三正丙胺、二異丙胺。
6.如權利要求1或2所述的三酮類化合物的合成方法,其特徵在於所述的烯醇酯和鹼性試劑的摩爾比為1∶1~10。
7.如權利要求1或2所述的三酮類化合物的合成方法,其特徵在於所述的重排反應在溫度20~80℃下進行,反應時間為2~5小時。
8.如權利要求7所述的三酮類化合物的合成方法,其特徵在於所述的重排反應在溫度30~50℃下進行。
9.如權利要求1所述的三酮類化合物的合成方法,其特徵在於所述的酸化、分離為:重排反應完成後,加入質量濃度為5~37%的鹽酸將反應液酸化至pH<1,靜置分層,有機相脫溶,得到三酮類化合物。
實施方式
- 實施例1
磺草酮的製備:在三口燒瓶中,加入328克(1.0摩爾)3-(2-氯-4-甲碸基苯甲醯氧基)-2-環己烯-1-酮、2升1,2-二氯乙烷、222.6克(2.2摩爾)三乙胺、6.8克(0.05摩爾)6-羥基嘌呤,攪拌,加熱,反應溫度在45~50℃,反應5小時,冷卻,用10%鹽酸酸化,使pH值<1,靜止分層,有機相脫溶,得到278克磺草酮,收率85%。
- 實施例2
硝草酮的製備:在三口燒瓶中,加入339克(1.0摩爾)3-(2-硝基-4-甲碸基苯甲醯氧基)-2-環己烯-1-酮、2.5升1,2-二氯乙烷、222.6克(2.2摩爾)三乙胺、6.8克(0.05摩爾)6-羥基嘌呤,攪拌,加熱,反應溫度在45~50℃,反應5小時,冷卻,用10%鹽酸酸化,使pH值<1,靜止分層,有機相脫溶,得到284.6克硝草酮,收率84%。
- 實施例3-5
參考實施例1的方法,改變三乙胺的用量,其他反應條件與實施例1相同,得到磺草酮,結果如表1。
實施例 | 三乙胺(摩爾) | 收率(%) |
3 | 1.0 | 62 |
4 | 5.0 | 83 |
5 | 10.0 | 84 |
- 實施例6-8
參考實施例1的方法,改變反應的溫度和反應的時間,其他反應條件與實施例1相同,得到磺草酮,結果如表2。
實施例 | 反應溫度(℃) | 反應時間(小時) | 收率(%) |
6 | 20-25 | 5 | 64 |
7 | 30-35 | 4 | 85 |
8 | 75-80 | 2 | 81 |
- 實施例9-12
參考實施例1的方法,用不同的鹼性試劑替代三乙胺,鹼化試劑的摩爾用量保持不變,其他反應條件與實施例1相同,得到磺草酮,結果如表3。
實施例 | 鹼性試劑 | 摩爾用量(摩爾) | 收率(%) |
9 | 碳酸鉀 | 2.2 | 73 |
10 | 碳酸鈉 | 2.2 | 65 |
11 | 三正丙胺 | 2.2 | 79 |
12 | 二異丙胺 | 2.2 | 72 |
- 實施例13-20
參考實施例1的方法,改變反應所用重排催化劑,其他反應條件與實施例1相同,得到磺草酮,結果如表4。
實施例 | 鹼性試劑 | 質量(克) | 摩爾數 | 收率(%) |
13 | 嘌呤 | 6.0 | 0.05 | 69 |
14 | 嘌呤 | 3.6 | 0.03 | 58 |
15 | 嘌呤 | 1.2 | 0.01 | 32 |
16 | 6-氯嘌呤 | 7.7 | 0.05 | 81 |
17 | 6-氯嘌呤 | 4.6 | 0.03 | 73 |
18 | 6-氯嘌呤 | 1.5 | 0.01 | 48 |
19 | 6-羥基嘌呤 | 4.1 | 0.03 | 78 |
20 | 6-羥基嘌呤 | 1.4 | 0.01 | 62 |
- 實施例21-25
參考實施例1的方法,用不同的有機溶劑替代1,2-二氯乙烷,其他反應條件與實施例1相同,得到磺草酮,結果如表5。
實施例 | 有機溶劑 | 用量(升) | 收率(%) |
21 | 氯代苯 | 1 | 73 |
22 | 三氟甲苯 | 2 | 85 |
23 | 乙腈 | 3 | 79 |
24 | 乙酸乙酯 | 4 | 84 |
25 | 甲苯 | 5 | 81 |
- 實施例26-28
參考實施例2的方法,改變三乙胺的用量,其他反應條件與實施例2相同,得到硝草酮,結果如表6。
實施例 | 三乙胺(摩爾) | 收率(%) |
26 | 1.0 | 57 |
27 | 5.0 | 85 |
28 | 10.0 | 82 |
- 實施例29-31
參考實施例2的方法,改變反應的溫度和反應的時間,其他反應條件與實施例2相同,得到硝草酮,結果如表6。
實施例 | 反應溫度(℃) | 反應時間(小時) | 收率(%) |
29 | 20-25 | 5 | 66 |
30 | 30-35 | 4 | 85 |
31 | 75-80 | 2 | 80 |
- 實施例32-35
參考實施例2的方法,用不同的鹼性試劑替代三乙胺,鹼化試劑的摩爾用量保持不變,其他反應條件與實施例2相同,得到硝草酮,結果如表7。
實施例 | 鹼性試劑 | 摩爾用量(摩爾) | 收率(%) |
32 | 碳酸鉀 | 2.2 | 70 |
33 | 碳酸鈉 | 2.2 | 62 |
34 | 三正丙胺 | 2.2 | 81 |
35 | 二異丙胺 | 2.2 | 69 |
- 實施例36-43
參考實施例2的方法,改變反應所用重排催化劑,其他反應條件與實施例2相同,得到硝草酮,結果如表9。
實施例 | 重排催化劑 | 質量(克) | 摩爾數 | 收率(%) |
36 | 嘌呤 | 6.0 | 0.05 | 69 |
37 | 嘌呤 | 3.6 | 0.03 | 53 |
38 | 嘌呤 | 1.2 | 0.01 | 37 |
39 | 6-氯嘌呤 | 7.7 | 0.05 | 82 |
40 | 6-氯嘌呤 | 4.6 | 0.03 | 76 |
41 | 6-氯嘌呤 | 1.5 | 0.01 | 47 |
42 | 6-羥基嘌呤 | 4.1 | 0.03 | 74 |
43 | 6-羥基嘌呤 | 1.4 | 0.01 | 56 |
- 實施例44-48
參考實施例2的方法,用不同的有機溶劑替代1,2-二氯乙烷,其他反應條件與實施例2相同,得到硝草酮,結果如表10。
實施例 | 有機溶劑 | 用量(升) | 收率(%) |
44 | 氯代苯 | 1 | 75 |
45 | 三氟甲苯 | 2 | 83 |
46 | 乙腈 | 3 | 80 |
47 | 乙酸乙酯 | 4 | 81 |
48 | 甲苯 | 5 | 82 |
榮譽表彰
2018年12月20日,《一種三酮類化合物的合成方法》獲得第二十屆中國專利獎優秀獎。

